Отек мозга как сделать
Добавил пользователь Morpheus Обновлено: 18.09.2024
Что говорят цифры?
В республике изданы рекомендации по ведению пациентов с ЧМТ, утвержденные Министерством здравоохранения. Активное участие в их подготовке принимали заместитель директора по научной работе РНПЦ неврологии и нейрохирургии, член-корреспондент НАН Беларуси, профессор Юрий Шанько, доцент кафедры неврологии и нейрохирургии БелМАПО Андрей Танин. Но и сегодня работа по поиску новых методик лечения ЧМТ продолжается.
Важно отметить, что все пациенты с ЧМТ нуждаются в госпитализации независимо от степени тяжести. При легкой и средней степени специализированная медпомощь оказывается в нейрохирургических отделениях, а при тяжелой (8–9 баллов по шкале комы Глазго) — в палате интенсивной терапии. Причем никакие письменные отказы самих пациентов или их родственников не являются юридическими документами для того, чтобы не госпитализировать пациентов данной категории.
Достаточно большое количество, около 3 000 пациентов с травмой различной степени проходят лечение в данных клиниках города. Из них с тяжелой травмой — примерно по 500 в каждой. Общие цифры значительные. Вместе с тем стоит учитывать, что эта статистика не полностью достоверна, поскольку треть пациентов погибают на догоспитальном этапе. К слову, когда в 2008–2009 годах в республике специалисты под руководством профессора Юрия Шанько начали активно заниматься проблемой ЧМТ, удалось снизить в целом уровень летальности. Так, если средний общемировой показатель в данной группе пациентов составляет 30 %, то в некоторые годы в Беларуси он достигал 24–25 %. И эти цифры абсолютно достоверны.
В настоящее время в клинической практике применяется ряд специфических методов стационарного лечения пациентов с тяжелыми ЧМТ.
Профилактическая гипотермия. Считается, что этот метод при ЧМТ может оказывать нейропротекторное действие помимо способности снижать внутричерепное давление (ВЧД). Вместе с тем переохлаждение связано с риском развития иммуносупрессии, коагулопатии, нарушения сердечного ритма у ряда пациентов.
Дренирование спинномозговой жидкости. Сегодня применяются различные варианты наружного вентрикулярного дренирования. Эти системы могут использоваться для непрерывного контроля ВЧД и периодического дренажа ликвора для снижения давления или постоянного выведения спинномозговой жидкости при прерывистом мониторинге ВЧД либо непрерывного дренирования ликвора и измерения ВЧД с помощью различного типа датчиков.
Анестезия, аналгезия и седация. Часто применяются в остром периоде тяжелой ЧМТ, в том числе для профилактики и контроля внутричерепной гипертензии и судорожных припадков. Барбитураты, вероятно, предотвращают ненужные движения пациента, сопротивление аппарату ИВЛ, кашель, подавляют метаболизм и стабилизируют тонус мозговых сосудов. Также данные группы лекарственных средств могут улучшать насыщение мозга кислородом и предотвращать негативные последствия травмы. Нейропротективный эффект достигается за счет ингибирования радикалов кислорода и перекисного окисления липидов клеточных мембран.
Стероиды. Не рекомендовано их использование для улучшения результата или снижения ВЧД. Высокие дозы метилпреднизолона у пациентов с тяжелой ЧМТ ассоциированы с ростом летальных исходов.
Питание. Рекомендуется для снижения летальности к 5–7-м суткам после травмы с целью достижения основного возмещения калорий. Кормление через тонкокишечный зонд позволяет снизить частоту ИВЛ-ассоциированной пневмонии. Это достаточно затратный пункт в лечении данной группы пациентов. Необходимы адекватные питательные смеси и четкий подсчет калоража для каждого с учетом индивидуальных особенностей.
К тому же это энергоемкий процесс для медперсонала. Само по себе питание пациентов с тяжелой ЧМТ, на мой взгляд, требует активного изучения, особенно в острейшем периоде ЧМТ.
Профилактика инфицирования. Превентивная антибиотикотерапия при замене катетера для измерения ВЧД снижает риск инфицирования, но повышает вероятность появления резистентных микроорганизмов. При тяжелой ЧМТ пациенты восприимчивы к инфекции также из-за необходимости ИВЛ. По некоторым данным, частота ИВЛ-ассоциированных пневмоний у данной категории может достигать 40 % и связана с продолжительностью респираторной поддержки.
Ранняя трахеотомия рекомендуется для сокращения длительности ИВЛ, когда общая польза превышает вред осложнений. Несмотря на это, к постановке трахеостомической канюли в каждом отдельном случае необходимо подходить индивидуально.
Профилактика тромбоза глубоких вен. Риск развития этой патологии при ЧМТ возрастает, несмотря на механическую и фармакологическую профилактику. Также вероятность венозной тромбоэмболии повышается с увеличением тяжести травмы. Превентивно могут использоваться препараты низкомолекулярного гепарина или низкие дозы нефракционированного гепарина в сочетании с механическими методами. Однако это связано с высоким риском внутричерепных кровоизлияний. По данному направлению в лечении ведется непрерывная работа.
Профилактика судорог. Необходимо помнить, что противосудорожные препараты с профилактической целью у пациентов с тяжелой ЧМТ не применяются. На частоту и глубину судорожных приступов при профилактическом применении они не влияют. Однако важно правильно оценить преимущества, эффективность и потенциальный ущерб.
Также у пациентов с тяжелой ЧМТ, у которых наблюдается выраженный отек мозга, используется нейрохирургическая тактика — декомпрессивная краниэктомия, получившая широкое применение в последние годы.
Несмотря на то что по существу отек головного мозга (ОГМ) является защитной реакцией на различные повреждающие факторы, при несвоевременных диагностике
- Вазогенный обусловлен повреждением гематоэнцефа-лического барьера (ГЭБ) и его повышенной проницаемостью для компонентов плазмы крови — в первую очередь ионов натрия и белка.
- Цитотоксический характеризуется перемещением жидкости из межклеточного во внутриклеточное пространство ткани мозга с сохранением проницаемости ГЭБ для белка. Прежде всего он развивается из-за сниженного поступления кислорода, перехода на анаэробный путь обмена веществ, нарушения работы ионных насосов, избыточного поступления в клетки мозга ионов натрия и воды. Если не купировать цитотоксический отек в течение 6–8 часов, то он перейдет в вазогенный. Кстати, при втором, как правило, в большей степени страдает белое вещество, а при первом — серое.
- Гидростатический возникает на фоне блокады путей оттока ликвора. Бывает двух видов: арезорбтивный, обусловленный нарушением всасывания ликвора в пахионовых грануляциях венозных синусов черепа, и окклюзионный, которому предшествует возникновение препятствий на пути ликвора в желудочковую систему.
- Осмотический развивается на фоне нарушения осмотических градиентов внутриклеточного и внутрисосудистого секторов при неповрежденном ГЭБ.
В начале формирования ОГМ специфическая симптоматика отсутствует. Клиническую картину определяет механическое раздражение болевых рецепторов мозговой оболочки и внутримозговых сосудов под действием высвобождаемых свободных радикалов и за счет повышенного ВЧД. Как результат — общемозговые симптомы и менингеальный синдром. Постепенно проявляются очаговые симптомы, прогрессирующие в дальнейшем. Это связано с нарушением функции определенных структур мозга из-за гипоксии и отека, а также со сдавлением нервных центров на фоне увеличенного объема мозга. Разрозненные межнейронные связи и возникшие очаги гиперактивных нейронов приводят к судорожному синдрому.
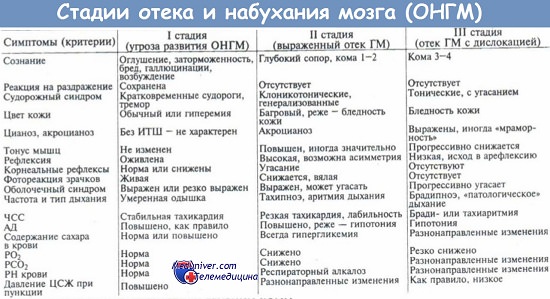
Основой диагностики ОГМ является степень угнетения сознания, для определения которой используется шкала комы Глазго. Клиническая картина традиционно включает три стадии:
- общемозговой синдром, проявления которого характерны для повышенного ВЧД;
- диффузное рострокаудальное нарастание неврологических симптомов;
- дислокация мозговых структур.
Для выявления достоверных признаков ОГМ проводят МРТ и КТ. В данных случаях на изображениях отмечается пониженная плотность структур. Повторные исследования позволяют определить изменение объема головного мозга и зоны отека, формы и размера желудочков, сопутствующую деформацию мозговых структур. Благодаря этому можно в динамике контролировать выраженность процесса.
- после осмотра наладить мониторирование основных витальных функций — кровообращения, дыхания и оксигенации, нейромониторинг в условиях отделения интенсивной терапии и реанимации;
- провести рентгенографию черепа, грудной клетки, а также УЗИ сердца и других органов (по показаниям);
- выполнить КТ или МРТ головного мозга. Исключение — наличие у пациента противопоказаний, в том числе нестабильной гемодинамики, некупированного инфекционно-токсического шока;
- выполнить общие анализы крови и мочи, а также биохимический анализ крови, чтобы определить уровни С-реактивного белка, прокальцитонина, глюкозы, мочевины, креатинина, билирубина, АЛТ, АСТ, ГГТП, ЩФ, холестерина, исследовать кислотно-основное состояние крови и содержание натрия и калия в ней;
- организовать консультацию врача-окулиста с осмотром глазного дна. По результатам этого, а также с учетом данных МРТ и/или КТ головного мозга и клинической симптоматики можно принимать решение о люмбальной пункции;
- исследовать кровь на гемокультуру, выполнить общий анализ ликвора и на хлориды, на глюкозу, его бактериологическое исследование, ПЦР-диагностику для выявления основных возбудителей гнойных и серозных менингитов;
- организовать осмотр врачом-неврологом — каждые 4 часа с определением неврологического статуса и оценкой очаговых, глазодвигательных, зрачковых и бульбарных расстройств.
При признаках дислокации прежде всего необходима ранняя ИВЛ кислородно-воздушной смесью. Вторая важная составляющая лечения — дегидратация, которую следует проводить, учитывая особенности патологического процесса и соблюдая принцип поддержания нормоволемии.
Терапия цитотоксического ОГМ. Данным пациентам требуется назначение маннитола или других осмодиуретиков. Но нужно отметить, что такая терапия в ряде случаев эффективна только в первые 48–72 часа.
Чтобы поддержать должный уровень церебрального перфузионного давления, следует придерживаться концепции Рознера, преду-сматривающей сохранение артериальной гипертензии, — проведение инфузионной терапии, гиперволемии и назначение вазопрессоров. При таком подходе сохраняются механизмы ауторегуляции мозгового кровообращения, отсутствуют повреждения ГЭБ, но при условии, что гипертензия не выходит за пределы ауторегуляции у конкретного пациента.
Кроме того, положительное действие оказывает барбитуровый наркоз, который обеспечивает выраженный противоотечный эффект.
Терапия вазогенного ОГМ. Показано применение препаратов ангиопротекторного действия. Особое место в данной группе принадлежит лизина эсцинату в комплексе с маннитолом, восстанавливающему упругоэластические свойства сосудистой стенки. Он регулирует процессы трансмембранного массопереноса, за счет чего усиливается реабсорбция и уменьшается гидратация интерстициального сектора.
Также следует отметить фармакологическую защиту мозга. Для этого применяются антиоксиданты, которые восстанавливают метаболизм мозговой ткани (актовегин, глиатилин, мексидол и другие).
Подводя итог, можно сказать, что в лечении ЧМТ и ОГМ еще остаются белые пятна. Дальнейшее изучение этой проблемы позволит улучшить прогнозы и снизить летальность у данной категории пациентов. В Беларуси сегодня разрабатываются новые методики лечения тяжелой ЧМТ в условиях отделения реанимации и интенсивной терапии с применением клеточных технологий. Стоит надеяться, что скоро они будут внедрены в клиническую практику.
Опухоль головного мозга – под этим термином понимается группа новообразований головного мозга. Они могут быть как доброкачественные, так и злокачественные. Возникновение такой патологии возможно в результате начала неконтролируемого деления клеток или метастазирования из опухолевого очага другого органа.
В зависимости от этого принято выделять:
- первичную опухоль – как результат деления клеток, которые в прошлом были нормальными;
- вторичную – возникающую в результате метастазирования.
Так же существует деление в зависимости от тканей, в которых возникает новообразование:
- нейроэпителиальная – источником опухоли являются непосредственно ткани самого мозга;
- оболочечная – формируется клетками мозговых оболочек;
- образование черепных нервов;
- опухоль гипофиза;
- метастазовая опухоль – в результате метастазирования из вне мозгового очага.
Симптомы
Клиническая картина опухоли головного мозга становится ярче по мере роста размеров самого новообразования. Она обуславливается давлением опухоли на ткань головного мозга, либо нарушениями в работе нервных структур.
Характерны следующие симптомы:
- острая головная боль, которая слабо купируется приемом анальгетиков;
- тошнота и рвота, не связанные с приёмом пищи;
- головокружение и потери сознания;
- судороги;
- ухудшение концентрации внимания и памяти;
- психоэмоциональная нестабильность;
- быстрая утомляемость и повышенная сонливость;
- нарушение двигательных и чувствительных функций;
- расстройство речи и зрения;
- потеря слуха.
Диагностика
Диагноз опухоли головного мозга труден в своей постановке и требует ряда подтверждающих его исследований. К ним относятся:
- КТ и МРТ;
- электроэнцефалография;
- спинномозговая пункция;
- биопсия опухоли с последующим гистологическим исследованием.
Лечение
Подход к лечению опухоли головного мозга должен быть комплексным в связи со всей тяжестью данного состояния.
В качестве основного метода лечения используется хирургическое вмешательство. Однако в зависимости от места расположения образования или слишком больших его размеров операция становится не всегда возможной. В такой практике часто применяют лазерные и ультразвуковые методы для удаления опухоли.
Также для уменьшения размеров образования и предотвращения его разрастания применяются лучевая терапия и химиотерапия. Курс данных мероприятий расписывается для каждого больного индивидуально в зависимости от тяжести состояния и природы опухоли.
Консервативная терапия при этом заболевании назначается для улучшения качества жизни больного и носит вспомогательный характер.
Отек головного мозга — стремительно развивающееся накопление жидкости в церебральных тканях, без оказания адекватной медицинской помощи приводящее к смертельному исходу. Основу клинической картины составляет постепенно или быстро нарастающее ухудшение состояния больного и углубление расстройств сознания, сопровождающееся менингеальными знаками и мышечной атонией. Подтверждают диагноз данные МРТ или КТ головного мозга. Дополнительное обследование осуществляется для поиска причины отека. Терапия начинается с дегидратации и поддержания метаболизма церебральных тканей, сочетается с лечением причинного заболевания и назначением симптоматических препаратов. По показаниям возможно срочное (декомпрессионная трепанация, вентрикулостомия) или отсроченное (удаление объемного образования, шунтирование) хирургическое лечение.
Общие сведения
Набухание головного мозга было описано еще в 1865 году Н.И. Пироговым. На сегодняшний день стало понятно, что отек головного мозга не является самостоятельной нозологической единицей, а представляет собой вторично развивающийся патологический процесс, возникающий как осложнение целого ряда заболеваний. Следует отметить, что отек любых других тканей организма — достаточно часто встречающееся явление, совсем не относящееся к ургентным состояниям. В случае головного мозга, отек является жизнеугрожающим состоянием, поскольку, находясь в замкнутом пространстве черепа, церебральные ткани не имеют возможности увеличиваться в объеме и оказываются сдавленными. Вследствие полиэтиологичности отека мозга, в своей практике с ним сталкиваются как специалисты в области неврологии и нейрохирургии, так и травматологи, неонатологи, онкологи, токсикологи.
Причины отека головного мозга
Наиболее часто отек головного мозга развивается при травмировании или органическом поражении его тканей. К таким состояниям относятся: тяжелая ЧМТ (ушиб головного мозга, перелом основания черепа, внутримозговая гематома, субдуральная гематома, диффузное аксональное повреждение, операции на головном мозге), обширный ишемический инсульт, геморрагический инсульт, субарахноидальное кровоизлияние и кровоизлияние в желудочки, первичные опухоли головного мозга (медуллобластома, гемангиобластома, астроцитома, глиома и др.) и его метастатическое поражение. Отек церебральных тканей возможен как осложнение инфекционных заболеваний (энцефалита, менингита) и гнойных процессов головного мозга (субдуральной эмпиемы).
Наряду с внутричерепными факторами к отеку мозга может привести анасарка, возникшая вследствие сердечной недостаточности, аллергические реакции (отек Квинке, анафилактический шок), острые инфекции (токсоплазмоз, скарлатина, свиной грипп, корь, паротит), эндогенные интоксикации (при тяжелом течении сахарного диабета, ОПН, печеночной недостаточности), отравления различными ядами и некоторыми медикаментами.
Патогенез
Основным звеном в развитии церебрального отека выступают микроциркуляторные нарушения. Первоначально они, как правило, возникают в области очага поражения мозговой ткани (участка ишемии, воспаления, травмы, кровоизлияния, опухоли). Развивается локальный перифокальный отек головного мозга. В случаях тяжелого поражения головного мозга, не проведения своевременного лечения или отсутствия должного эффекта последнего, возникает расстройство сосудистой регуляции, ведущее к тотальному расширению церебральных сосудов и подъему внутрисосудистого гидростатического давления. В результате жидкая часть крови пропотевает через стенки сосудов и пропитывает церебральную ткань. Развивается генерализованный отек головного мозга и его набухание.
В описанном выше процессе ключевыми компонентами являются сосудистый, циркуляторный и тканевой. Сосудистым компонентом выступает повышенная проницаемость стенок мозговых сосудов, циркуляторным — артериальная гипертензия и расширение сосудов, которые приводят к многократному повышению давления в церебральных капиллярах. Тканевой фактор заключается в склонности тканей головного мозга при недостаточности кровоснабжения накапливать жидкость.
В ограниченном пространстве черепной коробки 80-85% объема приходится на церебральные ткани, от 5 до 15% — на цереброспинальную жидкость (ликвор), около 6% занимает кровь. У взрослого нормальное внутричерепное давление в горизонтальном положении варьирует в пределах 3-15 мм рт. ст. Во время чихания или кашля оно ненадолго поднимается до 50 мм рт. ст., что не вызывает расстройств функционирования ЦНС. Отек головного мозга сопровождается быстро нарастающим повышением внутричерепного давления за счет увеличения объема церебральных тканей. Происходит сдавление сосудов, что усугубляет микроциркуляторные нарушения и ишемию мозговых клеток. Вследствие метаболических нарушений, в первую очередь гипоксии, возникает массовая гибель нейронов.
Кроме того, резкая внутричерепная гипертензия может приводить к дислокации нижележащих церебральных структур и ущемлению ствола мозга в большом затылочном отверстии. Нарушение функции находящихся в стволе дыхательного, сердечно-сосудистого и терморегуляторного центров является причиной многих летальных исходов.
Классификация
В связи с особенностями патогенеза отек головного мозга подразделяется на 4 типа: вазогенный, цитотоксический, осмотический и интерстициальный. Самым часто встречающимся типом является вазогенный отек головного мозга, в основе которого лежит повышение проницаемости гематоэнцефалического барьера. В патогенезе основную роль играет переход жидкости из сосудов в белое мозговое вещество. Вазогенный отек возникает перифокально в зоне опухоли, абсцесса, ишемии, оперативного вмешательства и т. п.
Цитотоксический отек мозга является результатом дисфункции глиальных клеток и нарушений в осморегуляции мембран нейронов. Развивается преимущественно в сером мозговом веществе. Его причинами могут выступать: интоксикации (в т. ч. отравление цианидами и угарным газом), ишемический инсульт, гипоксия, вирусные инфекции.
Осмотический отек головного мозга возникает при повышении осмолярности церебральных тканей без нарушения работы гематоэнцефалического барьера. Возникает при гиперволемии, полидипсии, утоплении, метаболических энцефалопатиях, неадекватном гемодиализе. Интерстициальный отек появляется вокруг церебральных желудочков при пропотевании через их стенки жидкой части ликвора.
Симптомы отека головного мозга
Ведущим признаком отека мозга является расстройство сознания, которое может варьировать от легкого сопора до комы. Нарастание глубины нарушения сознания свидетельствует о прогрессировании отека. Возможно, что дебютом клинических проявлений будет потеря сознания, отличающаяся от обычного обморока своей длительностью. Зачастую прогрессирование отека сопровождается судорогами, которые через короткий промежуток времени сменяются мышечной атонией. При осмотре выявляются характерные для менингита оболочечные симптомы.
В случаях, когда отек головного мозга возникает на фоне хронической или постепенно развивающейся острой церебральной патологии, сознание больных в начальном периоде может быть сохранено. Тогда основной жалобой выступает интенсивная головная боль с тошнотой и рвотой, возможны двигательные нарушения, зрительные расстройства, дискоординация движений, дизартрия, галлюцинаторный синдром.
Диагностика отека мозга
Заподозрить отек мозга неврологу позволяет прогрессирующее ухудшение состояния пациента и нарастание нарушения сознания, сопровождающиеся менингеальными симптомами. Подтверждение диагноза возможно при помощи КТ или МРТ головного мозга. Проведение диагностической люмбальной пункции опасно дислокацией церебральных структур со сдавлением мозгового ствола в большом затылочном отверстии. Сбор анамнестических данных, оценка неврологического статуса, клинический и биохимический анализ крови, анализ результатов нейровизуализирующего исследования — позволяют сделать заключение относительно причины отека мозга.
Поскольку отек мозга является угрентным состоянием, требующим неотложной медицинской помощи, его первичная диагностика должна занимать минимум времени и проводиться в стационарных условиях на фоне лечебных мероприятий. В зависимости от ситуации она осуществляется в условиях реанимационного отделения или отделения интенсивной терапии.
Лечение отека головного мозга
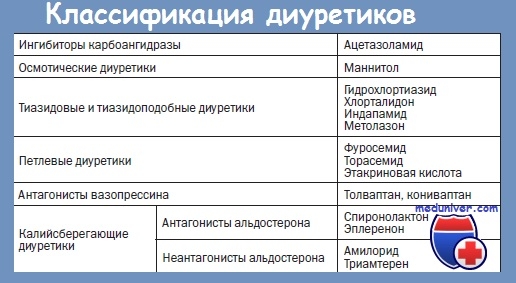
Приоритетными направлениями в терапии отека мозга выступают: дегидратация, улучшение церебрального метаболизма, устранение первопричины отека и лечение сопутствующих симптомов. Дегидратационная терапия имеет целью выведение избытка жидкости из церебральных тканей. Она осуществляется путем внутривенных инфузий маннита или других осмотических диуретиков с последующим назначением петлевых диуретиков ( торасемида, фуросемида). Дополнительное введение 25% р-ра магния сульфата и 40% р-ра глюкозы потенцирует действие диуретиков и снабжает церебральные нейроны питательными веществами. Возможно применение L-лизина эсцината, который обладает способностью выводить жидкость, хотя и не является мочегонным препаратом.
С целью улучшения церебрального метаболизма проводится оксигенотерапия (при необходимости — ИВЛ), местная гипотермия головы, введение метаболитов (мексидола, кортексина, цитиколина). Для укрепления сосудистой стенки и стабилизации клеточных мембран применяют глюкокортикостероиды (преднизолон, гидрокортизон).
В зависимости от этиологии отека мозга в его комплексное лечение включают дезинтоксикационные мероприятия, антибиотикотерапию, удаление опухолей, ликвидацию гематом и участков травматического размозжения головного мозга, шунтирующие операции (вентрикулоперитонеальное дренирование, вентрикулоцистерностомию и др.). Этиотропное хирургическое лечение, как правило, проводят только на фоне стабилизации состояния пациента.
Симптоматическая терапия направлена на купирование отдельных проявлений заболевания, осуществляется путем назначения противорвотных средств, антиконвульсантов, обезболивающих препаратов и т. п. По показаниям в ургентном порядке с целью уменьшения внутричерепного давления нейрохирургом может быть проведена декомпрессивная трепанация черепа, наружное вентрикулярное дренирование, эндоскопическое удаление гематомы.
Прогноз
В начальной стадии отек мозга представляет собой обратимый процесс, по мере прогрессирования он приводит к необратимым изменениям мозговых структур — гибели нейронов и деструкции миелиновых волокон. Быстрое развитие указанных нарушений обуславливает то, что полностью ликвидировать отек с 100% восстановлением мозговых функций удается лишь при его токсическом генезе у молодых и здоровых пациентов, вовремя доставленных в специализированное отделение. Самостоятельная регрессия симптомов наблюдается лишь при горном отеке мозга, если удалась своевременная транспортировка больного с высоты, на которой он развился.
Однако в подавляющем большинстве случаев у выживших пациентов наблюдаются остаточные явления перенесенного отека головного мозга. Они могут значительно варьировать от малозаметных окружающим симптомов (головной боли, повышенного внутричерепного давления, рассеянности, забывчивости, нарушений сна, депрессии) до выраженных инвалидизирующих расстройств когнитивных и двигательных функций, психической сферы.
Данный вид медицинской помощи должен осуществляться в отделениях реанимации и интенсивной терапии и быть построен на нижеприведенных принципах лечения отека головного мозга (Ш. Ш. Шамансуров и др., 1995).
Коррекция нарушения дыхания и сердечной деятельности. В зависимости от степени поражения ЦНС и тяжести состояния больных с тяжелыми формами отека, нарушения дыхания и сердечной деятельности могут быть первичными и вторичными. При их коррекции используются стандартные методики.
Патогенетическая терапия отека направлена, в первую очередь, на устранение гипоксии как наиболее неблагоприятного фактора, способствующего развитию отека. Эта терапия направлена на нормализацию гемодинамики, ликвородинамики, метаболизма нейронов.
Иными словами, терапия нацелена на коррекцию основных патофизиологических механизмов (циркуляторных, васкуляторных, тканевых), участвующих в развитии отека мозга.
Коррекция гематоциркуляторных нарушений включает:
1. Лечебные мероприятия, направленные на нормализацию показателей системной гемодинамики. Для поддержания адекватной перфузии головного мозга необходимо сконцентрировать усилия на нормализацию системного артериального давления путем рационального назначения вазоактивных (дилататоров или констрикторов) препаратов быстрого действия (клофелин, дибазол или кофеин бензоат натрия и др.).
2. Назначение блокаторов кальциевых каналов. Эти препараты способствуют улучшению мозговой циркуляции, уменьшают накопление тканевых гормонов и тем самым обеспечивают устойчивость мозга к гипоксии. К ним относятся верапамил и его производные (финоптин, изоптин), нимодипин, лидофлазин, нифедипин (коринфар), фендилин (сензид), циннаризин (стугерон).
3. Усиление микроциркуляции мозга путем назначения препаратов, нормализующих тонус сосудов и реологические свойства крови. Здесь целесообразно использовать следующие вазоактивные препараты: кавинтон, ксантинола никотинат (компламин, теоникол, ксарин), эуфиллин, трентал (агапурин), дипиридамол (курантил), галидор, сермион (редергин), реополиглюкин, гепарин, индометацин (вольтарен, ортофен, аспирин).
При коррекции васкулярного (барьерного) фактора назначают следующие препараты:
• глюкокортикоиды (назначается либо преднизолон, либо дексаметазон);
• ингибиторы протеолитических ферментов. Они инактивируют тканевые гормоны воспаления при отеке головного мозга (гистамин, брадикинин, трипсин и др.). Для этой цели в/в вводится контрикал в дозе 1-10 тыс. ЕД/кг, гордокс — 12-15 тыс. ЕД/кг, аминокапроновая кислота — 200—300 мг/кг/24 ч. Курс лечения ингибиторами протеолитических ферментов, как правило, не превышает 5—7 дней;
• препараты, стабилизирующие клеточные мембраны и ангиопротекторы. Назначение последних способствует уменьшению проницаемости стенки сосудов мозга. К этой группе препаратов относятся дицинон, троксевазин, гливенол, венорутон, аскорутин;
• блокаторы кальциевых каналов (о назначении этих препаратов сказано выше);
• иммунокорригирующие препараты. В качестве иммуносупрессоров чаще всего используются стероидные гормоны (кортизон, гидрокортизон, преднизолон).
Иммуностимулирующая терапия включает применение тимозина, Т-активина, В-активина, тимогена, левамизола, пропермила, витаминов группы В.
Коррекция тканевого фактора включает:
• обеспечение адекватной оксигенации крови. Достигается восстановлением и поддержанием проходимости дыхательных путей, проведением постоянной ингаляции увлажненного кислорода, применением в некоторых случаях гипербарической оксигенации и ИВЛ;
• нормализацию метаболических процессов в нейронах головного мозга. Для этой цели используются ноотропы (ноотропил, пирацетам, ами-налон, церебролизин, энцефабол, пантогам, пиридитол и др.).
Коррекция нарушений водно-электролитного обмена и дегидратационная терапия. Важным патогенетическим направлением лечения отека мозга является назначение дегидратационной терапии:
• осмотические диуретики ( глицерин, маннитол, сорбитол и др.);
• салуретики (лазикс, фуросемид и др.);
• кортикостероиды (гидрокортизон, преднизолон). Следует указать, что действие стероидов на отек мозга развивается медленно — эффект обнаруживается не раньше, чем через 24 ч после первого введения препарата. Они более эффективны при локальных отеках мозга; кроме этого необходимо знать, что длительное применение стероидов, особенно в малых дозировках, может вызвать увеличение объема мозга и ВЧД;
• барбитураты (внутримышечно 10% раствор тиопентала натрия в дозе 10 мг/кг каждые 3 ч, суточная доза детям до 80 мг/кг).
Хирургическая коррекция отека мозга. Когда этиологический фактор отека мозга представлен экспансивным процессом (гематома, опухоль, абсцесс и т. д.), он может быть прерван только с помощью нейрохирургического вмешательства.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

