Как сделать искусственные органы
Обновлено: 05.07.2024
Великим достижением начала XX века было то, что люди научились культивировать клетки млекопитающих вне организма. Вначале это культивирование происходило в висячей капле, без прикрепления клеток к поверхности. То есть капля свешивалась, и в этой капле, ни к чему не прикрепленные, плавали клетки. Потом техника стала совершенствоваться, и мы научились растить клетки в чашках Петри, рассматривая в микроскоп, что с ними происходит. Это достижение дало мощный импульс развитию клеточной биологии и генетики.
С развитием технологий у исследователей появилась возможность изучать уже не плоские культуры, а трехмерные или, как их стали сейчас называть, органоиды. Подобное направление появилось совсем недавно, буквально в последние пять лет.
В 2013 году австрийскими учеными было опубликовано пионерское исследование, в котором описывалось выращивание трехмерной структуры, напоминающей головной мозг.
Эта структура достигла размера в несколько миллиметров и получила название церебрального органоида. Исследователи работали со стволовыми клетками человека и, как и многие, выращивали их в чашке, на плоской поверхности, но потом решили оторвать от поверхности и перенести клетки в плавающую, суспензионную культуру. Для этого они поместили их в биореактор, который все время перемешивал делящиеся клетки и не давал им прикрепиться к поверхности. Группы делящихся клеток формировали маленькие сферы, а потом, что удивительно, эти сферы стали все больше и больше увеличиваться в размерах. Оказалось, что в биореакторе — в условиях, когда мы активно меняем культуральную среду вокруг растущей ткани и тем самым обеспечиваем клетки кислородом и питанием — в этих растущих сфероидах протекают процессы, сходные с природными. Там идет специализация клеток и формирование структуры органа.
Ученые использовали в своих экспериментах эмбриональные стволовые клетки, в которых во время специализации в нейроны, конечно же, проявляется и потенциал формирования всей структуры мозга. И когда нейрональной культуре предоставили возможность расти в трехмерном пространстве, получились зачатки мозга. Более детальный анализ этих органоидов показал, что в них происходят процессы, похожие на те, что происходят в мозге человека. Удивительным образом получилось, что вне человеческого организма (а исследователи использовали и эмбриональные стволовые, и репрограммированные стволовые клетки в качестве источника нейронов) сформировались структуры, соответствующие такому уникальному органу, как мозг. Более того, в случае использования репрограммированных клеток от больных микроцефалией (болезнью недоразвитого мозга) в культуре образовывались недоразвитые церебральные органоиды.
Таким образом, сегодня мы уже можем выращивать некоторые небольшие органоиды, которые будут повторять структуры отдельных органов человека. Тем самым мы получаем возможность более детально изучать какие-то процессы или что-то моделировать.
Немного по-другому был получен органоид кишечника. В качестве исходных клеток, как и в предыдущем случае, были взяты плюрипотентные стволовые клетки человека. Ученые определенным образом воздействовали на них с помощью ростовых факторов, а потом, дорастив до определенной стадии, поняли, что в чашке или биореакторе они не смогут хорошо расти, так как стали уже слишком большими и питательные вещества вовнутрь не проникают. Тогда исследователи решили пойти на такой трюк: они трансплантировали эти зачатки органоидов в лабораторную мышь, и в мышке эти клеточные структуры стали развиваться дальше.
В том месте, куда их трансплантировали, действительно развился кишечник — с криптами, ворсинками и другими необходимыми структурами.
Более того, когда этот кишечник человека, который развился в мышке, заразили Helicobacter pylori — бактерией, которая вызывает язвенную болезнь у человека, — органоид оказался инфицированным и проявил все признаки язвенной болезни.
Таким образом, получилось, что мы, с одной стороны, начали создавать что-то вне человеческого организма в лаборатории, а затем, чтобы получить более адекватную модель, перенесли это в животное, как в биореактор. Но и в этом случае органоид полностью имитировал то, что происходит в организме человека.
Органоиды дают сегодня уникальную возможность использовать их в первую очередь для разработки новых технологий, для поиска новых лекарств, для моделирования тех или иных заболеваний. Это уже относится не столько к области научного знания, сколько к его использованию для разработки определенной технологии создания человеческих органов.
Каждый из нас когда-нибудь задумывался о бренности своего тела. У одних такие мысли появились, когда у них выпал первый молочный зуб, у других — когда они нашли у себя первый седой волос, у третьих — когда кожа стала тонкой и морщинистой, а суставы перестали сгибаться. А что, если можно было бы менять органы, как запчасти в машине? Ожог 80 % поверхности тела — натянем новую кожу, отказал какой-то внутренний орган — не беда, заменим, будет как новенький!

Наши ткани состоят не столько из клеток, прижатых вплотную друг к дружке, сколько из того самого внеклеточного матрикса — будь то коллагеновые волокна или апатитная губка, как, например, в костях.
Эта конференция состоялась еще в 2011 году. Сейчас группа Шая Сокера (докладчика на видео) занимается биосенсорами и платформами скрининга лекарственных веществ на искусственных органах и тканях.
Справедливости ради нужно отметить, что иногда клетки сажают и на биосовместимый полимер. Одним из первых успешных опытов было создание новой легочной артерии: ученые взяли кусок периферической вены и выделили из него клетки, которые могут стать стенкой сосуда.
В случаях с более объемными органами на помощь приходит техника обесклеточивания (децеллюляризации). Здесь и всплывает имя скандально известного хирурга Паоло Маккиарини. Он первым пересадил человеку донорскую трахею, взятую из трупного материала, но пациентка умерла после операции. Есть мнение, что всему виной был обычный бактериальный сепсис, который закончился фатально. Маккиарини провел несколько таких экспериментальных операций, часть из которых прошла без серьезных осложнений, хотя некоторые коллеги называли его деятельность этическим Чернобылем.
Для большинства пациентов искусственная трахея была единственным способом продлить жизнь. При этом они страдали множеством сопутствующих заболеваний, которые сами по себе могли стать фактором, ухудшившим их состояние после трансплантации. Кроме того, одной из претензий этических комитетов к Маккиарини было то, что при каждой операции он применял новую экспериментальную методику: якобы смена способов и материалов для трахеи свидетельствовала о том, что хирург не знал, что делает. Комиссия в своем отчете заявила, что использовать непроверенные методики даже тогда, когда человек мог умереть с высокой степенью вероятности и при любом другом лечении, недопустимо.
К счастью, модели тканей и органов, выращенные на коллагеновом каркасе из донорского материала, можно успешно использовать в доклинических испытаниях лекарственных веществ. Теоретически это даже может дать более точные результаты, чем испытание на клеточной монокультуре.
Что же касается прикладных успехов биотрансплантации, то стоит начать с козырей — бьющегося мышиного сердца. Его вырастили с помощью обесклеточивания с последующим засевом стволовыми клетками:
Конечно, оно пока не способно эффективно качать кровь и сокращается не очень ритмично, но сам принцип выращивания в пробирке сложных органов, состоящих из нескольких типов тканей, уже работает.
В начале статьи мы упоминали механические протезы и их недостатки. Если откажет, например, искусственный клапан сердца, пациенту смогут помочь только в узкоспециализированной клинике — в медицинской литературе описано много случаев заедания створок механического клапана. А вот донорский или искусственно выращенный орган больного сможет спасти любой квалифицированный врач.

Сейчас проходят клинические испытания новые способы лечения небольших структурных дефектов внутренних органов с помощью стволовых клеток. Уже коммерчески доступны ECM-материалы на основе обесклеточенных матриксов мочевых пузырей свиней.
А вот с сердцем, легкими, почками и другими востребованным органами пока что не очень, увы. Большая часть современных разработок в области регенеративной медицины пока что находится лишь на стадии клинических испытаний. И к большому сожалению, если кому-то необходима такая помощь, остается лишь постоянно мониторить сайты крупных западных медцентров, специализирующихся на такого рода вещах.
Клиническое применение искусственных органов в настоящее время ограничено только временным поддержанием функций жизненно важных органов и не обеспечивает многолетнего их функционирования. Более оптимистичная ситуация при замене менее важных органов (органы чувств, кровеносные сосуды, клапаны сердца). Успех конструирования искусственных органов во многом определяется наличием и выбором адекватного биоматериала. Активная разработка новых материалов медицинского назначения привела к тому, что в настоящее время широкий спектр биосовместимых материалов весьма успешно применяют для изготовления различных эндопротезов и устройств, предназначенных для замены десятков (около 40) различных частей человеческого организма.
Для создания тканей и органов применяются в основном синтетические материалы, материалы на основе природных полимеров (хитозан, альгинат, коллаген), а также биокомпозитные материалы
Файлы: 1 файл
Материалы для конструирования искусственных органов.docx
Материалы для конструирования искусственных органов.
Для создания тканей и органов применяются в основном синтетические материалы, материалы на основе природных полимеров (хитозан, альгинат, коллаген), а также биокомпозитные материалы (табл. 3).Таблица 3. Классы биоматериалов, применяемых в тканевой инженерии. Коллаген практически не имеет антигенных свойств. Использованный в качестве матрицы, он разрушается за счет ферментативного гидролиза и структурно замещается собственными белками, синтезируемыми фибробластами. Из коллагена могут быть изготовлены матрицы с заданными свойствами для реконструкции практически любых органов и тканей. Являясь естественным тканевым (межклеточным) белком, он оптимально подходит в качестве носителя культуры клеток, обеспечивая рост и развитие ткани. Альгинат – полисахарид из морских водорослей, может быть использован в качестве матрицы-носителя, однако не обладает достаточной биологической совместимостью и оптимальными механическими свойствами. Обычно он используется в виде гидрогелей для восстановления хрящевой и нервной ткани.
Хитозан – азотсодержащий полисахарид, который является основной составляющей наружного покрова насекомых, ракообразных и паукообразных. Этот биоматериал получают из хитиновых панцирей ракообразных и моллюсков. В настоящее время заслуживает внимания комбинированный по составу препарат – коллагеново-хитозановый комплекс. В ходе лабораторных и клинических исследований была показана его инертность и способность сохранять жизнеспособность клеточной культуры как in vitro, так и in vivo. Этот комплекс разрешен Минздравом РФ в качестве перевязочного, ранозаживляющего средства и уже используется в клинической практике в хирургии и стоматологии
Одними из первых в тканевой инженерии стали применяться биодеградируемые синтетические биоматериалы на основе полимеров органических кислот, например молочной (PLA, полилактат) и гликолевой (PGA, полигликолид). При этом в состав полимера может входить как один тип кислотного остатка, так и их сочетания в различных пропорциях.
Почка была первым органом, для которого был создан искусственный конструктор. В 1940-х годах Кольфом был изобретен аппарат диализа, который стал искусственной заменой почки. Роль этого парного внутреннего органа в функционировании организма велика; почки поддерживают равновесие состава крови, контролируя давление, объем и кислотность крови, регулируя концентрации химических веществ, синтезируя гормоны, и выполняют роль фильтров. Почки могут быть повреждены вследствие наследственных дефектов, а также травм и многих заболеваний. Удаление продуктов обмена и воды почками – это весьма сложный процесс для имитирования. Почечная недостаточность последней степени может быть исправлена посредством диализа или трансплантации донорской почки. Диализ – это одновременная диффузия и фильтрация, отличающиеся от естественной функции почек; этот процесс прост, но весьма эффективен. Диализаторы используют для удаления избыточной жидкости из организма и растворимых продуктов обмена. Обменники (фильтрующие элементы диализатора) должны иметь высокую проницаемость для воды и полярных растворимых веществ, для их изготовления используют производные целлюлозы, пористые волокна из полисульфона, полиметилметакрилата или поликарбонатов. Диализат должен содержать заданные физиологические концентрации ионов и питательных веществ, чтобы исключить потери этих компонентов из организма. Диализ – это эффективный и спасительный раствор, но он не идеален при почечной недостаточности. Аппарат диализа удаляет мочевину и неизрасходованные питательные вещества, такие как вода, сахара и соли из крови, заменяя этим функцию естественной почки. Однако естественная почка также перенаправляет неиспользованные питательные вещества обратно в организм; это процесс, который диализ выполнить не может. В среднем пациент подвергается гемодиализу три раза в неделю в течение 5–6 часов за одно лечение, при этом пациент тратит время, а службы здравоохранения – огромные средства. В ряде исследовательских центров Европы и США начата разработка биоискусственной почки. Созданы модели, которые содержат обычный патрон-гемофильтр и биореакторную камеру с устройством стимуляции почечного канальца, включающее 109 клеток почечного проксимального канальца. Такая биоискусственная почка направляет питательные элементы по трубкам, обложенным почечными клетками, повторно поглощающими полезные питательные вещества и отсылающими их через пористые стеки трубок в кровь. В настоящее время устройство проходит ограниченные клинические испытания. Ученые сумели создать 3D-почку. Для этого больной орган тщательно сканируется, из него берется образец тканей, а на основе этих данных при помощи компьютерных технологий моделируется 3D-изображение новой почки, включая внутреннее строение. Затем специальный трехмерный принтер воссоздает структуру нового органа послойно, согласно запрограммированному образцу, отображающему даже сосуды. Воссоздание продолжается в течение 6-7 часов, затем результаты распечатываются. Основой структуры искусственной почки стали мембраны с полыми волокнами, которые обычно используются в традиционном способе лечения гемодиализом.
Гибридная печень Печень – большой и сложный орган, образованный мультифункциональными клетками, которые в зависимости от локализации и удаления от источника артериальной крови, имеют тысячи функций. Печень регулирует белковый обмен, уровень жиров и углеводов в крови, факторов свертывания крови, синтезирует множество важных для жизнедеятельности химических веществ и очищает кровь от токсинов. Это множество функций пока не удается имитировать с помощью искусственного органа. Наиболее успешно в настоящее время решается функция детоксикации крови клиническими методами с использованием плазмофореза и криофильтрации. Однако обаметода делают необходимым частые посещения клиники больными. Перспективным способом замены поврежденной печени в настоящее время является технология замены поврежденной печени гибридом искусственной ткани, так называемого конструктора, полученного методом тканевой инженерии. Второй путь лечения печеночной патологии, активно разрабатываемый в настоящее время, – имплантация в поврежденную печень стволовых клеток. Основными трудностями при разработке биоискусственной печени являются слабая пролиферативная активность клеток печени при культивировании и их низкая жизнеспособность. Для повышения физиологической активности гепатоцитов разрабатываются два подхода: внутримышечная имплантация пула изолированных гепатоцитов в микро- или макрокапсулах, изготовленных из полимерных материалов (типа альгината и агарозы); перфузия крови или плазмы пациента с использованием экстракорпоральных устройств, содержащих свободную взвесь функционирующих донорских гепатоцитов (в основном, свиных) или гепатоцитов, иммобилизованных на поверхности полимерных матриксов или в объеме. Есть данные о том, что инкапсулированные гепатоциты, вводимые интраперитониально, в течение небольшого срока (7–10 дней) способны заменять функцию печени. Однако по истечении 4–6 недель инкапсулированные гепатоциты теряют функциональную активность. Одной из причин этого может быть разрушение капсулы. Для депонирования гепатоцитов описаны положительные примеры использования для этих целей пористых гранул на основе поливинилформальдегида, а также полупроницаемых полых волокон типа Plasmaphan (AKZO-NOBEL, Wuppertal, Германия) с диаметром пор ~ 0,5 мкм. Разрабатываются экстракорпоральные системы, представляющие собой коллагеновый гель с иммобилизованными в нем гепатоцитами; в качестве носителей гепатоцитов исследуются полимерные двухмерные матриксы, изготовленные из сополимеров молочной и гликолевой кислот, модифицированные коллагеном. Успехи в области конструирования биоискусственной печени с применением гепатоцитов млекопитающих позволили начать применение таких конструкций в клинических условиях для поддержки функции печени у пациентов, ожидающих проведения ортотопической трансплантации печени.
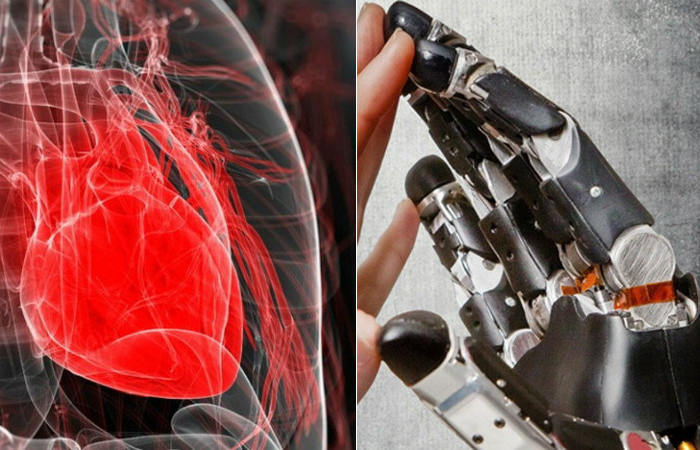
Человеческое тело весьма уязвимо. До недавнего времени при повреждении какого-либо органа заменить его не было возможно, и человек оставался калекой, получая достаточно зачастую очень неудобные и мало функуиональные протезы. Но уже сегодня исследователи добились существенных результатов в протезировании человеческих органов. Мы собрали 10-ку последних научных разработок, которые позволят уже в недалёком будущем заменять повреждённые части тела.
1. Сверхчувствительная электронная кожа

Кожа, покрывая и защищая всё тело человека, является наиболее легко повреждаемым органом. Стэнфордские ученые разработали супергибкий, сверхпрочный и суперчувствительный материал, который может стать основой для будущей синтетической кожи. Люди пытались разработать синтетическую кожу и раньше, но новый материал имеет гораздо большую сенсорную чувствительность. Он содержит органические транзисторы и слой эластичного материала, позволяющий ему растягиваться без повреждений. И она обладает автономным питанием - кожа содержит ряд упругих солнечных батарей.
2. Бьющееся сердце, созданное в чашке Петри
Ученые давно исследовали потенциал стволовых клеток для выращивания сердца, и недавно им удалось достичь существенного успеха в этом году, создав сердце в чашке Петри, которое могло биться самостоятельно. В течение 20 дней новое сердце билось со скоростью от 40 до 50 ударов в минуту. Оно пока слишком слабое, чтобы на самом деле перекачивать кровь, но подобная ткань имеет большой потенциал.
3. Протезы рук, которые чувствуют прикосновение

Нынешние протезы рук, конечно, могут захватывать вещи, но им не хватает одной из самых важных способностей настоящей человеческой руки - осязания. Люди с протезами не могут почувствовать, когда они находятся в контакте с объектом, не смотря на него напрямую. Исследовательская группа из Университета Чикаго решила эту проблему, создав руки, которые посылают электрические сигналы в мозг. Ученые провели эксперименты с обезьянами, изучая то, как их мозг реагирует на прикосновения.
4. Бионические ноги, управляемые мыслью

Хотя бионические ноги, конечно, являются огромным благом для тех, кто подвергся ампутированию, в них есть существенный недостаток — отсутствие реального соединения нервов с телом. Но в прошлом году, житель Сиэтла Зак Вотер получил первые в мире конечности, которые управляются силой мысли, благодаря тому, что воспринимают сигналы непосредственно от его мозга. Для оптимизирования этих искусственных ног, компания-производитель собирается сделать их еще тоньше и легче.
5. Миниатюрный человеческий мозг
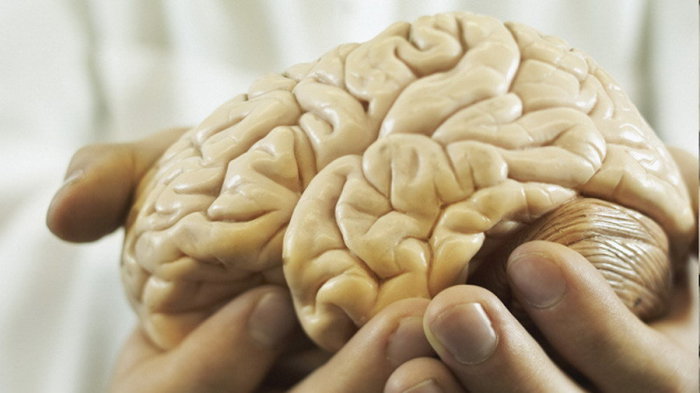
Смерть мозга — это фатально. Может быть, в один прекрасный день, человек будет в состоянии пересадить новый мозг в череп, но стоит помнить, что это не просто обычный орган. Он содержит все мысли и воспоминания, поэтому идея создания искусственных мозгов может показаться абсурдной. Но это не остановило ученых, которые вырастили из стволовых клеток настоящий человеческий мозг в лаборатории. Он, правда, пока размером с горошину и неспособен мыслить.
6. Уши, отпечатанные на 3D-принтере

Уже существует технология, с помощью которой можно искусственно восстановить слух, но внутренние имплантаты ничего не делают с видимой частью уха. Обычные искусственные уши выглядели как пластиковые игрушки. Но исследователи в этом году придумали новый метод, который обеспечивает возможность вырастить гибкие реалистичные уши из живых клеток. Эти клетки берут у крыс и коров, и из них формируется гель. Затем из этого геля с помощью 3D-принтера менее чем за час делают искусственное ухо.
7. Нос, который может чувствовать болезнь по запаху
Исследователи из Университета Иллинойса решили создать устройство, которое идентифицирует химические вещества по запаху, но их не устроила чувствительность человеческого носа. Вместо этого, они создали искусственный нос, который использует запах бактерий, чтобы выявить и диагностировать специфические заболевания.
8. Искусственная поджелудочная железа

Поджелудочная железа вырабатывает гормон инсулин, который в случае отсутствия его в организме необходимо вводить вручную. Диабетики постоянно проверяют уровень сахара в крови, а затем вводят инсулин, когда возникает необходимость. Искусственная поджелудочная железа, однако, сможет вводить инсулин в тело автоматически. Она контролирует уровень сахара в крови в любое время и регулирует его.
9. Искусственные глаза
Люди уже давно имеют возможность восстановить слух глухим, но восстановление зрения слепым — пока гораздо более сложный вопрос. Когда люди теряют зрение, их сетчатка больше не посылает сигналы от фоторецепторов в мозг. Для того, чтобы создать искусственный глаз, сначала нужно понять, как сетчатка обрабатывает эти сигналы, а этого ученые до недавнего времени не могли добиться. Ученые Weill Cornell Medical College смогли сделать это, по крайней мере с мышами и обезьянами, создав искусственную сетчатку, чьи чипы конвертируют изображения в электронные сигналы.
10. Пальцы и гигабайтами информации

Когда финский программист Джерри Джалава попал в аварию на мотоцикле в 2008 году, он потерял палец. Байкер нашел необычный выход из ситуации — он создал протез пальца, в который можно записать два гигабайта цифровой информации. Теперь он может просто вставлять необычный протез в разъем USB. В будущем Джалава планирует модернизировать своё изобретение, добавив поддержку беспроводной связи. Также он хочет добавить больше памяти.
В последнее время разработчики повернулись лицом к людям с ограниченными возможностями, предложив потрясающие модели инвалидных колясок, способные изменить их жизнь в лучшую сторону .
Возможность вырастить человеческий орган в пробирке и пересадить его человеку, нуждающемуся в пересадке — мечта трансплантологов. Ученые по всему миру работают над этим и уже научились делать ткани, небольшие работающие копии органов, и до полноценных запасных глаз, легких и почек нам на самом деле осталось совсем немного.
Легкие. Ученые из Техасского университета вырастили легкие человека в биореакторе. Правда, без кровеносных сосудов такие легкие не функциональны. Однако команда ученых из Медицинского центра Колумбийского университета (Columbia University Medical Center, New York) недавно впервые в мире получили функциональное легкое с перфузируемой и здоровой сосудистой системой у грызунов ex vivo.
Ткани сердечной мышцы. Биоинженерам из университета Мичигана удалось вырастить в пробирке кусок мышечной ткани. Правда, полноценно сердце из такой ткани пока работать не сможет, она вдвое слабее оригинала. Тем не менее пока это самый сильный образец сердечной ткани.
Кости. Израильская биотехнологическая компания Bonus BioGroup использовалат трехмерные сканы для создания гелеобразного каркаса кости перед посевом стволовыми клетками, взятыми из жира. Кости, получившиеся в результате, они успешно пересадили грызунам. Уже планируются эксперименты по выращиванию человеческих костей по этой же технологии.
Японские ученые вырастили глаз в чашке Петри. Искусственно выращенный глаз содержал основные слои сетчатки: пигментный эпителий, фоторецепторы, ганглионарные клетки и другие. Трансплантировать его целиком пока возможности нет, а вот пересадка тканей — весьма перспективное направление. В качестве исходного материала были использованы эмбриональные стволовые клетки.
Ученые из корпорации Genentech вырастили простату из одной клетки. Молекулярным биологам из Калифорнии удалось вырастить целый орган из единственной клетки.
Ученым удалось найти единственную мощную стволовую клетку в простатической ткани, которая способна вырасти в целый орган. Таких клеток оказалось чуть меньше 1% от общего числа. В исследовании 97 мышам трансплантировали такую клетку под почку и у 14 из них выросла полноценная простата, способная нормально функционировать. Точно такую же популяцию клеток биологи нашли и в простате человека, правда, в концентрации всего 0,2%.
Сердечные клапаны. Швейцарские ученые доктор Саймон Хоерстрап (Simon Hoerstrup) и Дорта Шмидт (Dorthe Schmidt) из университета Цюриха (University of Zurich) смогли вырастить человеческие сердечные клапаны, воспользовавшись стволовыми клетками, взятыми из околоплодной жидкости. Теперь медики смогут выращивать клапаны сердца специально для неродившегося еще ребенка, если у него еще в зародышевом состоянии обнаружатся дефекты сердца.
Ушная раковина. Используя стволовые клетки, ученые вырастили ухо человека на спине крысы. Эксперимент был проведен исследователями из Университета Токио (University of Tokyo) И Университета Киото (Kyoto University) под руководством Томаса Сервантеса (Thomas Cervantes).
Кожа. Ученые из Цюрихского университета (Швейцария) и университетской детской больницы этого города впервые сумели вырастить в лаборатории человеческую кожу, пронизанную кровеносными и лимфатическими сосудами. Полученный кожный лоскут способен почти полностью выполнять функцию здоровой кожи при ожогах, хирургических дефектах или кожных болезнях.
Поджелудочная железа. Ученые впервые создали васкуляризованные островки поджелудочной железы, способные вырабатывать инсулин. Еще одна попытка вылечить диабет I типа.
Почки. Ученые из австралийского университета Квинсленда научились выращивать искусственные почки из стволовых клеток кожи. Пока это лишь маленькие органоиды размером 1 см, но по устройству и функционированию они практически идентичны почкам взрослого человека.
Мочевой пузырь. Группа американских ученых под руководством Энтони Аталы (Anthony Atala) вырастила в лаборатории человеческие мочевые пузыри, полностью готовые к пересадке, из образцов собственных тканей пациентов. Те же ученые вырастили мочеиспускательные каналы для пациентов, у которых они были повреждены.
Кроме того, ученые уже научились выращивать хрящевые ткани, ткани скелетных мышц и костей, ткани гипофиза, тимуса, а также ткани, функционирующие аналогично тканям человеческого мозга.
Читайте также:

