Ракета на перхлорате аммония своими руками
Добавил пользователь Алексей Ф. Обновлено: 19.09.2024
Камрады! Кто-нибудь делал своими руками ракеты? Поделитесь опытом. Просьба ссылки не давать, всё читано, в т.ч. и на английском :) Интересен личный опыт.
Было такое в возрасте 12-15 лет. Вершиной стало создание ракеты длиной около метра с пороховой "боеголовкой" и автоматическим взрывателем. "Испытывали" в логу (между ул. Халтурина и ул. Добролюбова). Успешно все прошло - ракета ушла по баллистической траектории и врезавшись в заброшенный сарай (там внизу частные деревянные дома еще в то время были) со страшным грохотом взорвалась. Крыша сарая провалилась и часть дощатой стены выпала наружу. Но ничего не загорелось, слава Богу. Мы быстренько смотались и залегли. Вскоре приехали два "лунохода" с ментами. Вот так с шутками-прибаутками мы и коротали время в те советские годы. Генеральным конструктором ракеты был очень эрудированный парень. У ракеты был электрический запал и стартовала она со специальной направляющей конструкции. Двигатель - на порохе. Эффектные были "старты" :).
маленькие - обклейка карандаша из него же сопло(графит выскоблить, обработать)
средние из чего попало
не делал большие многоступенчатые но даавно мечтаю
еси будете их делать позовите чем смогу..
Rubin (29.07.2003, 16:00) :
Вершиной стало создание ракеты длиной около метра с пороховой "боеголовкой" и автоматическим взрывателем. "У ракеты был электрический запал и стартовала она со специальной направляющей конструкции. Двигатель - на порохе. Эффектные были "старты" :).
Здорово, у меня самая большая была где-то от силы 15 сантиметров, летела не далеко и не очень прямо %) было в детстве.
Almas (29.07.2003, 16:17) :
Karp (29.07.2003, 15:37) :
Камрады! Кто-нибудь делал своими руками ракеты? Поделитесь опытом. Просьба ссылки не давать, всё читано, в т.ч. и на английском :) Интересен личный опыт.
Ракетостроением серъезно занимались "муравейники".
Последний запуск видел собственными глазами. Дело было на Н.Островского, около шк.33.
Сабж метровый на площадке запуска. Стартовал очень легко, ушел "в точку", но без парашюта падал отвесно на землю. Ветер сносил его метров 50, пока он не очутился в р-не автостоянки перед домом спорта "Рубин". Запускающие субж пацаны и их наставник стояли с мокрыми от страха штанами, шептали заветные слова. На их счастье ракета вонзилась в асфальт хокейной плошадки (дело было летом). Это метров 10 от ряда автомашин.
Ну а так весело было наблюдать.
Ракетостроением занимались в период подготовке к сдаче госэкзамена по войне на комплекске ППИ. В аудитории стоял афигительных размеров стол с "местностью", танчки, домики и пр. Ну бывало сядем, засыпим в алюмнинивоую фольгу(обкрутить карандаш) смеси пороха и спичек и давай запускать баллистику. Кончилось все печально. Аудиторию "продымили", прибежал офицер, потом 4-е часа занимались шагистикой на плацу.
Делал сначала из пропитки и фольги, а потом пороховую - около 20 см длинной. Последняя 16-ти этажный дом сделала и взорвалась. Попал в милицию.
Karp (31.07.2003, 13:56) :
Может быть мой совет пригодится. Основу для корпуса проще всего изготовить методом "папье-маше". Нужно найти (выточить) подходящего диаметра (он будет внутренним) круглую гладкую палку, трубу и оклеивать ее многослойно хорошо размоченной в клее (можно обойном, казеиновым и т.п.) бумагой. После высыхания, снять "изделие" с оснастки, обработать торцы, красить и т.д. согласно задаче. Получается легкий и прочный крпус.
Вот и самодельный небольшой телескоп этим же методом можно изготовить - трубка в трубку.

Вызывается композитное ракетное топливо перхлорат аммония , или PCPA , материал , состоящий из матрицы макромолекулярных в полимерной топлива в качестве связующего вещества, заряд перхлорат аммония NH 4 ClO 4 в качестве окислителя и порошкообразного алюминия в качестве топлива . Полимер , как правило , основан на hydroxytelechelic полибутадиена (PBHT), но может также состоять из полибутадиена - акриловая кислота - акрилонитрил (PBAN) тройной сополимер.
Резюме
Использует
Это композитное ракетное топливо очень широко используется в космонавтике в взлетной разгонных ракетных топлив из космических ракет - носителей , таких как Ariane 5 , или в ретро - ракет космических аппаратов , таких как Mars Exploration Rover . PCPA выпускается в виде блоков, встроенных в корпус подруливающих устройств, с геометрией, строго определенной в соответствии с желаемой кривой тяги.
Собственные характеристики твердого ракетного топлива всегда ниже, чем у жидкого ракетного топлива , но тяги, получаемые твердотопливными ускорителями, могут быть намного больше в течение нескольких минут, необходимых для взлета, чтобы дать пусковой установке скорость, которая позволит ей освободиться от сила тяжести, использующая только его жидкостные ракетные ступени. Композитные пропелленты из перхлората аммония поэтому используются в приложениях, для которых прежде всего требуются мощность, простота и надежность с удельным импульсом, не превышающим 260 с .
Композиции
Связующее
Связка композитного пороха должна соответствовать нескольким условиям:
- он должен быть жидким во время смешивания компонентов ракетного топлива
- он должен быть химически совместим с окислителем
- он должен поглощать очень высокие заряды
- он должен обладать эластичностью, подходящей для обеспечения сцепления блока во время стрельбы и во время горения .
Традиционные связующие композитных ракетных топлив на 70-80% состоят из форполимера, который придает им большую часть их свойств благодаря природе его полимеризованных остатков ( бутадиен H 2 C = CH - CH = CH 2 или акрилонитрил H 2 C = CH - C≡N , например) или концом его цепей (например, гидроксил -ОН). Сами цепи состоят из органических мономеров (на основе углерода , азота , кислорода и водорода ), повторяющихся несколько десятков раз. Там нет тяжелых атомов (в частности, кремния , который исключает полисилоксаны ), потому что продукты сгорания должны быть как можно более легкими, чтобы оптимизировать скорость выброса дымовых газов и, следовательно, полученную тягу.
Сшивающий агент придает форполимеру консистенцию, обеспечивая связи между макромолекулярными цепями, в то время как пластификатор используется для облегчения формования блока пропеллента. Все представляет собой связующее, которое обычно составляет от 10 до 15% массы композитного топлива.
Преполимер
Hydroxytelechelic полибутадиена HO [-H 2 С-СН = СН-СН 2 ] р -OH (PBHT) - самый распространенный форполимер на сегодняшний день в наиболее эффективных PCPA. Он используется, в частности, на ступенях порошкового ускорителя Ariane 5 .
Поли ( бутадиен - [H 2 C - CH = CH - CH 2 -] p акриловая кислота - [H 2 C - C = COO–] p акрилонитрил - [H 2 C - CH (C≡N) -] p ) (PBAN), менее токсичный, чем PBHT , скорее использовался в 1970-х и 1980-х годах для разработки ускорителей для ракет-носителей Titan III и космических кораблей .
Преимущество PBHT по сравнению с PBAN состоит в том, что он может быть сшит при комнатной температуре изоцианатами , недостатком является токсичность этих изоцианатов.
Сшивающий агент
Триол часто используется в качестве сшивающего агента с диизоцианатами для образования уретановых –NH-COO– мостиков с концевыми гидроксильными группами PBHT . Триолы обеспечивают трехмерное сшивание, а диизоцианаты играют роль удлинителей цепи. Образование уретанового мостика между изоцианатами R 1 –N = C = O и HO - R спирты 2 проводится по реакции:
Эти мостики образуются между полибутадиеном и диизоцианатом, а также между диизоцианатом и триолом. Степень сшивки определяет механические свойства топлива. Он должен гарантировать достаточное удлинение и устойчивость к нагрузкам.
Пластификатор
В дополнение к сшивающему агенту твердые пропелленты также содержат пластификатор, функция которого заключается в снижении вязкости пасты для облегчения ее применения. Обычно это масло, не реагирующее с полимером, за разбавление которого оно отвечает, чтобы ограничить нековалентные взаимодействия между цепями как в жидком состоянии, так и после сшивки.
Окислитель
Перхлорат аммония NH 4 ClO 4 по определению является окислителем PCPA. Обычно он составляет от 60 до 70% масс.
Горючие
Топливо представляет собой металлический порошок, чаще всего алюминий , иногда магний . Алюминий, безусловно, является лучшим в PCPA. Обычно он составляет от 15 до 20% масс.
Катализатор горения
Мы часто добавляем щепотку оксида железа Fe 2 O 3. , оксид меди CuO, диоксид марганца MnO 2 или дихромат меди CuCr 2 O 7 (менее 0,1% от массы топлива) в качестве катализатора горения, роль которого заключается в:
- способствовать разложению окислителя и топлива
- способствовать газофазной реакции в зоне горения
- способствовать теплообмену на поверхности порохового блока
Также используются жидкие производные железа или бора , которые также играют роль пластификатора, что позволяет избежать перегрузки связующего твердыми частицами.
Регулятор горения
Также используются замедлители горения, которые служат для регулирования давления и, следовательно, тяги во время сгорания блока. Соли щелочных или щелочноземельных металлов влияют на кинетику разложения перхлората аммония и при низкой концентрации (от 1 до 2% от массы пропеллента), но они неэффективны для порошков, заряженных алюминием. В этом случае можно использовать хладагент, который снижает температуру сгорания топлива и, следовательно, создаваемую тягу за счет уменьшения энтальпии сгорания или разбавления дымовых газов азотом: это имеет место в случае нитрата. Аммоний NH 4 НЕТ 3 и нитрогуанидин H 2 N - C (= NH) –NH - N + OO - .
Выполнение
Системы твердого топлива
- F prop сила тяги метательного взрывчатого вещества, выраженная в ньютонах.
- v e скорость выброса выхлопных газов, измеряемая в метрах в секунду.
- м ˙ > \,> массовый расход выхлопных газов, измеряемый в килограммах в секунду.
Скорость выброса может модулироваться давлением в камере сгорания и, следовательно, в частности температурой сгорания, в то время как массовый расход может модулироваться скоростью сгорания (которая сама модулируется составом топливного блока. Топливо при сгорании поверхность) и самой поверхностью горения, регулируемой геометрией топливного блока в ракете.
Массовый расход и скорость горения
Массовый расход выражается как функция поверхности горения следующим образом:
Например, звездообразный профиль будет давать стабильную тягу в течение более длительного периода времени, чем чисто цилиндрический профиль:


Скорость горения сложнее контролировать, это зависит от ряда довольно тонких факторов:
- химический состав пороха, который может варьироваться в зависимости от места
- размер частиц наполнителя, добавляемого в связующее ( перхлорат аммония и алюминия )
- давление в камере сгорания
- теплообменные свойства системы
- явления эрозии блока дымовыми газами
- начальная температура блока
- tc скорость горения, выраженная в м / с
- имеет постоянный
- Pc давление в камере сгорания
- n постоянный показатель степени, обычно от 0,3 до 0,5 для PCPA.
Это значение n меньше 1 указывает на то, что PCPA являются достаточно безопасным топливом, кинетика горения которого не будет стремиться к бесконечности в случае неконтролируемого повышения давления в камере сгорания.
Пример ракет-носителей космического корабля
Каждая ракета-носитель американского космического корабля "Шаттл" содержит примерно:
Описание: Хлорид аммония используют в дымовых составах. При нагревании хлорид аммония разлогается на хлористый водород и аммиак, в холодной области они рекомбинируют, образуя дым из мельчайших частичек хлорида аммония.
Опасности: Дымы на основе хлорида аммония раздражают глаза и легкие, вследствие содержания в них некоторых количеств хлороводорода и аммиака. Сам же хлорид аммония не токсичен и даже изредка используется в кандитерском деле. Стоит помнить о том что хлорид аммония несовместим с хлоратами поскольку может образовывать крайне нестойкий хлорат аммония, который в свою очередь может вызывать самовоспламенение и даже самопроизвольные взрывы смесей.
Источники: Хлорид аммония легко получить нейтрализацией раствора аммиака соляной кислотой, рекомендуется использовать некоторый избыток аммиака для полного разложения соляной кислоты. Если же продукт будет содержать остатки кислоты - это сделает его применение опасным, поскольку может вызвать самовоспламенение смесей на его основе. Полученный раствор выпаривают для получения готового продукта.
Нитрат аммония (аммиачная селитра)
Формула: NH4NO3
Описание: Нитрат аммония - окислитель. Нитрат аммония довольно гигроскопичен и редко используется в пиротехнике. Более часто он применяется в составах ракетного топлива.
Опасности: Как извесно большие массы нитрата аммония могут взрываться, хотя его чувствительность крайне низка. Риск взрыва увеличивается ели нитрат аммония литой или смешан с металлическими топливами типа аллюминия или магния, а так же органическими веществами. Нитрат аммония несовместим с хлоратами поскольку может образовывать крайне нестойкий хлорат аммония, который в свою очередь может вызывать самовоспламенение и даже самопроизвольные взрывы смесей. Нитрат аммония так же не совместим с металическими горючими, в этом случае имеется возможность саморазогрева и самовоспламенения особенно во влажном состоянии. Для предотвращения подобного эффекта в состав вводят 1-2 % борной кислоты, тем не менее лучше избегать использования подобных смесей, поскольку высокая гигроскопичность нитрата аммония сильно усугубляет проблему.
Источники: Раствор нитрата аммония может быть приготовлен нейтрализацией раствора аммиака азотной кислотой. Рекомендуется использовать небольшой избыток аммиака для полного разложения кислоты, в присутствии следов кислоты применение продукта станет опасным и может привести к самовоспламенению смесей на его основе. Необходимые количества нитрата аммония легко могут быть приобретены в садовом магазине, где его продают как удобрение.
Перхлорат аммония
Формула: NH4ClO4
Описание: Перхлорат аммония - окислитель, часто используемый в пиротехнике. Перхлорат аммония может использоваться для создания потрясающих составов цветных огней, хотя эти составы не всегда имеют достаточную для звездок скорость горения, что является преимуществом при изготовления огненных надписей и свеч где низкая скорость горения весьма желательна. Перхлорат аммония является основой высококачественных ракетных топлив, используемых для запуска ракет и космических аппаратов.
Опасности: Перхлорат аммония способен детонировать, хотя его чувствительность достаточно низка. Опасность взрыва увеличивается при использовании больших количеств его смесей с металлическим или органическим горючим.
Источники: Перхлорат аммония можно приобрести у поставщиков химической продукции. Тонкодисперсный порошок перхлората аммония - вещество оборот которого строго регулирован и не может быть легко приобретен. Поскольку перхлорат аммония является одным из основных необходимых в пиротехнике компонентов есть смысл изготавливать его в домашних условиях. Перхлорат аммония может быть получен реакцией обмена соли аммония с перхлоратом натрия, который в свою очередь может быть получен электролизом водного раствора хлорида натрия, подробную информацию о получении хлоратов и перхлоратов можно найти здесь.
Ракетное топливо содержит в своем составе горючее и окислитель и, в отличие от реактивного топлива, не нуждается во внешнем компоненте: воздухе или воде. Ракетные топлива по своему агрегатному состоянию делятся на жидкие, твердые и гибридные. Жидкие топлива подразделяются на криогенные (с температурой кипения компонентов ниже нуля градусов по Цельсию) и высококипящие (остальные). Твердые топлива состоят из химического соединения, твердого раствора или пластифицированной смеси компонентов. Гибридные топлива состоят из компонентов в разном агрегатном состоянии, на данный момент находятся в стадии исследований.

Исторически первым ракетным топливом послужил дымный порох, состоящий из смеси селитры (окислителя), древесного угля (горючего) и серы (связующего), который впервые был использован в китайских ракетах во 2 веке н.э. Боеприпасы с ракетным двигателем твердого топлива (РДТТ) применялись в военном деле как зажигательное и сигнальное средство.

После изобретения в конце XIX века бездымного пороха на его основе было разработано однокомпонентное баллиститное топливо, состоящее из твердого раствора нитроцеллюлозы (горючего) в нитроглицерине (окислителе). Баллиститное топливо обладает кратно большей энергетикой по сравнению с дымным порохом, имеет высокую механическую прочность, хорошо формуется, длительно сохраняет химическую стабильность при хранении, обладает низкой себестоимостью. Эти качества предопределили широкое использование баллиститного топлива в наиболее массовых боеприпасах, оснащенных РДТТ – реактивных снарядах и гранатах.

После Второй мировой войны ракетное оружие получило приоритет в развитии по сравнению с другими видами вооружения по причине своей способности доставлять к цели ядерные заряды на любое расстояние – от нескольких километров (реактивные системы) до межконтинентальной дальности (баллистические ракеты). Кроме того, ракетное оружие существенно потеснило артиллерийское в авиации, ПВО, сухопутных войсках и на флоте за счет отсутствия силы отдачи при пуске боеприпасов с ракетными двигателями.
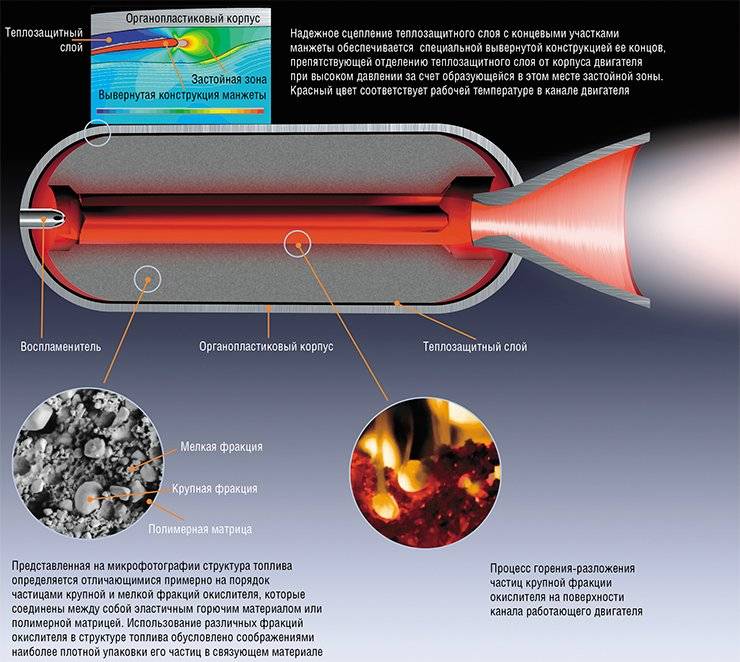
Одновременно с баллиститным и жидким ракетным топливом развивались многокомпонентные смесевые твердые топлива, как наиболее приспособленные к применению в военных целях в связи с их широким температурным диапазоном эксплуатации, устранением опасности разлива компонентов, меньшей стоимости твердотопливных ракетных двигателей за счет отсутствия в их конструкции трубопроводов, клапанов и насосов, большей тягой на единицу веса.
Основные характеристики ракетных топлив
Кроме агрегатного состояния своих компонентов, ракетные топлива характеризуются следующими показателями:
— удельный импульс тяги;
— термическая стабильность;
— химическая стабильность;
— биологическая токсичность;
— плотность;
— дымность.
Удельный импульс тяги ракетных топлив зависит от давления и температуры в камере сгорания двигателя, а также молекулярного состава продуктов сгорания. Кроме того, удельный импульс зависит от степени расширения сопла двигателя, но это больше относится к внешней среде применения ракетной техники (воздушная атмосфера или космическое пространство).

Повышенное давление обеспечивается с помощью использования конструкционных материалов с высокой прочностью (стальных сплавов для ЖРД и органопластиков для РДТТ). В этом аспекте ЖРД опережают РДТТ по причине компактности своего двигательного агрегата по сравнению с корпусом твердотопливного двигателя, являющегося одной большой камерой сгорания.
Высокая температура продуктов сгорания достигается с помощью добавления в твердое топливо металлического алюминия или химического соединения – гидрида алюминия. Жидкое топливо может использовать подобные добавки только в случае его загущения специальными добавками. Теплозащита ЖРД обеспечивается с помощью охлаждения топливом, теплозащита РДТТ – с помощью прочного скрепления топливной шашки со стенками двигателя и применения выгорающих вкладышей из углерод-углеродного композита в критическом сечении сопла.

Молекулярный состав продуктов сгорания/разложения топлива влияет на скорость истечения и их агрегатное состояние на срезе сопла. Чем меньше вес молекул, тем больше скорость истечения: наиболее предпочтительными продуктами сгорания являются молекулы воды, за ними следуют молекулы азота, углекислого газа, окислы хлора и других галогенов; наименее предпочтительным является окисел алюминия, который конденсируется в сопле двигателя до твердого состояния, снижая тем самым объем расширяющихся газов. Кроме того, фракция окисла алюминия вынуждает применять сопла конической формы из-за абразивного износа наиболее эффективных сопел Лаваля с параболической поверхностью.
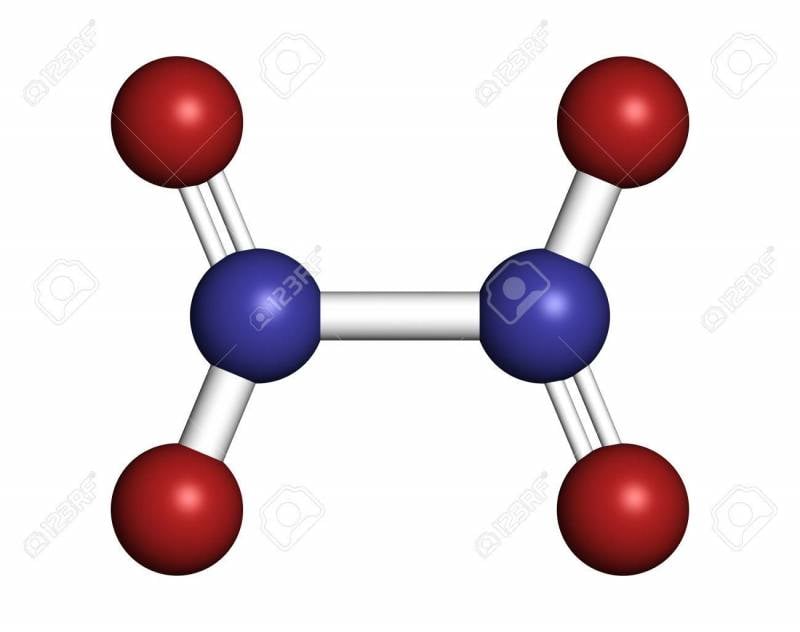
Термическая стабильность твердых топлив в основном определяется соответствующим свойством растворителя и полимерного связующего. В составе баллиститных топлив растворителем является нитроглицерин, который в твердом растворе с нитроцеллюлозой имеет температурный диапазон эксплуатации от минус до плюс 50°C. В смесевых топливах в качестве полимерного связующего используются различные синтетические каучуки с тем же температурным диапазоном эксплуатации. Однако термическая стабильность основных компонентов твердого топлива (динитрамид аммония +97°C, гидрид алюминия +105°C, нитроцеллюлоза +160°C, перхлорат аммония и октоген +200°C) значительно превышает аналогичное свойство известных связующих, в связи с чем актуальным является поиск их новых составов.
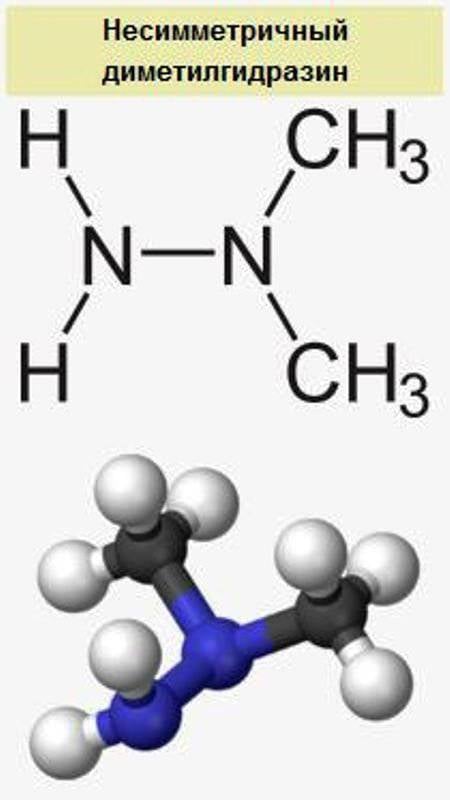
Наиболее химически стабильной является топливная пара АТ+НДМГ, поскольку для неё разработана уникальная отечественная технология ампулизированного хранения в алюминиевых баках под небольшим избыточным давлением азота в течение практически неограниченного времени. Все твердые топлива со временем химически деградируют из-за самопроизвольного разложения полимеров и их технологических растворителей, после чего олигомеры вступают в химические реакции с другими, более стойкими компонентами топлива. Поэтому шашки РДТТ нуждаются в регулярной замене.
Биологически токсичным компонентом ракетных топлив является НДМГ, который поражает центральную нервную систему, слизистые оболочки глаз и пищеварительного тракта человека, провоцирует раковые заболевания. В связи с этим работа с НДМГ ведется в изолирующих костюмах химзащиты с применением автономных дыхательных аппаратов.
Величина плотности топлива прямо влияет на массу топливных баков ЖРД и корпуса РДТТ: чем больше плотность, тем меньше паразитная масса ракеты. Наименьшая плотность у топливной пары водород+кислород — 0,34 г/куб. см, у пары керосин+кислород плотность составляет 1,09 г/куб. см, АТ+НДМГ – 1,19 г/куб. см, нитроцеллюлоза+нитроглицерин – 1,62 г/куб. см, алюминий/гидрид алюминия + перхлорат/динитрамид аммония – 1,7 г/куб.см, октоген+перхлорат аммония – 1,9 г/куб. см. При этом надо учитывать, что у РДТТ осевого горения плотность топливного заряда примерно в два раза меньше плотности топлива из-за звездообразного сечения канала горения, применяемого с целью поддержания постоянного давления в камере сгорания вне зависимости от степени выгорания топлива. То же самое относится к баллиститным топливам, которые формируются в виде набора лент или шашек для сокращения времени горения и дистанции разгона реактивных снарядов и ракет. В отличии от них плотность топливного заряда в РДТТ торцевого горения на основе октогена совпадает с указанной для него максимальной плотностью.

Последним из основных характеристик ракетных топлив является дымность продуктов сгорания, визуально демаскирующих полет ракет и реактивных снарядов. Указанный признак присущ твердым топливам, содержащим в своем составе алюминий, окислы которого конденсируются до твердого состояния в процессе расширения в сопле ракетного двигателя. Поэтому указанные топлива применяются в РДТТ баллистических ракет, активный участок траектории которых находится вне зоны прямой видимости противника. Авиационные ракеты снаряжаются топливом на основе октогена и перхлората аммония, реактивные снаряды, гранаты и противотанковые ракеты – баллиститным топливом.
Энергетика ракетных топлив
Для сравнения энергетических возможностей различных видов ракетного топлива необходимо задать для них сопоставимые условия горения в виде давления в камере сгорания и степени расширения сопла ракетного двигателя – например, 150 атмосфер и 300-кратное расширение. Тогда для топливных пар/троек удельный импульс составит:
кислород+водород – 4,4 км/с;
кислород+керосин – 3,4 км/с;
АТ+НДМГ – 3,3 км/с;
динитрамид аммония + гидрид водорода + октоген – 3,2 км/с;
перхлорат аммония + алюминий + октоген – 3,1 км/с;
перхлорат аммония + октоген – 2,9 км/с;
нитроцеллюлоза + нитроглицерин – 2,5 км/с.

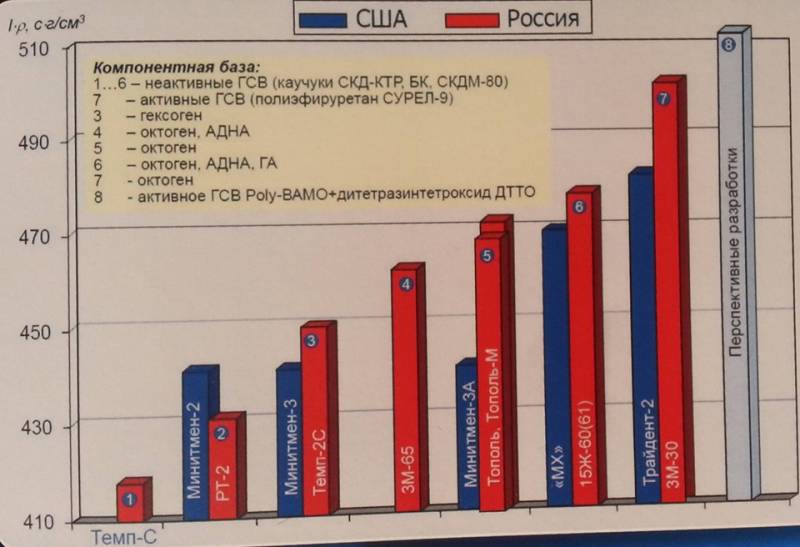
окислитель – динитрамид аммония, 58%;
горючее – гидрид алюминия, 27%;
пластификатор – нитроизобутилтринитратглицерин, 11,25%;
связующее — полибутадиеннитрильный каучук, 2,25%;
отвердитель – сера, 1,49%;
стабилизатор горения — ультрадисперсный алюминий, 0,01%;
добавки – сажа, лецитин и т.д.
Перспективы развития ракетных топлив
Основными направлениями развития жидких ракетных топлив являются (в порядке очередности реализации):
— использование переохлажденного кислорода с целью увеличения плотности окислителя;
— переход к топливной паре кислород+метан, горючий компонент которой обладает на 15% большей энергетикой и в 6 раз лучшей теплоемкостью, чем керосин с учетом того, что алюминиевые баки при температуре жидкого метана упрочняются;
— добавление озона в состав кислорода на уровне 24% с целью повышения температуры кипения и энергетики окислителя (большая доля озона является взрывоопасной);
— использование тиксотропного (загущенного) топлива, компоненты которого содержат взвеси из пентаборана, пентафторида, металлов или их гидридов.
Переохлажденный кислород уже используется в ракете-носителе Falcon 9, ЖРД на топливной паре кислород+метан разрабатываются в России и США.

Другим перспективным направлением является расширение номенклатуры используемых нитраминных взрывчатых веществ, обладающих большим кислородным балансом по сравнению с октогеном (минус 22%). В первую очередь это гексанитрогексаазаизовюрцитан (Cl-20, кислородный баланс минус 10%) и октанитрокубан (нулевой кислородный баланс), перспективы применения которых зависят от снижения стоимости их производства – в настоящее время Cl-20 на порядок дороже октогена, октонитрокубан на порядок дороже Cl-20.
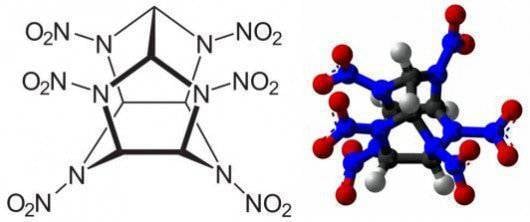
Кроме совершенствования известных типов компонентов, исследования также ведутся в направлении создания полимерных соединений, молекулы которых состоят исключительно из атомов азота, соединенных между собой одинарными связями. В результате разложения полимерного соединения под действием нагрева азот образует простые молекулы из двух атомов, соединенных тройной связью. Выделяемая при этом энергия двукратно превышает энергию нитраминных ВВ. Впервые азотные соединения с алмазоподобной кристаллической решеткой были получены российскими и немецкими учеными в 2009 году в ходе экспериментов на совместной опытной установке под действием давления в 1 млн. атмосфер и температуры в 1725°C. В настоящее время ведутся работы по достижению метастабильного состояния азотных полимеров при обычных давлении и температуре.
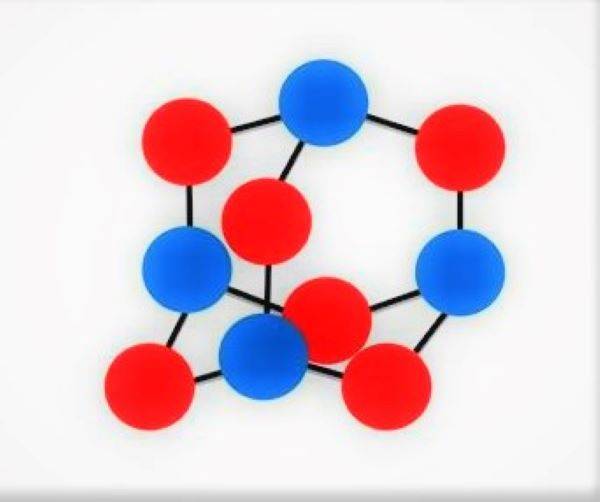
Перспективными кислородсодержащими химическими соединениями являются высшие окислы азота. Известный оксид азота V (плоская молекула которого состоит из двух атомов азота и пяти атомов кислорода) не представляет практической ценности в виде компонента твердого топлива в связи с низкой температурой его плавления (32°C). Исследования в этом направлении ведутся путем поиска метода синтеза оксида азота VI (гексаоксид тетраазота), каркасная молекула которого имеет форму тетраэдра, в вершинах которого расположены четыре атома азота, связанных с шестью атомами кислорода, расположенными на ребрах тетраэдра. Полная замкнутость межатомных связей в молекуле оксида азота VI дает возможность прогнозировать для него повышенную термическую стабильность, сходную с уротропином. Кислородный баланс оксида азота VI (плюс 63%) позволяет существенно повысить удельный вес в составе твердого ракетного топлива таких высокоэнергетических компонентов, как металлы, гидриды металлов, нитрамины и углеводородные полимеры.
Читайте также:

