Очистка воды гипохлоритом натрия своими руками
Добавил пользователь Skiper Обновлено: 05.10.2024
Классической характерной чертой дачной жизни является сезонность проживания загородом, при этом, как правило, в теплое время года. Вследствие этого все оборудование и системы жизнеобеспечения на зиму должны выводиться из эксплуатации и, при необходимости, консервироваться. При этом их запуск и обслуживание также должны быть простыми и недорогостоящими, так как обычно летом на даче чаще всего проживают дети, их бабушки и мамы, у которых нет возможности вникать во все технические премудрости и тонкости настроек того или иного прибора.
Говоря о системе водоснабжения в общем и элементах очистки воды в частности следует прежде всего обратить внимание на качество сборки фитинговых узлов и их надежности. После зимы есть риск, что резьбовые соединения, чье исполнения окажется на фум-ленте или низкокачественном льне, потекут. В случае же, если сам фитинг, а это может быть кран шаровый или муфта, выполнены из металла низкого качества, то и вовсе после начала эксплуатации он может треснуть. В данном вопросе наши рекомендации будут следующими:
- Все металлические сантехнические резьбовые соединения следует выполнять на хорошем льне с использованием специализированной смазки;
- Соединения, где используется пластик, выполнять на фум-ленте с соблюдением числа резьбовых намоток и ширины ленты;
- Аккуратно осуществлять затяжку фитингов, не перебарщивая с моментом силы;
- Прокладки или уплотнения из резины смазывать силиконовой смазкой;
- При прокладке трубопроводов использовать качественный полипропилен или металлопластик, не экономя на материале.
Водоочистное оборудование
Дачное оборудование для очистки воды, по аналогии с прочим оборудованием, должно иметь соответствующие параметры своим условиям работы, а именно:
- Неприхотливость и простота в обращении даже неподготовленными людьми;
- Возможность вывода из эксплуатации на зиму без больших затрат;
- Надежность на всем протяжении срока службы;
- Эффективность работы в продолжении всего сезона.
Если же вода поступает из колодца, то тут не всегда возможно обойтись картриджами, особенно если водопотребление большое и по многим химическим элементам нет достижения до качества питьевой воды из нецентрализованного источника водоснабжения.
Для такой воды характерны превышения по таким примесям, как железо, кальциевые соли, обуславливающие жесткость воды, органические соединения, бактерии, реже аммонийный азот и фосфор.
Фильтрация воды от железа
При очистке колодезной воды от железа в первую очередь следует определиться с ее составом. Для этого воду требуется сдать на анализ в специализированную лабораторию. Чаще всего железо в колодезной воде встречается в коллоидной или растворенной, но еще не окисленной форме. Так как вода в колодце имеет достаточную площадь поверхности раздела фаз и постоянно растворяет в себе газы воздуха, то должен присутствовать и кислород. Вследствие этих особенностей мы рекомендуем следующую схему очистки:

Фильтрационное умягчение воды
Вода из колодца может быть насыщена солями кальция, что будет делать ее довольно жесткой и, вследствие этого, вызывать накипные отложения на приборах нагрева, таких как чайник, бойлер или тэн стиральной машины. Для умягчения следует применять фильтры-умягчители с катионообменной смолой. Их преимущество будет заключаться еще и в том, что помимо снижения жесткости удаляется и железо, если таковое есть в количествах, допустимых для применения на катионитовых фильтрах.
Для умягчения воды на даче наша компания предлагает следующие системы фильтрации:

Обеззараживание питьевой воды и удаление органических примесей
Для обеззараживания воды следует применять либо гипохлорит натрия, либо ультрафиолетовую лампу. В первом случае требуется контроль дозации реагента, во втором периодическое техническое обслуживание, заключающееся в чистке колбы.
Применение гипохлорита натрия связано не только с обеззараживанием воды, но и с окислением органики, в особенности это касается связанных коллоидов железа.
Дозация гипохлорита натрия ведется на самом начальном этапе очистки, когда требуется окислить органические соединения. На втором этапе требуется удалить все взвешенные частицы и коллоиды. На третьем этапе воду следует пропустить через угольный фильтр, на котором произойдет сорбция оставшихся органических веществ и свободного хлора. После угольного фильтра следует поставить либо ультрафиолетовую лампу для финального обеззараживания, либо вновь провести добавление гипохлорита для ликвидации бактерий.
Для обеззаражнивания воды мы рекомендуем применять оборудование такого типа:

Несмотря на имеющиеся в природе типовые технические решения систем очистки воды, мы настоятельно рекомендуем не делать самостоятельный подбор, не проконсультировавшись предварительно с профессионалами в этой области.
Пример модернизации после ошибки нашего клиента
Для того, что бы не быть голословными, приведем пример из практики, на котором хорошо видно, как можно ошибиться при самостоятельном выборе фильтров для системы очистки питьевой воды.
Анализ воды показал превышения по следующим металлам:
- Железо – 15 мг/л, при норме 0,3 мг/л.
- Марганец – 1 мг/л, при норме 0,01 мг/л.
- Жесткость – 2,8 мг-экв/л при норме до 10 мг-экв/л. Оптимум 2,5 мг-экв/л.
На основании данных превышений гражданин решил, что ему вполне подойдет фильтр-умягчитель. После его установки была вновь отобрана проба воды и сдана на анализ.
Результат был следующим:
- Железо – 0,1 мг/л, при норме 0,3 мг/л.
- Марганец – 0,05 мг/л, при норме 0,1 мг/л.
- Жесткость – 0,8 мг-экв/л при норме до 10 мг-экв/л. Оптимум 2,5 мг-экв/л.
При этом катионообменную смолу пришлось менять уже через полгода эксплуатации из-за резко ухудшившегося качества воды.
Обратившись к нам со своей проблемой клиент получил модернизированную систему очистки, а именно:
- Колонну обезжелезивания с дозацией гипохлорита натрия.
- Угольный фильтр.
При этом уголь засыпали в ту же колонну, где до этого была смола.
После этого получили следующие результаты по воде:
- Железо – 0,05 мг/л, при норме 0,3 мг/л.
- Марганец – 0,02 мг/л, при норме 0,1 мг/л.
- Жесткость – 2,8 мг-экв/л при норме до 10 мг-экв/л. Оптимум 2,5 мг-экв/л.
Замену фильтрующей загрузки при такой системе необходимо было выполнять не чаще чем 1 раз в год, при этом суммарная ее стоимость не превышала стоимость замены катионита. Затраты на гипохлорит натрия и вовсе оказались несущественны.
Качество же воды при этом улучшилось, так как снизилось содержание железа и марганца, а жесткость осталась в своем оптимуме.

Проблема обеззараживания природных вод возникла в 80 – е годы XIX века после установления истинной причины появления водных инфекций. В настоящее время хорошо известно, что вода может быть источником распространения тяжелых инфекционных заболеваний и естественно, что профилактика этих заболеваний является одной из важнейших проблем в комплексе санитарно-гигиенических мероприятий проводимых на станциях водоподготовки и водоотведения. В статье мастер сантехник расскажет о применении гипохлорита натрия для обеззараживания воды.
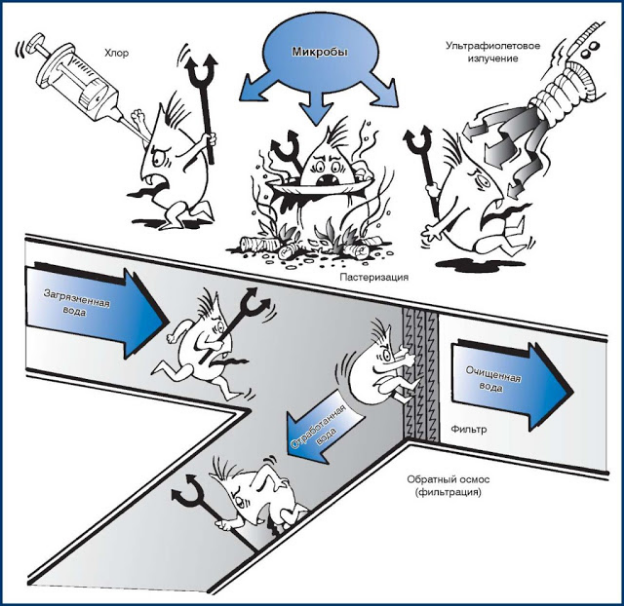
В настоящее время существуют различные методы обеззараживания воды: ультрафиолетовое и ионизирующее излучение, озонирование, бромирование, хлорирование , серебрение, термообработка, микрофильтрование и др. Каждые из этих методов характеризуются своими достоинствами и недостатками.
Но наибольшее практическое применение получили методы обеззараживания газообразным хлором или веществами, содержащий активный хлор, которые дают гарантии потребителю, предусмотренными ТКП 45-4.01-31-2009 (02250) и ТКП 45-4.01-181-2009 (02250).
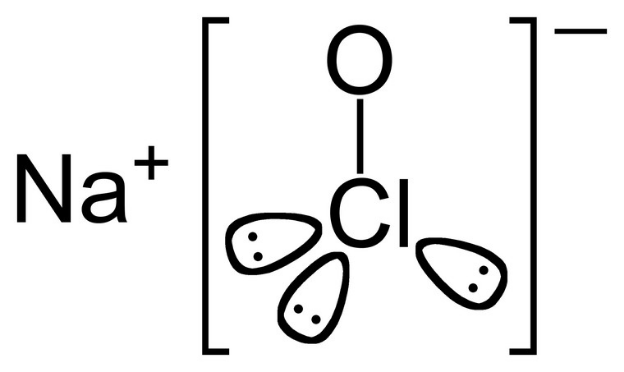
Гипохлорит натрия, или натрий хлорноватистокислый (ГПХН) – это соединение неорганической природы с формулой NaOCl. В безводном состоянии выглядит как твердая масса из бесцветных кристаллов, не отличающаяся устойчивостью. В воде растворяется хорошо. В виде водного раствора с характерным хлорным запахом, а также значительным коррозионным воздействием.
Водные растворы Гипохлорита натрия весьма неустойчивы и со временем разлагаются даже при обычной температуре (со скоростью 0,08 до 0,1 % в сутки). На скорость распада ГПХН влияет воздействие солнечного света, наличие катионов тяжелых металлов и хлоридов щелочных металлов. При этом наличие в водном растворе сульфата магния или кальция, борной кислоты, силикатов и пр. замедляют процесс разложения ГПХН. Следует заметить, что наиболее устойчивы растворы с сильнощелочной средой (значение pH > 10).

Микроэлемент стал известен в 18 веке, когда известный химик К. Шееле открыл элемент хлор. Позже Бертолле обнаружил, что при растворении газа в воде образуется кислотная смесь, которая оказывает отбеливающее и дезинфицирующее действие. Смесь была названа белильной жидкостью, централизовано основали ее массовое производство. Со временем стало ясно, что в данной форме хранить и транспортировать вещество неудобно, так как оно начинает быстро разлагаться под влиянием света, температуры, просто на открытом воздухе. Способ получения компонента был доработан и усовершенствован – едкий хлор стали пропускать через поташ. В результате получался стабильный KCLO. Соединение было названо жавелевой водой, стало активно использоваться в бытовых целях.
Единственный недостаток поташа – высокая цена. В начале 19 века А. Лабаррак заменил поташ на дешевую каустическую соду. Натрий гипохлорит NaCLO до сих пор активно применяется в разных хозяйственных отраслях.
Плотность гипохлорита натрия составляет 1250-1265 кг/м³. Кристаллы на открытом воздухе самопроизвольно плавятся и становятся жидкими. Цвет водного раствора бледно-зеленый, слабый характерный запах присутствует. Соединение начинает быстро разлагаться при внешних воздействиях, попадании в емкость посторонних предметов. Вероятно выделение токсичного хлора, опасного для органов зрения и кожи. Окисляющая реакция сильная.
Натрий гипохлорит из водного раствора выделяется выпариванием с образованием игольчатых кристаллов. С учетом условий среды при разложении могут образовываться различные вещества и продукты. В обычных условиях это соль с кислородом, при нагревании – соль поваренная и хлорат натрия. При действии кислот реакция сопровождается выделением свободного хлора. Окислительные свойства выражены со всеми восстановителями. Соли преобразуют сульфита с нитритами в сульфаты и нитраты, растворяют мышьяк и фосфор с образованием кислот, переводят аммиак в гидразин. Коррозионные свойства выраженные, поэтому вещество для обработки металлических изделий не используется. Главное действие – окисляющее.
- Первый – хлор пропускается через гидроксид натрия раствор с получением конечного продукта. Это химический способ;
- Второй вариант – электрохимический. Он предполагает подвергание электролизу раствора NaCL либо морской воды. Оба решения находят свое повсеместное применение на производствах. Лабораторный синтез предполагает получение малых порций продукта. Он предполагает пропускание хлора через раствор каустика/карбоната натрия.
Основными достоинствами технологии обеззараживания воды гипохлоритом натрия является безопасность его применения и значительное уменьшение воздействия на окружающую среду по сравнению с жидким хлором.
Предлагаемый метод отличается высокой степенью экологической и промышленной безопасности, не требует создания системы нейтрализации аварийных выбросов, мероприятий по охране окружающей среды и защите обслуживающего персонала.
Гипохлорит натрия обладает выраженным бактерицидным эффектом, под действием которого бактерии и вирусы, находящиеся в воде, погибают в результате окисления веществ, входящих в состав протоплазмы клеток, что при относительно низкой стоимости и простоте получения гипохлорита натрия обеспечивает его широкое применение для обеззараживания на различных объектах.
Дезинфекция насосных скважин и водонапорных башен, резервуаров и трубопроводов, предотвращение биологического обрастания в системах водяного обогрева и охлаждения.
Применение для удаления органических веществ из поверхностных вод при первичном хлорировании, при вторичном — обеспечение консервирующего и последействующего эффекта.
Дезинфекция и очистка хирургического инструмента, диализаторов, эндоскопов, обработка кожных покровов. Дезинфекция посуды, игрушек, пластмассовых и крашеных поверхностей, линолеума, санитарных хранилищ, помещений, одежды. Устранение неприятных запахов.
Применение при обработке бытовых и промышленных сточных вод, для деструкции животных и растительных микроорганизмов, устранения запахов (особенно образующихся из серосодержащих веществ), обезвреживания промышленных стоков, в том числе содержащих цианистые соединения, удаления из сточных вод ртути, а также для обработки охлаждающей конденсаторной воды на электростанциях.
Похожие темы научных работ по химическим технологиям , автор научной работы — Арцибашева М. С., Ковалёва Л. А.
Способ повышения КПД электролизных установок в групповом водопроводе Лиманского района путем применения водородных технологий
Комплексная технология обеззараживания воды и стоков и установкапрототип для ее промышленной реализации
чем в разнотравье, собранном в пригороде Магнитогорска: меди в 1,5-2 раза; цинка до 3 раз; железа свыше 5 раз; кадмия свыше 10 раз. Таким образом, можно сделать вывод о аэротехногенном загрязнении растительности данными поллютантами.
1. Ильин В.Б. Тяжелые металлы в системе почва-растение. Новосибирск: Наука, 1991. 150 с.
2. Алексеев Ю.В. Тяжелые металлы в почвах и растениях. Л.: Аг-ропромиздат, 1987. 142 с.
3. Бондарева Л.Г. Ландшафты, металлы и человек. М.: Мысль, 1976. 75 с.
4. Кабата-Пендиас А., ПендиасХ. Микроэлементы в почвах и растениях. М.: Мир, 1989. 439 с
5. Зырин Н.Г. Задачи и перспективы развития учения о микроэлементах в почвоведении // Биологическая роль микроэлементов в почвах. М.: Наука, 1983. С. 149-154.
М.С. Арцибашева, Л.А. Ковалёва
ОБЕЗЗАРАЖИВАНИЕ ВОДЫ ГИПОХЛОРИТОМ НАТРИЯ
Обеззараживанием воды называют процесс уничтожения находящихся там микроорганизмов. До 98% бактерий задерживается в процессе очистки воды.
Для обеззараживания используют в основном два метода: обработку воды сильными окислителями и воздействие на воду ультрафиолетовыми лучами. Также можно получить необходимый эффект фильтрования воды через ультрафильтры, обработкой ультразвуком, кипячением воды. Для очистки поверхностных вод почти исключительно применяют окислители: хлор, хлорсодержа-щие реагенты, озон. Для обеззараживания подземных вод можно использовать бактерицидные установки; для обеззараживания небольших порций воды - перманганат калия, перекись водорода.
© Арцибашева М.С., Ковалёва Л.А., 2011
Наиболее широко применяется метод обеззараживания воды - хлорирование жидким хлором.
Заводы поставляют хлор в баллонах массой до 100 кг и в контейнерах массой до 3000 кг, а также в железнодорожных цистернах вместимостью 48 тн.
При добавке в воду хлора происходит его гидролиз CÍ2 + H2O ^ HClO + HCl
Часть хлорноватистой кислоты HCÍO диссоциируется с образованием гипохлористого иона CÍO-.
При наличие в воде аммиака образуются моно- и дихлорам-
HCÍO + NH3 ^ NH2CI + H2O HCIO + NH2CI ^ NHCI2 + H2O
Основными обеззараживающими веществами являются: Cl2, HCIO, CIO-, NH2CI и NHCI2. Их называют активным хлором. При этом CI2, HCIO, CIO- образуют свободный хлор, a NH2CI и NHCI2 -связанный хлор. Бактерицидность хлора больше при малых значениях pH, поэтому воду хлорируют до ввода подщелачивющихся реагентов.
Дезинфекция питьевой воды осуществляется за счёт дозирования. Необходимая доза вещества устанавливается пробным хлорированием воды. Она определяется хлорпоглощаемостью воды (количество хлора, необходимое для связывания содержащихся в воде органических соединений). С целью уничтожения микробов хлор вводят с избытком из того расчёта, чтобы через 30 мин после хлорирования воды содержание остаточного хлора было 0,3-0,5 мг/л для хозяйственно-питьевых вод.
Более чем вековой опыт использования метода обеззараживания воды хлором позволил выявить отдельные его недостатки:
1. Хлор является сильнодействующим ядовитым веществом, поэтому все предприятия, его использующие, являются объектами повышенной опасности.
2. Необходимость точной дозировки.
3. Необходимость обеспечения хорошего смешивания хлора с водой и достаточной продолжительности их контакта (не менее 30 мин).
4. Возможность утечки хлора при использовании напорных хлораторов.
5. Необходимость хранения большого запаса хлора. Так как из одного баллона (при комнатной температуре) может быть получено около 0,5-0,7 кг хлора в час, то при большом его расходе может возникнуть необходимость одновременного использования значительного числа баллонов.
6. Соблюдение особых правил при устройстве хлораторных установок, требования которых направлены на защиту обслуживающего персонала отдействия хлора.
В настоящее время наиболее перспективным методом является метод обеззараживания воды гипохлоритом натрия (№СЮ), который позволит избежать опасности при транспортировке и хранении токсичного газа. Данный реагент получают на станциях в процессе электролиза раствора поваренной соли.
Цех для производства и дозирования раствора гипохлорита натрия (дезинфектанта) (рис. 1) состоит из:
• двух водонагревателей для подогрева воды в холодное время года;
• первого главного ввода воды с фильтром обратной промывки;
• редуктора и манометра;
• двух ёмкостей для приготовления раствора соли;
• одной сдвоенной установки умягчения воды, оборудованной блоком управления, переключением и регенерацией;
• двух установок электролиза;
• двух ёмкостей приёма и хранения гипохлорита натрия;
• трёх станций дозирования готового раствора в водоводы.
Для приготовления раствора соли и электролиза необходимо использовать умягчённую воду, чтобы уменьшить количество отложений солей жёсткости на электроде (рис. 2).
Для приготовления насыщенного соляного раствора имеются две ёмкости, называемые солерастворителями, или сатураторами. Соль загружается в ёмкость вручную, а вода поступает автоматически через механический клапан.
Для того, чтобы Вам было проще разобраться в особенностях очистки воды, мы подготовили несколько статей. В них описано, какие методы очистки воды мы используем и как они работают.
- Анализ воды
- Обезжелезивание
- Умягчение
- Сероводород
- Обеззараживание
- Комплексная очистка
АНАЛИЗ ВОДЫ. О ЧЕМ ОН ГОВОРИТ.
Давайте разберемся, что из себя представляет анализ воды. Какие показатели носят информационный характер, а превышение каких могут негативно отразиться на здоровье и бытовой технике.
Как правило, протокол исследования воды выглядит следующим образом:

Анализ воды может делаться на разные параметры, но необходимыми для подбора водоочистного оборудования являются: рН, цветность, мутность, железо общее, марганец, перманганатная окисляемость, общая жесткость, солесодержание или сухой остаток, аммоний.
Рассмотрим подробнее каждый из них:

рН (водородный показатель): это показатель характеризующий баланс ионов водорода (H+) и гидроксид-ионов (OH−). Нейтральной считается величина, равная семи. При значении ниже семи вода обладает кислотными свойствами, выше- щелочными. При подборе фильтрационного оборудования следует учитывать этот параметр, так как в кислой среде вещества находятся в растворенном виде, и трудно окисляются. В щелочной же среде элементы быстро окисляются, и их легче удалить из раствора.
Мутность: этот показатель говорит о наличии взвешенных частиц, например песка, глины, окисленного железа. Следует учитывать, что при высоком содержании растворенного железа вода из источника будет выглядеть прозрачной, но пока ее доставят в лабораторию, железо окислится и вода помутнеет. Для правильного подбора фильтра нужно обязательно сообщить об исходном состоянии воды, была она мутной или прозрачной.
Цветность: показатель качества воды, обусловленный главным образом присутствием в воде гуминовых и фульфовых кислот (органики), а также соединений железа. Как правило превышение цветности говорит либо о высоком содержании железа, либо о высокой перманганатной окисляемости, о которых позже.

Железо общее: железо в воде присутствует в трех формах, двухвалентное (Fe2+), трехвалентное (Fe3+) и органическое. Двухвалентное железо- это растворенная форма, оно прозрачно в воде, не имеет запаха. При контакте с кислородом железо окисляется и переходит в растворе в трехвалентную форму. Это нерастворимое железо. Именно оно дает желтый цвет и железистый запах. Из-за того, что железо довольно быстро окисляется, не имеет смысл делать анализ на Fe2+ и Fe3+ по отдельности, пока проба доедет до лаборатории часть железа поменяет форму. Трехвалентное железо удаляется осадочным методом, он дешевле остальных и не требует реагентов. Для перевода двухвалентного железа в нерастворимую форму используют как правило аэрацию. Про органическое железо (перманганатную окисляемость) расскажем в соответствующей теме.
Марганец: этот элемент неотступно следует за железом. С высокой вероятностью при превышении железа превышен и марганец. Марганец удаляется теми же методами, что и железо, но намного сложнее. На эффективность удаления марганца прямо влияет уровень рН.
Перманганатная окисляемость: показывает уровень содержания органических соединений железа. Эти соединения слишком малы, чтобы их задержать осадочным методом и стойки к окислению. В системах с аэрацией окисление происходит уже после прохождения системы очистки воды. Для удаления органического железа используется либо сильный окислитель, такой как гипохлорит натрия, либо анионообменная смола. Использование реагента менее предпочтительно, так как нужно предусматривать ступень удаления излишков этого регента, что увеличивает стоимость оборудования. Минусом же ионообменных смол является полное умягчение воды.

Общая жесткость: характеризует величину содержания солей кальция и магния в воде. Именно эти соли образуют накипь на нагревательных элементах чайников, стиральных машин, бойлеров, и т.д. Самым эффективным способом их удаления является ионный обмен, в ходе которого специальная фильтрующая загрузка задерживает ионы кальция и магния, взамен отдает в воду натрий. Натрий абсолютно безвреден для организма и техники. После того, как натрий на загрузке кончится, он восстанавливается в процессе регенерации таблетированной солью. Раствор соли (NaOH) возвращает в загрузку натрий, а хлориды натрия и кальция сливаются в дренаж. Если кроме солей жесткости нет других превышений, то путем подмеса исходной воды можно сделать уровень жесткости комфортным.
Солесодержание (сухой остаток): о содержании солей можно судить по количеству сухого остатка в 1 литре воды и потере его веса при прокаливании. Сухой остаток, образующийся при выпаривании воды, состоит из минеральных солей и нелетучих органических примесей. При прокаливании сухого остатка органические соединения удаляются, и остаются только соли. Наибольший вклад в общую минерализацию воды вносят распространенные неорганические соли (бикарбонаты, хлориды и сульфаты кальция, магния, калия и натрия), а также небольшое количество органических веществ. При высоком солесодержании используются установки обратного осмоса.
Аммоний: в природных водах источником накопления вещества служат продукты разложения и жизнедеятельности различных организмов. Однако большая часть ионов аммония попадает в воду со стоками животноводческих ферм, сельскохозяйственных полей, промышленных предприятий. Высокая плотность содержания аммония может быть в водоёмах, находящихся вблизи от коммунальных очистных сооружений, канализации и выгребных ям. Для удаления аммония используются окислители, например гипохлорит натрий, ионообменные смолы и цеолиты.
Важно понимать, что чем подробнее будет анализ, тем качественнее будет подобрано оборудование. Системы очистки воды подбираются индивидуально под каждый конкретный анализ.

Проблема обеззараживания природных вод возникла в 80 – е годы XIX века после установления истинной причины появления водных инфекций. В настоящее время хорошо известно, что вода может быть источником распространения тяжелых инфекционных заболеваний и естественно, что профилактика этих заболеваний является одной из важнейших проблем в комплексе санитарно-гигиенических мероприятий проводимых на станциях водоподготовки и водоотведения. В статье мастер сантехник расскажет о применении гипохлорита натрия для обеззараживания воды.

В настоящее время существуют различные методы обеззараживания воды: ультрафиолетовое и ионизирующее излучение, озонирование, бромирование, хлорирование , серебрение, термообработка, микрофильтрование и др. Каждые из этих методов характеризуются своими достоинствами и недостатками.
Но наибольшее практическое применение получили методы обеззараживания газообразным хлором или веществами, содержащий активный хлор, которые дают гарантии потребителю, предусмотренными ТКП 45-4.01-31-2009 (02250) и ТКП 45-4.01-181-2009 (02250).
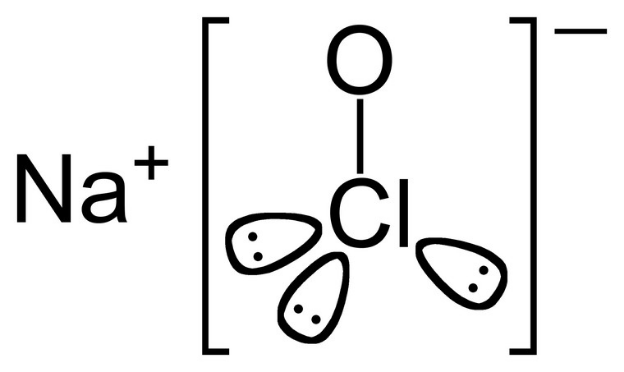
Гипохлорит натрия, или натрий хлорноватистокислый (ГПХН) – это соединение неорганической природы с формулой NaOCl. В безводном состоянии выглядит как твердая масса из бесцветных кристаллов, не отличающаяся устойчивостью. В воде растворяется хорошо. В виде водного раствора с характерным хлорным запахом, а также значительным коррозионным воздействием.
Водные растворы Гипохлорита натрия весьма неустойчивы и со временем разлагаются даже при обычной температуре (со скоростью 0,08 до 0,1 % в сутки). На скорость распада ГПХН влияет воздействие солнечного света, наличие катионов тяжелых металлов и хлоридов щелочных металлов. При этом наличие в водном растворе сульфата магния или кальция, борной кислоты, силикатов и пр. замедляют процесс разложения ГПХН. Следует заметить, что наиболее устойчивы растворы с сильнощелочной средой (значение pH > 10).

Микроэлемент стал известен в 18 веке, когда известный химик К. Шееле открыл элемент хлор. Позже Бертолле обнаружил, что при растворении газа в воде образуется кислотная смесь, которая оказывает отбеливающее и дезинфицирующее действие. Смесь была названа белильной жидкостью, централизовано основали ее массовое производство. Со временем стало ясно, что в данной форме хранить и транспортировать вещество неудобно, так как оно начинает быстро разлагаться под влиянием света, температуры, просто на открытом воздухе. Способ получения компонента был доработан и усовершенствован – едкий хлор стали пропускать через поташ. В результате получался стабильный KCLO. Соединение было названо жавелевой водой, стало активно использоваться в бытовых целях.
Единственный недостаток поташа – высокая цена. В начале 19 века А. Лабаррак заменил поташ на дешевую каустическую соду. Натрий гипохлорит NaCLO до сих пор активно применяется в разных хозяйственных отраслях.
Плотность гипохлорита натрия составляет 1250-1265 кг/м³. Кристаллы на открытом воздухе самопроизвольно плавятся и становятся жидкими. Цвет водного раствора бледно-зеленый, слабый характерный запах присутствует. Соединение начинает быстро разлагаться при внешних воздействиях, попадании в емкость посторонних предметов. Вероятно выделение токсичного хлора, опасного для органов зрения и кожи. Окисляющая реакция сильная.
Натрий гипохлорит из водного раствора выделяется выпариванием с образованием игольчатых кристаллов. С учетом условий среды при разложении могут образовываться различные вещества и продукты. В обычных условиях это соль с кислородом, при нагревании – соль поваренная и хлорат натрия. При действии кислот реакция сопровождается выделением свободного хлора. Окислительные свойства выражены со всеми восстановителями. Соли преобразуют сульфита с нитритами в сульфаты и нитраты, растворяют мышьяк и фосфор с образованием кислот, переводят аммиак в гидразин. Коррозионные свойства выраженные, поэтому вещество для обработки металлических изделий не используется. Главное действие – окисляющее.
- Первый – хлор пропускается через гидроксид натрия раствор с получением конечного продукта. Это химический способ;
- Второй вариант – электрохимический. Он предполагает подвергание электролизу раствора NaCL либо морской воды. Оба решения находят свое повсеместное применение на производствах. Лабораторный синтез предполагает получение малых порций продукта. Он предполагает пропускание хлора через раствор каустика/карбоната натрия.
Основными достоинствами технологии обеззараживания воды гипохлоритом натрия является безопасность его применения и значительное уменьшение воздействия на окружающую среду по сравнению с жидким хлором.
Предлагаемый метод отличается высокой степенью экологической и промышленной безопасности, не требует создания системы нейтрализации аварийных выбросов, мероприятий по охране окружающей среды и защите обслуживающего персонала.
Гипохлорит натрия обладает выраженным бактерицидным эффектом, под действием которого бактерии и вирусы, находящиеся в воде, погибают в результате окисления веществ, входящих в состав протоплазмы клеток, что при относительно низкой стоимости и простоте получения гипохлорита натрия обеспечивает его широкое применение для обеззараживания на различных объектах.
Дезинфекция насосных скважин и водонапорных башен, резервуаров и трубопроводов, предотвращение биологического обрастания в системах водяного обогрева и охлаждения.
Применение для удаления органических веществ из поверхностных вод при первичном хлорировании, при вторичном — обеспечение консервирующего и последействующего эффекта.
Дезинфекция и очистка хирургического инструмента, диализаторов, эндоскопов, обработка кожных покровов. Дезинфекция посуды, игрушек, пластмассовых и крашеных поверхностей, линолеума, санитарных хранилищ, помещений, одежды. Устранение неприятных запахов.
Применение при обработке бытовых и промышленных сточных вод, для деструкции животных и растительных микроорганизмов, устранения запахов (особенно образующихся из серосодержащих веществ), обезвреживания промышленных стоков, в том числе содержащих цианистые соединения, удаления из сточных вод ртути, а также для обработки охлаждающей конденсаторной воды на электростанциях.
Читайте также:

