Магниевый аккумулятор своими руками
Добавил пользователь Валентин П. Обновлено: 04.10.2024
Для того чтобы
ДОБАВИТЬ САЙТ В ЗАКЛАДКИ
Нажмите одновременно
(CTRL+D)
Здесь Вы обнаружите, практические советы, подсказки, идеи, схемы, чертежи, фото. Рассылка пишется для любителей мастерить, строить, самодельничать.
Узнайте первым о новых обзорах "Для умелых рук"
Чтобы прочитать новую цитату обновите страницу,или перейдите на любую другую
Для изготовления гальванического элемента нам потребуется:
1) Большой сосуд (ведро, можно даже дырявое, или что-то в этом роде, можно даже полиэтиленовые пакеты)
2) Цинковую и медную пластину. Если нет пластин, то можно использовать и просто цинковую и медную проволоку, но пластины обладают большей площадью, и дают больший ток.
3) Земля. Да, можете взять и просто накопать земли.
4) Соляной раствор. Тут уж точных рекомендаций не дам. На ведро воды ну пол-пачки соли достаточно.
Все просто - засыпаем землю, втыкам электроды, поливаем, и на концах электродов вы увидите напряжение, порядка 0,5-1В. Конечно немного, но что вам мешает сделать батарею таких элементов? Для зарядки мобильника вполне хватит. Насыпали, залили и идете заниматься своими делами!
Хорошим вариантом самодельного элемента является воздушно-алюминиевый.
Для этого нужно взять алюминиевую фольгу-катод,салфетку пропитать соленой (или морской водой), пробовал также брать кислый флюс, в качестве анода-горка угольного порошка,я брал тонер от картреджей лазерного принтера. Напряжение составляет 0.5-1.0в при токе 10мА
Чтобы сделать гальванический элемент нам необходимо: два электрода, окислитель, восстановитель и электролит.
Возьмем три пластинки: медную, железную и магниевую - они будут служить электродами. Чтобы измерить напряжение, нам необходим вольтметр, для этих целей вполне подойдет цифровой (или аналоговый) тестер. А в качестве "стакана" с электролитом мы используем большой и красивый. апельсин. Сок фруктов и овощей содержит растворенные электролиты - соли и органические кислоты. Их концентрация не очень высока, но нас это вполне устраивает.
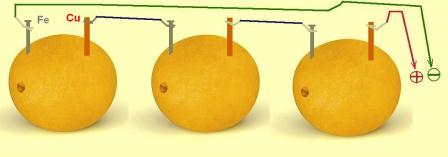

Вместо апельсина можно использовать грейпфрут, яблоко, лимон, луковицу, картофель и многие другие фрукты и овощи. Любопытно, что батарейки из апельсина, яблока, грейпфрута и луковицы давали довольно близкие значения напряжения - разница не превышала 0.1 В. Восстановителем в нашем случае служит железо или магний, окислителем - ионы водорода и кислород (которые содержатся в соке). Обратите внимание, что железо в гальваническом элементе медь-железо заряжено отрицательно, а в элементе железо-магний - положительно. Если у вас нет магния, эксперимент можно провести и с двумя электродами - медным и железным. Вместо железа можно взять цинк или кусочек оцинкованной жести. Цинковый электрод должен дать большую разность потенциалов с медью и меньшую с магнием.

В случае цитрусовых, эксперимент выглядит особенно красиво, если разрезать плод поперек, так, чтобы были видны "дольки" и вставить в них электроды (обычно так разрезают лимон). Если плод разрезать вдоль, это будет выглядеть не так эффектно.



Приведенные цифры не следует воспринимать как абсолютные. Напряжение нашей батарейки зависит от концентрации ионов водорода (а также - других ионов) в соке фруктов и овощей, скорости диффузии кислорода, состояния поверхности электродов и других факторов. Напряжение сделанной вами батарейки может значительно отличатся от того, что наблюдалось в данном эксперименте. Можно соединить несколько фруктовых батареек последовательно - это увеличит напряжение пропорционально количеству взятых фруктов.

Для батарейки из картошки подойдут те же самые материалы, но она даёт меньше напряжения по этому рекомендуется внутрь картошки добавить немного соли, эффект будет намного больше.

На фото снизу:
- часы, как испытательный прибор
- соль
- молотый кофе
- провода
- медные пластины
- алюминиевые пластины
- стакан
- пластиковый разделитель из бутылки

В стакан кладём медную пластину (текстолит, монета, толстая проволока) и алюминиевую нарезку (из пивных банок). Чтобы медь с алюминием не соприкасались, ставим между ними разделитель из любого диэлектрика (пластик от бутылки, кофейная гуща), при этом он не должен мешать свободному протоку воды. К пластинам подсоединяем провода, один к медной и один к алюминиевой. Теперь возьмём воды и добавим туда несколько ложек соли, перемешаем их до полного растворения соли. Наливаем этот раствор в стакан. Всё батарейка сделана.


Кофейная гуща тут чисто для антуража, и чтобы можно было дать красивое название. А так её функция может быть использована для разделения проводников, можно вовсе отказаться от кофейной гущи.
Небольшой парфянский сосуд был найден в Хужут-Рабу, в окрестностях современного Багдада (ныне Ирак), некогда являвшегося частью западных территорий Большого Ирана. В июне 1936 г. возле Багдада прокладывали новую железную дорогу — и рабочие обнаружили древнее захоронение. В процессе последующих раскопок выяснилось, что оно принадлежит к парфянскому периоду (ок. 250 г. до н.э. — 250 г. н.э.).

Впервые этот сосуд был описан немецким археологом Вильгельмом Кёнигом в 1938 г. — он посчитал его очень похожим на электрическую батарею, и опубликовал статью на эту тему в 1940 г.

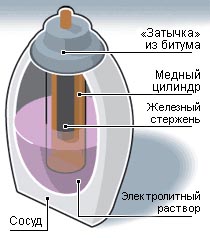
По схожему принципу можно собрать свою батарейку. Берём "сосуд", который можно сделать из: глины, пластилина, бутылки, банки, стакана, вставляем в неё медную пластину закрученную в цилиндр, в этот цилиндр вставляем никелированный гвоздь. Эти пластина и гвоздь являются электродами, они должны немного выглядывать из банки. Для их закрепления в корпусе "сосуда" можно использовать: клей эпоксидный, пластилин, замазку для окон и т.д.
Теперь надо сделать электролит. Он может быть щелочной или кислотный. Для щёлочи надо сделать концентрированный раствор из: вода + соль или вода + сода. Для кислотного подайдёт разбавленная уксусная, щавелевая кислота в воде или можно использовать сок цитрусовых.
Заливаем электролит внутрь банки и тщательно закупориваем "сосуд". Всё Багдадская батарейка готова.


Начитавшись в безграничных просторах интернета про самодельные солнечные элементы, я решил провести свои "эксперименты" в этой области. Я расскажу вам о самом простом способе изготовления солнечных батарей своими руками.
Для начала я решил определиться с элементной базой. Для солнечного элемента нам надо P-N переходы. Они есть в диодах и транзисторах. Решено было выбрать кремниевые транзисторы КТ801. Они выпускались в металлическом корпусе и поэтому их можно открыть не портя кристалл. Достаточно надавить пассатижами на крышку и она отломается.

Теперь разберёмся в параметрах. При среднем дневном освещении, каждый наш транзистор выдаёт 0.53В (База - плюс, а Коллектор и Эмиттер - минусы). А дальше идёт один нюанс. Транзисторы 1972 года выпуска имеет большой белый кристалл, и выдают около 1.1мА. Транзисторы с 1973 по 1980гг. выпуска имеют большой кристалл с зелёным покрытием, и выдают около 0.9мА. Транзисторы выпускаемые позже имеют маленькие кристаллы и выдают всего 0.13мА.
Для эксперимента я использовал батарею из двух параллельных цепочек по 4 транзистора. Под нагрузкой она выдавала около 1.8В, 2-2.5мА. Это довольно скромные параметры, зато как говорится "на халяву". Питать такой батарейкой можно китайские наручные часы, или зарядить аккумулятор и питать светодиод, жучок и др.

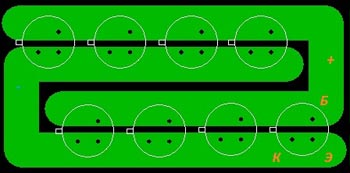
Для удобства крепления и измерений можно закрепить транзисторы на печатной плате как на рисунке ниже. Моё устройство выполнено навесным монтажом, так как это ускоряет сборку.
Вроде бы конструкция стандартна, цинково-медные контакты и подсоленная вода, но тут интересна сама конструкция батарейки.
Нам понадобится:
- лоток для льда
- монеты из меди/медного сплава
- монеты из никеля/алюминиевой бронзы/цинка
- скрепки
- соль
- вода
- светодиод (для проверки)
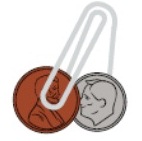
Чтобы получить батарею, необходимо соединить монеты в электроды и залить их электролитом. В каждой ячейке лотка необходимо разместить две монеты из разных сплавов, например медную и никелевую. Далее соединяем последовательно все ячейки с помощью скрепки. Прижимая к одной стороне стенки медную монету, а с другой никелевую закрепляем их скрепкой. После этого в каждый лоток необходимо залить электролит: соль+вода. Обратите внимание на концы лотка, так как ячейки идут в два ряда то, с одной стороны нам надо их соединить, а с другой должно остаться без соединения.
Теперь проверяем работоспособность батареи с помощью диода или мультиметра, для этого замыкаем им две не соединённые ячейки.
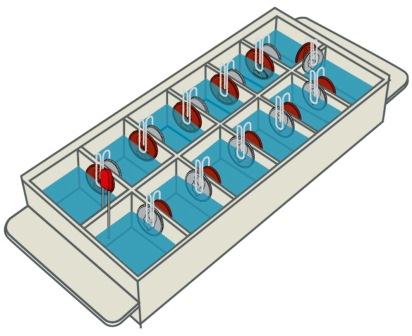
Одна ячейка производит электричество напряжением 0,5 в, а соединённые в одну батарею - 2 в и 110 мА. По этому желательно один электролит на все ячейки, а не разнородный.
Особенности:
1. Ячейка должна быть полностью залита электролитом, но контакт должен быть только с монетой, а не скрепкой.
2. Одна из пар ячеек не должна замыкаться между собой.
3. Цинковые монеты используются в качестве положительных электродов, а медные - отрицательные.
4. Монеты должны быть из разных металлов/сплавов (медь и никель), желательно так же отсутствие одинаковых примесей в сплавах.

Теперь мы изготовим достаточно простое устройство, а точнее источник питания - самодельный аккумулятор напряжения. Как известно, два разных металла погруженные в раствор электролита, способны в себе накапливать электрический ток. В качестве электродов было решено использовать медную и алюминиевую фольгу (на мой взгляд они самые доступные).

Кроме фольги нам еще понадобится - лист бумаги, прозрачный скотч и сам сосуд, в котором мы поместим банку аккумулятора (очень удобно использование стеклянного сосуда из - под нафтизина или валериановых таблеток).


Фольги почти одинакового размера, только алюминиевая фольга чуть длиннее, причины этому нет, просто на медную фольгу легче нанести припой, чем на алюминиевую и провод к фольге не припаян, просто свернут в нее затем зажат при помощи плоскогубцев.

Далее обе фольги были завернуты в лист бумаги. Не допустимо касание металлов друг к другу, между ними ограждением служит лист бумаги. Затем фольги нужно взять вместе и завернуть в кружок и обмотать ниткой или прозрачным скотчем.

Затем изготовленный сверток нужно поместить в сосуд. После этого берем 50 мл воды и разбавляем в нее 10 - 20 граммов соли. Раствор хорошенько перемешиваем и подогреваем до тех пор, пока вся соль не расплавится.

После расплавления соли раствор заливаем в сосуд, где у нас готовая заготовка для нашего самодельного аккумулятора. После заливки ждем несколько минут и измеряем напряжение на проводах аккумулятора.
Забыл уточнить полярность аккумулятора, медная фольга - плюс питания, алюминиевая соответственно минус. Измерения покажут напряжение порядка 0,5-0,7 вольт. Но первоначальное напряжение ни о чем не говорит. Нужно зарядить наш аккумулятор. Заряжать можно от любого источника постоянного тока с напряжением 2,5-3 вольт, зарядка длится пол часа. После зарядки опять измеряем напряжение, оно возросло до 1,3 вольт и может достигать до 1,45 вольт. Максимальный ток такого самодельного аккумулятора может достигать до 350 миллиампер.
Можно изготовить несколько таких аккумуляторов и использовать как резервный источник питания скажем для светодиодной панели или фонаря. Для повышения мощности аккумулятора можно использовать фольгу больших размеров, но конечно такой самопальный аккумулятор держать заряд будет не очень долго (в течении одной недели заряд иссякнет), еще один минус - малый срок службы (не более 3 месяцев), поскольку на меди образуется оксид а во время процесса заряд-разряд алюминиевая фольга начинает поддаваться коррозии и постепенно разделится на мелкие кусочки, но думаю для экспериментов стоит попробовать собрать такой простенький аккумулятор.
Имея немного свободного времени и желания, легко собрать из подручных материалов переходник-адаптер для питания различных гаджетов от внешнего источника питания. Что понравилось в данной статье, так это простота такого адаптера. Опишу подробнее технологию изготовления. Думаю, она окажется полезной кому-то ещё, тем более, что ничего сложно здесь нет абсолютно.
За материалом даже никуда не ходил. Как раз на столе валялась старая карточка МТС. Не зря же сто рублей платил. Померил, в аккурат подходит для изготовления модели одного аккумулятора для фотика.
Раскройка картона:


Даже обрезков осталось совсем немного.
Картон, что и надо - жесткий, толщина где-то 0.25 мм. Сделал разметку и надрезал по швам. Картон не прорезал насквозь, а примерно чуть больше половины толщины, чтобы легче было сгибать и клеить. Для контактов расклепал медную проволоку 1.5 квадратных миллиметра. Получилось примерно так.

Припаял провода и проклеил все швы на два раза клеем ПВА "Момент СТОЛЯР". Швы тоненькие, поэтому пришлось мазать кончиком зубочистки терпеливо, по капельке… Хотя, если кому не терпится, можно и скотчем склеить.
Подключаем к "вампирчику" и работаем:


Подключил, всё заработало.
Пока обнаружилось только одно неудобство - провод. Толстый, тянется к фотоаппарату и к "вампирчику" Поэтому задумал пристроить к камере такой же аккумулятор, как в "вампирчике", только с защитой. Кстати, аккумуляторы с защитой здесь ставить не обязательно, т.к. фотоаппарат уже имеет встроенный измеритель уровня заряда и при разряде аккумулятора он просто не включится.
И не забывайте соблюдать полярность.
Дорогой посетитель. Если Вам нравятся страничка, поделитесь ею с друзьями
в т.ч. гостей: 104
пользователей: 0
Заголовок не совсем точен - эта статья, скорее, введение в понимание работы ветряка и на что следует обратить внимание в первую очередь при желании самостоятельно его изготовить.
Описана распространенная плата БМС для литиевых аккумуляторов. Дана схема и некоторые ее доработки для более стабильной работы.
Относительно простая доработка солнечной батареи с USB выходами для увеличения снимаемой с нее мощности и получения возможности заряжать внешние LiIon аккумуляторы.
Рассмотрена простая схема "идеального" диода. Работа схемы разобрана до мелочей, поэтому собрать ее сможет даже полный "чайник" в электронике.
Используя физический принцип радиационного охлаждения неба, команда смогла собрать небольшое, но полезное количество энергии из холодного ночного неба, используя простое, недорогое и некритичное устройство.
Как влияет на характеристики Li-Ion аккумулятора его глубоких разряд (вплоть до нуля)? Насколько он вреден, или, наоборот, относительно безопасен? В статье попытка разобраться с этим. Не на профессиональном, конечно, уровне, но как информация к размышлению.
Продолжение описания сборки самодельного модульного накопителя на LiFePo4 аккумуляторах.
Обзор конструкции самодельного модульного накопителя, доступного для самостоятельного изготовления и по многим характеристикам не имеющего аналогов среди тех, что можно купить. Много фото.
Весьма неплохая платка повышающего преобразователя, поддерживающая протоколы быстрой зарядки.
Алмаз, графит, древесный уголь – это все углерод в различных трехмерных кристаллических решетках. Но нас интересует новый вид кристаллов, двухмерный, плоский. Он назван графеном и имеет выдающиеся свойства. Расщепить кристаллы на молекулярном уровне удалось совсем недавно, в 2004 году. Огромный поверхностный заряд материала обусловлен плоской структурой. Для использования в электротехнике важны и другие свойства – отличная тепло- электропроводность, увеличение допустимой мощности микроэлектронных схем. При толщине поверхности 91*10 -12 м или 91 пикометра, на ней удерживается вес в 4 кг. Для аккумулятора важно, что тонкий слой графена принимает заряд мгновенно, и аккумулятор емкостью 55 А/ч заряжается за 8 минут.

Устройство графенового аккумулятора
Расщепленный кристалл стремится снова стать объемным. Ученым удается сдерживать двухмерную структуру и заставить работать в виде гальванического элемента. Стабильность зависит от подобранной электронной пары. Устройством аккумулятор напоминает литий-ионные, но вместо графитового слоя внедрен графеновый.
Ученые прогнозируют, будущее за графеновыми аккумуляторами. Их плюсы неоспоримы, а минусы минимальны. Но создать устойчивые компоненты, закрепить двухмерность углерода не просто.
Зарубежные научные корпорации пошли по пути создания графеновых накопителей энергии с электролитом в виде LiCoO2. Идут разработки, уже имеется опытное производство аккумуляторов с 2015 года. Первой стала испанская компания Graphenano. На зарядку графенового аккумулятора требуется всего 8 минут. При этом заявлено, что емкость литий-графеновых аккумуляторов в 10 раз больше, чем литий-ионных.
Российские исследователи заменили анод оксидом магния. Композиция дешевле, меньше нагревается аккумулятор и уменьшается опасность возгорания. Ученые прогнозируют емкость новых, магниево-графеновых аккумуляторов, больше литиевых в 2,5 раза.
Не остались в стороне разработчики в области IT-технологий. Графеновые аккумуляторы входят в производство. Уже в 2018 году эксперты из компании Elecjet выпустят портативный заряжающий аккумулятор USB-C на графеновой основе. Зарядить телефоны iPhone 5,6,7 можно будет за 5-10 минут.
В январе 2018 года компания Samsung обещала поставить в торговые сети новый смартфон Galaxy S9 с настоящей графеновой батареей. При емкости в 3000мА/ч заряжаться телефон будет 15 минут. Компания получила патент на графеновый аккумулятор для смартфонов и будет единственным мировым поставщиком.
Графеновый аккумулятор для электромобиля

В основном разработки ученых направлены на создание крупных аккумуляторов для транспорта. Автомобильный пробег на одной зарядке модели Tesla Mobil S составляет 800-1000 км, скорость зарядки 10-12 минут. Транспорт экологически чистый. С развитием производства графеновых аккумуляторов неизбежно строительство сети зарядных станций.

Производство графеновых аккумуляторов перспективно. Именно такого емкого и быстро заряжающегося источника энергии не хватает для развития электромобилей. Важно и то, что весит новый аккумулятор в 2 раза меньше литий-ионных батарей. Его механические свойства идеально вписываются в условия эксплуатации машин. Графен в 200 раз прочнее стали, эластичный. Первые опытные образцы уже проходят испытания.
Графеновый аккумулятор для квадрокоптера

Любой летательный аппарат эффективности полета и его дальности обязан бортовой АКБ. При выборе источника энергии важны емкость, токоотдача, вес и габариты. До появления графеновых аккумуляторов непревзойденными качествами обладали литий-полимерные. Но они склонны к возгоранию при перезаряде и нагревании. Этих недостатков лишены магний графеновые аккумуляторы. Купить некоторые из образцов уже возможно.
Лучшим считается аккумулятор в жестком корпусе Turnigy Graphene 5000 mAh 2S2P. Новая батарея поддерживает высокую выходную мощность, под нагрузкой остается холодной. При этом батарея обеспечивает разряд 90С постоянно и 130С кратковременно. Вес конструкции с проводами и разъемами 291 грамм. Заряжается быстро с потреблением тока до 15 С, от LiPo зарядки.
Есть и другие аккумуляторы, разработанные на основе графеновых составляющих от разработчика Graphene. К ним относится:
- модель FlyMod от компании ONBO Power;
- Dinogy Ultra Graphene 02 4S 80C – вторая доработанная модель;
- Thunder Power Adrenaline – лучшие модели для продолжительных полетов.

Графеновый аккумулятор своими руками
Уже понятно, создать двухмерную структуру графена и закрепить его свойства – задача не из простых. Ученые всего мира работают над проблемой. Сделать в кустарных условиях графеновый аккумулятор невозможно.
Но усвоив, что слой углерода должен быть микроскопически тонким, мастера получают такой разными способами. Они истирют графит в тонкодисперсный порошок, производят химическую обработку, наносят его на подложку из алюминия. Предлагаем ознакомиться с одним из способов получения нужного состава.
Есть способы сбора угольной пыли на липкую ленту, выжигание лучом лазера с получением чешуйчатого материала, растворение графита в смеси азотной и серной кислот. Высохший осадок выжигают в установке, получая легкие хлопья. Считают этот вид сажи графеном и работают с ним.
Видео
Предлагаем посмотреть видео и оценить один из способов получения гибкого графенового аккумулятора своими руками.

Приветствую Други! Выставляю на обозрение очередную самоделку.
Т.к. я немного заморочен на энергенике во всех её проявлениях, решил попробовать. итак:
Покопавшись на свалке интернета, я нашёл много информации о том, как сделать походную соляную батарейку.
Для этого использовались различные материалы. Для получения гальванической пары нужны были такие металлы как Цинк+ медь, Алюминий+медь. Это основные материалы которые обще доступные. Но я пошёл несколько иначе. Нашёл, путём разных экспериментов такую пару как Магний+медь. Эта пара выдавала максимальное напряжение и ток в соляном растворе. (1.2-1.4 вольта)
Начнём по порядку.
В качестве корпуса я использовал корпус аккумулятора от скутера (Спросите там где занимаются ремонтом скутеров, у них можно мешками набрать)
Раздолбал его. ОСТОРОЖНО. ТАМ КИСЛОТА. ЕЁ НАДО СЛИТЬ И ОСТАТКИ ДЕАКТИВИРОВАТЬ РАСТВОРОМ СОДЫ. и пусть рядом тоже будет сода, потом руки помоете.
Теперь вопрос, ГДЕ взять магний?
Ответ довольно прост. Корпус двигателя от запорожца, старых немецких автомобилей. Ну и на худой конец, аноды от электрических Водогреек. Они так и называются Магниевые аноды.
Отпиливаем лишние штырьки, распиливаем пополам. и из 3-х анодов получаем 6 маленьких(на фото пока 4, т.к. 2 уже в работе).
Далее делаем с медной проволокой вот так!
и прикручиваем к магнию (я использовал болтики М3 с предварительной нарезкой резьбы)
потом все эти пары загружаем в подготовленную ёмкость.
Помните! Что на Магнии будет отрицательный потенциал, а на меди положительный.
теперь заливаем просто солёную воду и делаем замеры. Напряжение питания 7.7 вольта (холостой ход)
теперь ток короткого замыкания почти 70 мА. На самом деле, поиграйтесь расстояниями между пластинами, площадью пластин и раствором воды с солью. Лично я получал и 150 мА(не изменяя форму пластин).
кому ток маленький, его можно увеличить за счёт увеличения площади пластин, в частности можно расплющить магний и медь навить на пластинку. Чем больше площадь, тем больше ток.
ну и испытания просто на последовательно спаянных светодиодов мощностью по 0.2 ватта каждый
Помните! эта статья рассказывает о возможности такого девайса в походе. Все доработки и ньюансы делайте сами. А не указывайте Мне как лучше надо было сделать. Хотите лучше сделать? ДЕЛАЙТЕ.
При копировании статьи, указывайте автора и ресурс!
Всем Бобра!
35 комментариев
Ну я по тому же принцыпу делал, ваще на коленке… из рюмок, фольги и медных проводов. Макс, а в чем плюс магния то? Так я и не понял что-то. По вольтажу тоже самое что и у меня выходит.
а я нифига советовать не буду, потому что в этой теме дуб дубом.Максим молодец, скажи только, принципиально чтоб ёмкость разделена была, или можно и в ведре?
ну рюмки таскать с собой ))))) я как бы это всё облагородил… магний более активный, и он всё таки больше выдаёт напряжение… фольгу быстрее разъест чем кусок магния.
Пластиковые стаканчики в каждом лесу валяются.Вот их вместо рюмок можно забацать.А если ведра пластиковые найти, то ооочень долго будут работать. :-)
развернул статью, появилась мысль, а дай-ка угадаю, кто автор статьи… и не ошибся! )))
спасибо за интересный опыт.
Не, ну про магний я не верю исходя из химии хотя бы

Гальвани́ческий элеме́нт — химический источник электрического тока, основанный на взаимодействии двух металлов и (или) их оксидов в электролите, приводящем к возникновению в замкнутой цепи электрического тока.
Грубо говоря, свободные электроны от отрицательно заряженного металла по средствам электролита будут двигаться к положительно заряженному металлу. Теперь смотрим на таблицу алиментов элементов Менделеева на магний — Магний (лат. Magnesium), Mg, химический элемент II группы периодической системы Менделеева, атомный номер 12, атомная масса 24,305.
Теперь Цинк — Цинк (лат. Zincum), Zn, химический элемент II группы периодической системы Менделеева; атомный номер 30, атомная масса 65,38,
Ну и у кого количество электронов больше при атомной массе цинка почти втрое больше чем у магния.
У магния их 12, у цинка 30 и кто будет давать больший поток электронов, а следовательно и электричества ?!
Читайте также:

