Как сделать эмбрион человека
Добавил пользователь Alex Обновлено: 18.09.2024
Пн – Пт с 9:00 до 21:00
Суббота с 9:00 до 17:00
Воскресенье и праздничные дни - в индивидуальном графике
Адрес: г.Москва, улица Советской армии, 7 (м. Достоевская)
Какие эмбрионы лучше: 3-хдневные или 5-тидневные?
Если получилось мало эмбрионов, нужно ли их доращивать до 5 суток?
На начальных этапах развития экстракорпорального оплодотворения (ЭКО) эмбрионы переносили в полость матки на 1е и 2-е сутки после проведения пункции. К настоящему времени наука шагнула далеко вперед и в лаборатории можно создать оптимальные условия для культивирования эмбрионов до стадии бластоцисты (5-е сутки развития). Это стало рутинной практикой благодаря внедрению нового оборудования, такого как мультигазовые инкубаторы, а также новых сред для культивирования эмбрионов.
Перенос эмбрионов в матку на стадии бластоцисты повышает шанс наступления беременности по сравнению с переносом эмбрионов на более ранних стадиях. Культивирование эмбрионов до 5х суток является своеобразной селекцией, поскольку не все эмбрионы достигают стадии бластоцисты.
Однако не всем пациенткам можно рекомендовать этот метод. У пациенток со сниженным овариальным резервом, тяжелым мужским фактором высок риск отмены переноса эмбрионов из-за того, что эмбрионы не смогут достигнуть стадии бластоцисты при культивировании in vitro. Следует также отметить, как бы мы ни пытались в лаборатории создать для эмбриона условия максимально приближенные к естественным (in vivo), мы не сможем их воссоздать на все 100%. При культивировании in vitro мы лишь обеспечиваем оптимальный температурный режим, газовый состав окружающей среды, снабжаем эмбрион питательными веществами. В полости матки помимо прочего, эмбрионы получают различные ростовые факторы и клеточные сигналы от окружающих тканей. Исходя из того, что в полости матки эмбрионы получают наиболее оптимальные условия для своего развития, клиники ВРТ практикуют перенос как на 3-и, так и на 5-е сутки развития эмбриона.
Хорошие и отличные эмбрионы - в чем разница? Как их качество влияет на будущего ребенка?
Чем лучше качество эмбрионов, тем выше шанс наступления беременности. Именно поэтому, для переноса в полость матки отбираются эмбрионы с наилучшими морфологическими характеристиками.
Однако иногда бывает, что наилучшими из всего пула эмбрионов являются эмбрионы среднего или низкого качества. Не стоит отчаиваться. Даже в таком случае возможно наступление беременности и рождение здорового ребенка. К настоящему времени не установлено корреляции между качеством эмбриона и здоровьем ребенка.
Почему переносят 2 эмбриона?
При переносе в полость матки двух эмбрионов шанс наступления беременности в среднем повышается на 15%. Следует также учесть, что риск многоплодия также повышается. В том случае, если у пациентки имеются медицинские противопоказания к вынашиванию многоплодной беременности, то следует выполнить селективный перенос одного эмбриона.
Если один эмбрион прижился, а второй нет, что происходит с тем, который не прижился?
К сожалению, не все эмбрионы дают начало новой жизни. Эмбрион, который не имплантировался, мог погибнуть еще до начала процесса имплантации, что может быть связано с генетическими аномалиями самого эмбриона.
Показано, что до 60% эмбрионов человека могут иметь те или иные генетические поломки. Однако не следует забывать, что сам процесс имплантации также довольно сложен. И даже перенос в полость матки генетически нормально эмбриона отличного качества не гарантирует беременность. Принимающая среда – эндометрий –должна обладать морфологической, биохимической, рецепторной зрелостью. Имплантация – также сложный иммунологический процесс, поскольку эмбрион является чужеродным для организма матери. Любые отклонения могут привести к негативному исходу программы ЭКО.
По Законодательству, в нашей стране разрешено переносить 2 эмбриона, свыше двух эмбрионов переносят при отрицательных предыдущих попытках и низком качестве эмбрионов. Для переноса более 2-х между клиникой и пациентом заключается дополнительное соглашение.
Чтобы понять, как ведет себя эмбрион человека в ранние стадии развития, исследователи создали из стволовых клеток его трехмерную модель.

Через несколько недель после зачатии то, что в будущем станет вашим телом, претерпевает существенные метаморфозы и растет как вверх, так и вниз. Однако долгое время для ученых было большой загадкой то, как именно наши клетки узнают о том, куда расти.
Чтобы выяснить это, исследователи создали связку стволовых клеток, максимально приближенную к эмбриону человека на ранних стадиях развития. В результате они получили гораздо лучшее представление о биохимии, лежащей в основе этого процесса в развивающемся человеческом организме.

Ученые в разных странах мира пытаются создать искусственную матку.
Имитация материнства
Самым трудным оказалось воссоздать плаценту, через которую осуществляется связь матери и ребенка. Наладить оптимальный кровоток, гормональный обмен – все это пока науке не под силу. Шаг влево, шаг вправо – и плод погибнет.
Плодный пузырь с эмбрионом прикрепляется к стенкам матки – в этом залог нормального развития, так что вторая проблема, над которой бьются ученые, – выращивание маточных тканей.

Еще одна трудная задача – воссоздание условий, в которых плод растет в материнском чреве. Современные кювезы, предназначенные для недоношенных детей, для этого не подходят. В них новорожденного помещают в сухую среду, между тем все 280 дней до появления на свет для него привычно и, значит, комфортно нахождение в жидкости. Но как имитировать плодный пузырь и околоплодные воды? Сразу возникает вопрос с обеспечением дыхания: вместо привычных трубок скорее всего будут использовать жидкостную вентиляцию легких.
Увы, этот вопрос не всегда тревожит людей, погруженных в науку. Как признается доктор Лиу из США, пытающаяся создать искусственную плаценту, только после явно выраженного недовольства людей она задумалась об этической стороне вопроса. И – отказалась от дальнейшей работы.

Но многие ученые продолжают свои поиски, правда, признаваясь, что имитировать замысел природы – невероятно сложно. Возможно ли создать искусственную матку – это лишь вопрос времени. Более насущный – нужно ли?
Благие намерения
Искусственная матка, безусловно, – благо для недоношенных детей, которых рождается все больше и которых так сложно выхаживать. По словам заведующей акушерским отделением НЦ акушерства, гинекологии и перинатологии им. В. И. Кулакова Натальи КАН, у младенцев, рожденных на 22‑й неделе беременности, летальность доходит до 70%!
Кроме того, новая технология дает возможность стать мамами и бесплодным женщинам, или тем, кто по состоянию здоровья не может выносить своего ребенка.
Но также ясно, что у этой идеи есть и оборотная сторона. Для многих современных женщин материнство не является первоочередной задачей. Они спешат получить образование, сделать карьеру, заработать деньги…
Впрочем, сегодня, рассказывает старший научный сотрудник Института демографии НИУ ВШЭ Ольга Исупова, материнство фактически можно разложить на части: забор яйцеклетки, ЭКО, суррогатное материнство…
Во всем мире растет число бездетных. В России их пока еще 17%, хотя несколько лет назад было вообще только 7%. А в Германии бездетными является уже треть населения. Даже в Китае, как ни парадоксально это звучит, рождаемость падает: сначала это был регулируемый процесс, а теперь люди решили, что чем меньше детей, тем легче жить.
Баланс науки и морали

Яйцеклетки (ооциты) полученные во время трансвагинальных пункций в программе ЭКО
- Эмбриологический этап ЭКО начинается с просмотра фолликулярной жидкости после пункции фолликулов, которая содержит яйцеклетки, которые окружены клетками кумулюса (трофическими клетками, выполняющими питательную функцию). Такие ооциты – кумулюсные комплексы переносят в питательную среду и помещают в инкубатор, где они ожидают оплодотворения сперматозоидами
- Оплодотворение проводится сконцентрированной спермой через 4-6 часов после получения яйцеклеток
- При тяжелых формах мужского бесплодия, при которых существенно снижена оплодотворяющая способность спермы, выполняется процедура ИКСИ (интрацитоплазматическая инъекция сперматозойда).
День 1. Эмбрионы — оплодотворенные яйцеклетки
- Через 16-18 часов после того, как яйцеклетки и сперматозоиды помещаются вместе, проводится оценка оплодотворения. Оплодотворенная яйцеклетка имеет два пронуклеуса, представляющих хромосомы от мужчины и женщины и двух полярных тел, хромосом, которые были экструдированы после завершения мейоза.
- Иногда мы увидим три пронуклеуса в оплодотворенной яйцеклетке, это значит, что в оплодотворении учавствовал более, чем один сперматозоид или это может свидетельствовать об аномалиях развития сперматозоида в процессе сперматогенеза или яйцеклетки в оогенезе. Такие яйцеклетки, а так же неоплодотворившиеся яйцеклетки в дальнейшем не используются. Нормально оплодотворившиеся яйцеклетки продолжают культивировать дальше.
День 2. Эмбрионы — классификация качества
- На 2-е сутки после слияния генетического материала сперматозоида и яйцеклетки происходит дробление – деление клетки на две.
Клетки дробящего эмбриона называются бластомерами. На этой стадии можно оценить качество эмбриона по степени фрагментации (объему эмбриона, занимаемому безъядерными фрагментами цитоплазмы), считается, что чем она больше, тем ниже считается потенциал этого эмбриона к имплантации и дальнейшему развитию. Помимо фрагментации оценивается форма и относительные размеры бластомеров (T. Hardson, 2001). - Наиболее общепринятая классификация дробящихся эмбрионов по качеству – A-B-C-D, где А – самый лучший, D – самый худший. Цифрами указывают количество бластомеров.
Оценка качества эмбрионов по степени фрагментации (A. VanSteiterghemetal., 1995)
— Тип A — эмбрион отличного качества без ануклеарных (безъядерных) фрагментов (4А)
— Тип В — эмбрион хорошего качества с содержанием ануклеарных фрагментов до 20% (4В)
— Тип С — эмбрион удовлетворительного качества с содержанием ануклеарных фрагментов от 21% до 50% (4С)
— Тип D — эмбрион неудовлетворительного качества с содержанием ануклеарных фрагментов более 50% (4D)
День 3. Эмбрионы
День 4. Морула
На 4-е сутки развития эмбрион человека состоит уже, как правило, из 10-16 клеток, межклеточные контакты постепенно уплотняются и поверхность эмбриона сглаживается (процесс компактизации) – начинается стадия морулы (от лат. Morulae – тутовая ягода). Именно на этой стадии invivo (в организме матери) эмбрион попадает из маточной трубы в полость матки. К концу 4-х суток развития внутри морулы постепенно образуется полость – начинается процесс кавитации.
День 5. Бластоцисты
Перенос бластоцисты (перенос на 5-е сутки) имеет большую частоту успешной имплантации, позволяя переносить меньшее количество эмбрионов высокого качества, снижать риск многоплодной беременности при увеличении частоты наступления беременности.
- 5-6 день эмбриологического развития.
С того момента как полость внутри достигает 50% ее объема, эмбрион называется бластоцистой - Бластоциста состоит из 2-х популяций клеток – трофобласт (наружный слой) и внутренняя клеточная масса
- Трофобласт отвечает за имплантацию — внедрение эмбриона в маточный эпителий (эндометрий). Клетки трофобласта в дальнейшем превращаются в плаценту
- Внутренняя клеточная масса дает формирование тканям и органам будущего ребенка
- Чем больше полость бластоцисты и лучше развита внутренняя клеточная масса и трофобласт, тем больше потенциал эмбриона к имплантации.
Развитие бластоцисты и имплантация
Вероятность формирования бластоцисты
Преимущества переноса бластоцисты в ЭКО
- При естественной беременности, 2-3 дневной эмбрион обычно находится в маточной трубе не в полости матки.
Эмбрион продолжает свое развитие и, обычно, через 80 часов после овуляции достигает матки - Имплантация эмбриона начинается обычно 2-3 дня спустя, после формирования бластоцисты и ее хэтчинга
- Поэтому, если in vitro культивирование позволяет иметь здоровую бластоцисту, перенос эмбрионов осуществляется на 5-ый день:
- эндометрий полости матки на 5-ый день переноса высоко рецептивен к перенесенному эмбриону, как при естественном зачатии, когда эмбрион попадает в полость матки.
Вспомогательный хэтчинг
Одним из основных факторов, от которого зависит успех лечения бесплодия методом экстракорпорального оплодотворения является способность эмбриона имплантироваться в стенку матки.
Яйцеклетка человека и эмбрион на ранних стадиях развития окружены защитной двухслойной оболочкой (zona pellucida – блестящая оболочка).
Она играет очень важную роль:
- после проникновения сперматозоида в яйцеклетку, оболочка изменяет свою структуру, не пропуская остальные сперматозоиды.
- облегчает транспорт оплодотворенной яйцеклетки по маточной трубе к полости матки.
Оболочка эмбриона может быть очень толстой и плотной, и это может мешать его нормальному прикреплению к стенке матки.
Суть метода вспомогательного хетчинга – искусственное истончение блестящей оболочки эмбриона различными способами:
- механически (с помощью специальных микроинструментов)
- химически (с помощью кислого раствора Тироде)
- с помощью лазера. Это наиболее передовой, быстрый и безопасный для эмбриона способ проведения вспомогательного хетчинга
Для этой процедуры мы используем лазерный аппарат OCTAX Laser Shot ТМ (Германия).
OCTAX Laser Shot ТМ — это передовая лазерная технология для ВРТ с цифровым управлением, цифровой обработкой, использованием последних компьютерных технологий и оптики высокого качества.
Суть метода лазерного хетчинга — это использование лазерного луча, что позволяет сделать высокоточный надрез необходимого размера. Лазерный хэтчинг делается только эмбрионам, предназначенным для переноса. Для этого эмбрион фиксируется микропипеткой и высокоточным лазером делается небольшое отверстие в наружной части его оболочки или несколько насечек для истончения ее слоя.
Лазерный хэтчинг практикуется в ведущих центрах всего мира. Исследования утверждают, что его использование повышает шансы наступления беременности (для пациентов которым показана эта процедура). Нет никаких данных о негативном влияние хэтчинга на результат программы лечения бесплодия, эта процедура абсолютно безопасна для самого эмбриона.
Лазерный хэтчинг назначается:
- Женщинам старше 38 лет, поскольку с возрастом zona pellucida утолщается и становится твердой.
- Пациентам, имеющим предыдущие неудачные попытки ЭКО при эмбрионах хорошего качества.
- При переносах размороженных эмбрионов.
- Пациентам с повышенным уровнем ФСГ
- Женщинам, которые от природы имеют яйцеклетки с толстой zona pellucida.
Криоконсервация эмбрионов
Что же дает эта процедура пациентам, нужна ли она?
Во-первых, когда на пункции яичников было получено большое количество яйцеклеток, а в последствии и нормальных, жизнеспособных эмбрионов. Кстати, такой исход возможен не всегда, и пара которой предложили криоконсервацию — счастливчики.
Это дает некую подстраховку и уверенность в будущем. При удачной попытке в цикле стимуляции хранящиеся эмбрионы можно использовать для рождения второго и третьего ребенка, а в случае неудачи — повторить попытку в естественном цикле без большой гормональной нагрузки и операции.
Во-вторых, бывают случаи, когда врач принимает решение об отказе от переноса при развитии тяжелой формы гиперстимуляции (СГЯ) или по другим медицинским показаниям.
Криоконсервации можно подвергнуть и яйцеклетки. Особенно это актуально в том случае, когда женщина планирует отсрочить материнство до наступления более подходящих социально-экономических условий. С возрастом организм женщины все хуже откликается на гормональную стимуляцию, и получить достаточное количество яйцеклеток хорошего качества не всегда возможно. Новые технологии дают возможность сохранить фертильность пациентам, планирующим химио- и радиотерапию. Криоконсервация в этих случаях дает возможность сохранить молодые, более здоровые яйцеклетки, и в последующем родить своего биологического ребенка.
Сегодня уже более 2000 детей родилось благодаря витрификации яйцеклеток и эмбрионов. К настоящему времени метод был значительно усовершенствован, за счёт улучшения растворов мы добиваемся отличных результатов выживаемости человеческих ооцитов и эмбрионов после оттаивания. Так, выживаемость для бластоцист составляет 99%, а для эмбрионов -98%.
При витрификации (от лат. vitrum — стекло и facio — делаю, превращаю) происходит охлаждение до температуры жидкого азота, и переход яйцеклеток и эмбрионов в твердое, стекловидное состояние. Такой особенный вид заморозки возможен благодаря действию специальных веществ — криопротекторов.
Но криопротекторы — это не естественные для клеток составляющие, они токсичны. Чтобы криопротекторы в меньшей степени успели проявить свою токсичность, процедура витрификации проводится достаточно быстро, в чем и состоит преимущество этого метода заморозки. Только эмбрионы и яйцеклетки, застывшие в виде аморфной стекловидной массы, могут долго сохранять жизнеспособность, а при осторожном размораживании их жизнедеятельность полностью восстанавливается, что повышает возможность наступления беременности.
Полное освобождение от криопротекторов происходит приблизительно за 3 часа. По прошествии этого времени эмбрион полностью восстанавливается и готов для переноса в полость матки, а яйцеклетка к процедуре оплодотворения методом ИКСИ.
Особенностью криоконсервации является уплотнение оболочки яйцеклетки или эмбриона, но эта проблема легко решается. В случае разморозки эмбриона проводят вспомогательный хэтчинг (дополнительное рассечение оболочки для выхода из нее эмбриона и удачной имплантации в эндометрий). А в случае яйцеклеки проводят оплодотворение при помощи ИКСИ, и также вспомогательный хэтчинг развившемуся эмбриону.
Таким образом, витрификация позволяет:
- избежать многоплодной беременности;
- сохранить нормальные жизнеспособные эмбрионы, оставшиеся после цикла ЭКО для последующего переноса;
- родить второго и третьего ребенка без стимуляции в естественном цикле;
- осуществлять программы донорства гамет и эмбрионов;
- сохранить эмбрионы и гаметы у пациентов, проходящих лечение рака;
- сохранить яйцеклетки по другим медицинским показаниям (напр., когда женщина страдает прогрессирующим эндометриозом, у нее нарушается функция яичников и количество яйцеклеток хорошего качества снижается);
- транспортировать биологический материал на любые расстояния.
Все это значительно увеличивает результативность процедуры ЭКО, сокращает ее стоимость и затрачиваемое время и дает возможность оказать помощь большему количеству семей, желающих иметь ребенка.
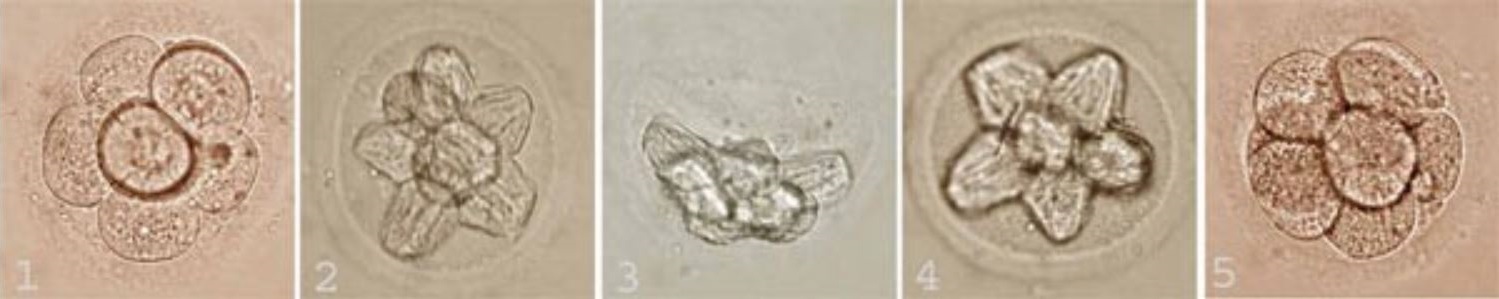
Фотографии эмбрионов человека, полученные на различных этапах витрификации
![Эмбриологические аспекты ЭКО/ИКСИ]()
1 — эмбрион до криоконсервации;
2, 3, 4 — так выглядит эмбрион при температуре жидкого азота (−196 °C) — его клетки сильнее обезвожены, но живы;
5 — восстановление размера клеток эмбриона после разморозки (оттаивания).Записаться на прием к акушеру-гинекологу, репродуктологу вы можете по телефону 8 (831) 411-11-20
Читайте также: