Хроматограмму спирта как сделать
Добавил пользователь Владимир З. Обновлено: 30.08.2024
А что комментировать? Вы скажите что хотели сделать, на каком оборудовании, высота царги режимы и т.д.?
А так – для зерна и фруктов слишком чисто, т.е. ароматики нет совсем.
Для сахара – чистый спирт, примеси на грани, но в пределах ГОСТа. Ну может чутка хвостов перебрали, но это не страшно.
Хорошо живет на свете Винни-Пух.
Прима Тора от альянса. Царги 2х дюймовые общая высота 1.3 метра. Сахарная брага. Однократная ректификация-. До требований ГОСТа- как до столицы Китая. Показатели превышают требования в 7 раз. Вопрос в том, чтобы ориентируясь на показания хроматограммы улучшить продукт. Можете предложить конкретные шаги? Указать наошибки в технологии? Для себя пока вижу увеличение царги на 0.3м ( ограничение по потолку)(уже заказал), замену мочалок на спн (как деньги будут), и больше голов и хвостов отсекать. Колличество фигня, качество наше все. ЗЫ: Пробовал углевать БАУ но это ннаверное в другую тему..
Расчет по группам это что?
Хотелось бы получить рекомендации по уменьшению концентрации примесей в исходнике-браге и как с азеотропными растворами бороться (типа изобутанола. Очень его много). По задумке чистенькой спирт основа всех настоек. Научусь на приме делать достойную водку ( на сахаре), вот тогда буду осваивать вкусные дистилляты. Как то так
Так Вы сами все сказали – СПН нужен. Высоту можно не увеличивать. Головы – первые 10% отсекайте, подход хвостов по термометру и будет счастье в хроматограмме))
Мочалки в разы менее эффективны чем СПН. Разделяющая способность меньше, примесей больше. При всем при этом, когда получите свой супер-чистый спирт, устройте слепую дегустацию водок на его основе, и этого экземпляра. Гарантирую, что разницу невозможно будет почуствовать.)))
У Вас уже отличный продукт, выше стремиться можно только из любви к исскусству))
Хорошо живет на свете Винни-Пух.
Так Вы сами все сказали – СПН нужен. Высоту можно не увеличивать. Головы – первые 10% отсекайте, подход хвостов по термометру и будет счастье в хроматограмме)) Мочалки в разы менее эффективны чем СПН. Разделяющая способность меньше, примесей больше. При всем при этом, когда получите свой супер-чистый спирт, устройте слепую дегустацию водок на его основе, и этого экземпляра. Гарантирую, что разницу невозможно будет почуствовать.))) У Вас уже отличный продукт, выше стремиться можно только из любви к исскусству))
На ХД сейчас обсуждают принудительное контролируемое затопление колонны с насадкой, тоесть переход с плëночного в эмульгационный режим . По расчëтам хозяина форума повышается разделяющая способность почти в 2 раза. Только там опять автоматика не дешовая нужна.есть у меня идея как можно затопить без дорогой автоматики))) только надо пообсуждать
Быстро выпитый стакан не считается налитым.
При всем при этом, когда получите свой супер-чистый спирт, устройте слепую дегустацию водок на его основе, и этого экземпляра. Гарантирую, что разницу невозможно будет почуствовать.))) У Вас уже отличный продукт, выше стремиться можно только из любви к исскусству))
Не-а. Я не капризничаю. 35мл изобутанола в литре продукта дают весьма отчётливый привкус резины-растворителя. И дегустировал продукт стороннего производства ( другой аппарат, насадка спн всего 0,8 м царга) и ещё другого тоже пробовал. Мое хуже. Попробую после работы над ошибками отнести на повторный анализ и образец друга конкурента для сравнения прихватить.
Аннотация научной статьи по химическим наукам, автор научной работы — Адаменко Г. В., Бурак И. И., Колков М. А.
Целью данного исследования была разработка чувствительной методики количественного определения спирта этилового в комбинированных антисептических спиртосодержащих средствах и спиртовых растворах. В качестве антисептических средств спирт этиловый применяется в различных концентрациях, и небольшое различие в концентрации оказывает разное бактерицидное действие, поэтому актуальной является разработка чувствительной методики определения содержания спирта этилового в комбинированных антисептических спиртосодержащих средствах и спиртовых растворах. Работа выполнена с использованием физико-химических и статистических методов. Для исследования брали пробы спирта этилового трех концентраций (70%, 72% и 94%). Выполнено три серии опытов. В первой серии определяли содержание спирта этилового хроматографическим методом по разработанной нами методике, во второй и третьей сериях проводили количественное определение этих же проб гидрометрическим и пикнометрическим методами . После чего результаты сравнивались и обрабатывались статистически. Обработка производилась в программе Statistica 6.0. Результаты количественного определения спирта этилового , полученные хроматографическим, пикнометрическим и гидрометрическим методами анализа, являются правильными и не отягощены систематической ошибкой. По воспроизводимости хроматографический, пикнометрический и гидрометрический методы анализа статистически значимо не отличались друг от друга. Разработанная методика анализа хроматографическим методом может быть предложена для определения содержания спирта этилового в комбинированных антисептических спиртосодержащих средствах и спиртовых растворах.
Похожие темы научных работ по химическим наукам , автор научной работы — Адаменко Г. В., Бурак И. И., Колков М. А.
Валидация аналитической методики определения остаточных органических растворителей для стандартизации субстанции 5,7-бис-(мета-нитрофениламино)-4,6-динитробензофуроксана
Оценка показателей точности методики количественного определения компонентов в спиртосодержащей продукции
The aim of this study was to develop sensitive technique for the quantitative determination of ethyl alcohol in combined antiseptic agents containing alcohol and alcohol solutions. As an antiseptic ethyl alcohol is used in various concentrations and a minor difference in its concentrations has a different bactericidal effect, so the development of sensitive method for the determination of ethyl alcohol in combined antiseptic agents containing alcohol and alcohol solutions is urgent. The research was done with the use of physicalchemical and statistical methods. For the study ethyl alcohol samples of three concentrations (70%, 72% and 94%) were taken. Three series of experiments were performed. In the first series ethyl alcohol content was determined by chromatography in accordance with our method, in the second and the third series quantification of the same samples was carried out with the help of hydrometric and pyknometric methods. The results were then compared and processed statistically. Processing was carried out in the program Statistica 6.0. The results of the quantitative determination of ethyl alcohol obtained by chromatographic, pyknometric and hydrometric analysis methods are correct and are not burdened with a systematic error. By the reproducibility chromatographic, pyknometric and hydrometric methods of analysis statistically did not differ significantly from each other. The developed technique of analysis by the chromatographic method can be proposed for the determination of ethyl alcohol content in combined antiseptic agents containing alcohol and alcohol solutions.
ОПРЕДЕЛЕНИЕ СПИРТА ЭТИЛОВОГО МЕТОДОМ ГАЗОЖИДКОСТНОЙ ХРОМАТОГРАФИИ © КОЛЛЕКТИВ АВТОРОВ, 2014
МЕТОДИКА ОПРЕДЕЛЕНИЯ СПИРТА ЭТИЛОВОГО МЕТОДОМ ГАЗОЖИДКОСТНОЙ ХРОМАТОГРАФИИ
АДАМЕНКО Г.В., БУРАК И.И., КОЛКОВ М.А.
Целью данного исследования была разработка чувствительной методики количественного определения спирта этилового в комбинированных антисептических спиртосодержащих средствах и спиртовых растворах.
В качестве антисептических средств спирт этиловый применяется в различных концентрациях, и небольшое различие в концентрации оказывает разное бактерицидное действие, поэтому актуальной является разработка чувствительной методики определения содержания спирта этилового в комбинированных антисептических спиртосодержащих средствах и спиртовых растворах.
Работа выполнена с использованием физико-химических и статистических методов.
Для исследования брали пробы спирта этилового трех концентраций (70%, 72% и 94%). Выполнено три серии опытов. В первой серии определяли содержание спирта этилового хроматографическим методом по разработанной нами методике, во второй и третьей сериях проводили количественное определение этих же проб гидрометрическим и пикнометрическим методами. После чего результаты сравнивались и обрабатывались статистически. Обработка производилась в программе Statistica 6.0.
Результаты количественного определения спирта этилового, полученные хроматографическим, пикнометрическим и гидрометрическим методами анализа, являются правильными и не отягощены систематической ошибкой.
По воспроизводимости хроматографический, пикнометрический и гидрометрический методы анализа статистически значимо не отличались друг от друга.
Разработанная методика анализа хроматографическим методом может быть предложена для определения содержания спирта этилового в комбинированных антисептических спиртосодержащих средствах и спиртовых растворах.
Ключевые слова: спирт этиловый, хроматографический метод, гидрометрический метод, пикнометрический метод.
The aim of this study was to develop sensitive technique for the quantitative determination of ethyl alcohol in combined antiseptic agents containing alcohol and alcohol solutions.
As an antiseptic ethyl alcohol is used in various concentrations and a minor difference in its concentrations has a different bactericidal effect, so the development of sensitive method for the determination of ethyl alcohol in combined antiseptic agents containing alcohol and alcohol solutions is urgent.
The research was done with the use of physical-chemical and statistical methods.
For the study ethyl alcohol samples of three concentrations (70%, 72% and 94%) were taken. Three series of experiments were performed. In the first series ethyl alcohol content was determined by chromatography in accordance with our method, in the second and the third series quantification of the same samples was carried out with the help of hydrometric and pyknometric methods. The results were then compared and processed statistically. Processing was carried out in the program Statistica 6.0.
The results of the quantitative determination of ethyl alcohol obtained by chromatographic, pyknometric and hydrometric analysis methods are correct and are not burdened with a systematic error.
By the reproducibility chromatographic, pyknometric and hydrometric methods of analysis statistically did not differ significantly from each other.
The developed technique of analysis by the chromatographic method can be proposed for the determination of ethyl alcohol content in combined antiseptic agents containing alcohol and alcohol solutions.
Key words: ethyl alcohol, chromatographic method, hydrometric method, pyknometric method. 178
ВЕСТНИК ВГМУ, 2014, ТОМ 13, №4
Среди различных групп химических соединений, обладающих антисептическими свойствами, наибольший интерес представляют алифатические спирты, что связано с их низкой стоимостью, а также широким бактерицидным и бактериостатическим действием на грамположительные и грамотрицательные бактерии, а также на многие виды грибов и вирусов, включая РС-вирусы, вирус гепатита и ВИЧ [1].
Для обработки операционного и инъекционного поля широко применяется спирт этиловый. Спирт этиловый в концентрации 70% оказывает бактерицидное и бактериостатическое действие на грамотрицательные и грамположительные бактерии, некоторые виды грибов. Механизм действия состоит в необратимой коагуляции белков и в мембра-нотропном действии. Спирт этиловый в концентрации 70% рекомендуется к применению в медицине как наружное антисептическое средство [2].
Спирт этиловый синтетический ректификованный применяется в качестве кожного антисептика. Спектр его антимикробного действия - бактерии, вирусы, ВИЧ-инфекции, гепатиты, кандиды 4.
Спирт является естественным антисептиком, имеет высокую скорость уничтожения бактерий и способен быстро испаряться. Кроме того, спирт обладает бактерицидным действием в отношении большинства грампо-ложительных, грамотрицательных и туберкулезных бактерий, а также хорошо действует против некоторых видов грибков и многих вирусов, включая РС-вирусы, вирус гепатита [5].
95% спирт этиловый также является противомикробным средством, при местном применении оказывает антисептическое действие (денатурирует белки микроорганизмов), которое более выражено по сравнению с 7080% спиртовыми растворами. Активен в от-
ношении грамположительных и грамотрица-тельных бактерий и вирусов. При системном назначении обладает способностью вызывать анальгезию и общую анестезию. Является растворителем для некоторых лекарственных средств, а также экстрагентом для ряда веществ, содержащихся в лекарственном растительном сырье. Применяется для консервации биологического материала, в качестве местнораздражающего средства.
Широкое применение получил спирт этиловый 72% в комбинации с бриллиантовым зеленым, йодом кристаллическим, хлоргекси-дином биглюконатом. Увеличение концентрации спирта этилового до 72% увеличивает бактерицидное действие в отношении типовых культур стафилококка, кишечной палочки, синегнойной палочки и кандид.
Изложенное выше позволяет заключить, что в качестве антисептических средств спирт этиловый применяется в различных концентрациях и небольшое различие в концентрации оказывает разное бактерицидное действие, поэтому актуальной является разработка чувствительной методики определения содержания спирта этилового в комбинированных спиртосодержащих средствах и спиртовых растворах.
Для исследования брали пробы спирта этилового трех концентраций (70%, 72% и 94%). Выполнено три серии опытов. В первой серии определяли содержание спирта этилового хроматографическим методом по разработанной нами методике, во второй и третьей сериях проводили валидацию данной методики гидрометрическим и пикнометрическим методами [6]. После чего результаты сравнивались и обрабатывались статистически. Обработка производилась в программе Statistica 6.0.
- 200°С, колонки - 150°С, детектора - 250°С. Газ-носитель - азот, расход - 35 мл/мин, расход воздуха - 300 мл/мин, расход водорода -
ОПРЕДЕЛЕНИЕ СПИРТА ЭТИЛОВОГО МЕТОДОМ ГАЗОЖИДКОСТНОЙ ХРОМАТОГРАФИИ
где: tR - время удерживания вещества, w05 - ширина пика вещества, измеренная на половине высоты, n - число теоретических тарелок. Эффективность колонки составила: по этанолу - 121 теоретических тарелок, по пропанолу - 156 теоретических тарелок. Критерий разделения рассчитывали по формуле:
где Rs - критерий разделения, tR - время удерживания пропанола, сек, tRx - время удер-
живания этанола, сек, wSy и wSx - ширины пиков пропанола и этанола соответственно, сек. Критерий разделения составил 2,15.
Содержание спирта этилового (Х) в препарате в процентах по объему вычисляли по формуле:
где В1 - среднее значение отношений площадей пиков спирта этилового к площадям пиков спирта пропилового (внутреннего стандарта) из хроматограмм испытуемого раствора;
В0 - среднее значение отношений площадей пиков спирта этилового к площадям пиков спирта пропилового (внутреннего стандарта) из хроматограмм раствора РСО спирта этилового;
m0 - масса навески РСО спирта этилового, г;
m1 - масса навески препарата, взятого для анализа, г;
W - объемная доля спирта этилового, используемого для приготовления РСО спирта этилового, %;
р0 - плотность спирта этилового, используемого для приготовления РСО, г/см3;
р1 - плотность препарата, г/см3.
Результаты и обсуждение
Результаты исследования показали, что типичная хроматограмма представляла следующий вид (рис. 1).
трыги Miarntr іСІ іИігЯЄІ Г-ТЙ І^ОМГИ
Рисунок 1 - Хроматограмма этанола и пропанола (внутренний стандарт).
ВЕСТНИК ВГМУ, 2014, ТОМ 13, №4
Испытуемый раствор Стандартный раствор
Площадь пика этанола Площадь пика пропанола Отношение Площадь пика этанола Площадь пика пропанола Отношение
444 377 1,17 327 392 0,83
458 393 1,16 340 403 0,84
479 381 1,25 323 366 0,88
462 362 1,27 328 368 0,89
429 380 1,13 316 400 0,78
Среднее 1,20 Среднее 0,84
547 418 1,30 354 413 0,85
552 394 1,39 374 415 0,90
552 424 1,30 349 411 0,85
562 423 1,32 345 403 0,85
539 419 1,28 365 428 0,85
Среднее 1,32 Среднее 0,86
Испытуемый раствор Стандартный раствор
Площадь пика этанола Площадь пика пропанола Отношение Площадь пика этанола Площадь пика пропанола Отношение
323 397 0,81 340 403 0,84
356 421 0,84 324 368 0,88
347 411 0,84 347 405 0,85
376 441 0,85 367 427 0,86
344 402 0,85 350 408 0,85
Среднее 0,84 Среднее 0,86
343 423 0,81 354 418 0,84
342 418 0,81 368 432 0,85
349 427 0,81 357 418 0,85
301 367 0,82 346 398 0,86
335 409 0,81 340 399 0,85
Среднее 0,81 Среднее 0,85
Величины для расчета: В1 - 1,20, m0 -0,294 г, pj - 0,8154, W - 96,4% (об/об), В0 - 0,84, m1 - 0,439 г, р0 - 0,8058. Подставляя полученные значения в формулу получали величину содержания спирта в пробе, которая составила 92,4% (об/об).
Величины для расчета в параллельном определении: В1 - 1,32, m0 - 0,300 г, р0 - 0,8058. Подставляя полученные значения в формулу получали величину содержания спирта в пробе, которая составила 93,7% (об/об). Среднее
значение двух параллельных определений составило 93,0% (об/об).
Величины для расчета: В1 - 0,84, m0 -0,300 г, pj - 0,8804, W- 96,4% (об/об), В0 - 0,86, m1 - 0,439 г, р0 - 0,8058. Подставляя полученные значения в формулу, получали величину содержания спирта в препарате, которая составила 71,8% (об/об).
Величины для расчета в параллельном определении: В1 - 0,82, m0 - 0,300 г, pj - 0,8804, W - 96,4% (об/об), В0 - 0,86, m1 - 0,433 г, р0 -
ОПРЕДЕЛЕНИЕ СПИРТА ЭТИЛОВОГО МЕТОДОМ ГАЗОЖИДКОСТНОЙ ХРОМАТОГРАФИИ
0,8058. Подставляя полученные значения в формулу, получали величину содержания спирта в препарате, которая составила 69,8% (об/об). Среднее значение двух параллельных определений составило 71,0% (об/об).
Величины для расчета: Bj - 0,79, m0 -0,300 г, Р01 - 0,8856, W - 96,4% (об/об), В0 - 0,85, mj - 0,430 г, р0 - 0,8058. Подставляя полученные значения в формулу, получали величину содержания спирта в препарате, которая составила 68,2% (об/об).
Величины для расчета: Bj - 0,79, m0 -0,300 г, Р1 - 0,8856, W - 96,4% (об/об), В0 - 0,85, mj - 0,433 г, р0 - 0,8058. Подставляя получен-
ные значения в формулу, получали величину содержания спирта в препарате, которая составила 68,5% (об/об). Среднее значение двух параллельных определений составило 68,3% (об/об).
Далее проводили определение спирта этилового в тех же пробах пикнометрическим и гидрометрическим методами. Результаты, полученные пикнометрическим и гидрометрическим методами, приведены в таблицах 4 и 5. Средние результаты, полученные тремя методами анализов, приведены в таблице 6.
После чего результаты сравнивали и обрабатывали статистически, используя параметрический критерий ANOVA. Установлено, что указанные методы статистически значимо не отличались (p Надоели баннеры? Вы всегда можете отключить рекламу.

Если вам нужно быстро и профессионально провести анализ спирта на хроматографе, рекомендуем заказать такие лабораторные исследования в аккредитованной лаборатории, которая создана на базе нашей независимо-экспертной организации
Зачем важно выполнять эти проверки?
- при производстве грубо нарушаются технологии;
- допускаются несоответствия нормативным требованиям (ГОСТы, ТУ, стандарты);
- продукция является контрафактной и реализуется нелегально.
Законодательные требования
- производственного контролирования качества и безопасности изготавливаемой продукции;
- выполнения тестирований и проверок в лабораторных условиях.
- фотометрический;
- хроматографический;
- титриметрический.
Похожие статьи
Бесплатная консультация экспертов
Здравствуйте, подскажите пожалуйста, хотим сделать экспертизу воздуха, у нас курят в доме периодически электронные сигареты,…
Добрый день! Подскажите, пожалуйста, сколько примерно стоит проведение экспертизы запаха на токсичность от мягкой мебели?
Здравствуйте! Можно ли провести анализ образца полиэтиленовой плёнки на содержание формальдегида? Сроки и цена? Так…

В обзоре рассмотрены современное состояние и тенденции развития хроматографических методов анализа этанола, произведенного из пищевого сырья, а также невыдержанных дистиллятов и алкогольной продукции с пищевым этанолом водок и других спиртных напитков из зернового сырья, полученных методом дистилляции. Используемые в настоящее время хроматографические методы, в частности методы газовой и жидкостной хроматографии в тандеме с масс-спектрометрией, позволяют надежно охарактеризовать основные микропримеси этанола различного происхождения. При мониторинге технологии брагоректификации, розлива, хранения, распознавании контрафакта, бракованных партий и фальсификации успешно применяют газовую хроматографию с пламенно-ионизационным детектированием, газохроматографический парофазный анализ, совмещенный с ольфактометрией или химическими сенсорами, пиролитическую и ионную хроматографию, капиллярный электрофорез. Анализ пищевого этанола и дистиллятов, полученных из пищевого сырья методом спиртового брожения крахмалосодержащего и сахаросодержащего сырья, имеет ряд существенных отличий от анализа пивоваренной и винодельческой продукции из-за разного профиля компонентов и микропримесей, содержащихся в них. Питьевой этанол практически не содержит нелетучих компонентов, характерных для пива и вина изопреноидов, моно-, ди- и олигосахаридов, органических кислот, полифенолов, гликонов и агликонов антоцианового типа, витаминов, пептидов и др., но в то же время в нем присутствуют микропримеси летучих компонентов, попавших в конечный продукт из исходного сырья при хранении, транспортировке и др. Главной задачей аналитического контроля этанола, получаемого из пищевого сырья, дистиллятов и водно спиртовых растворов, предназначенных для изготовления алкогольных напитков, является установление их безопасности, т.е. идентификация и определение количественного содержания вредных примесей. Другой задачей, важной для потребителя, является распознавание сорта, контра факта, бракованной и фальсифицированной продукции. Состав и содержание примесей, присущих пищевому этанолу, зависят от большого количества факторов. Технология производства спирта включает в себя следующие процессы: разваривание крахмалистого сырья водой для разрушения клеточной структуры и растворения крахмала, ферментация, во время которой происходит ферментативное расщепление крахмала, брожение, т.е. ферментативное превращение сахаров в спирт, и брагоректификация на разгонных колоннах. Как правило, микропримеси в спирте являются побочными продуктами ферментативного брожения альдегиды, сивушные масла, карбоновые кислоты. Часть примесей образуется в результате вторичных реакций при разваривании зернового сырья альдегиды, метанол, терпеноиды и брагоректификации альдегиды, альдоли, ацетали, кетоны, простые и сложные эфиры, фурфурол и другие кислородсодержащие полифункциональные соединения. Загрязнение спирта также может происходить в процессе транспортировки и хранения готовой продукции: в результате взаимодействия этанола с кислородом воздуха могут появиться примеси альдегидов, кетонов, сложных эфиров и полифункциональных соеди нений, кроме того, некоторые примеси мигрируют из контактирующих со спиртом емкостей. Ряд контаминантов вносится в этанол с некачественным сырьем, технологическими материалами и водой азотистые, сернистые вещества, неорганические соли и др.. Содержание наиболее вредных для здоровья человека примесей в спирте альдегиды, метанол, сивушные масла строго регламентируется ГОСТ , ГОСТ. Обычно фальсификаты, в производстве которых использован технический синтетический или гидролизный этанол, не соответствуют регулируемым нормативам по основным физико-химическим показателям, определяющим критерии безопасности, хотя в некоторых случаях они также могут удовлетворять требованиям ГОСТ и СанПиН для пищевого спирта. Для надежного выявления фальсифицированных спиртных напитков и снижения рисков попадания в торговые сети некачественных и опасных ликероводочных изделий необходимо внедрять в аналитическую практику самые современные методики, позволяющие достоверно определять происхождение этанола.
Химико-токсикологическое исследование крепких алкогольных напитков домашнего изготовления (самогон). Нужный В.П., Савчук С.А., Каюмов Р.И.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследованию подвергали образцы самогона, приобретенного у респондентов в процессе социологического обследования. Все образцы были пронумерованы и имели сопроводительное пояснение, в котором указывались место приобретения, особенности технологии изготовления и др. В общей сложности на анализ представлен 81 образец в стеклянных или пластиковых бутылках емкостью 0,25 л, укупоренных пластмассовыми пробками.
Для сравнения анализировался химический состав промышленных образцов алкогольных напитков, изготовленных методом дистилляции (коньяк, виски, граппа).
Определение содержания алкоголя в образцах осуществляли по плотности растворов с помощью ареометра и алкоголеметрических таблиц.
Газовая хроматография (ГХ-ДИП). Анализ проводили на газовом хроматографе Hewlett-Packard 5890 А с пламенно-иоизационным (ДИП) детектором. Температура узла ввода пробы - 2400 С, детектора - 2200С.
Хромато-масс-спектрометрия (ГХ-МС). Анализ проводили с использованием хромато-масс-спектрометрической системы (Hewlett-Packard, США), включающей масс-селективный детектор HP-5973(MSD) и газовый хроматограф HP-6890. Энергия ионизирующих электронов составляла 70 эВ. Регистрацию сигнала выполняли в режиме полного сканирования в диапазоне 40-440 а.е.м. (скорость сканирования 3 скана в 1 сек). Температура узла ввода 240˚С, соединительной коммуникации к масс-спектрометру 180˚С. Для идентификации определяемых веществ использовали библиотеку масс-спектров NIST98L.
Условия хроматографического разделения (ГХ-ДИП и ГХ-МС). При проведении анализов использовали два варианта хроматографического разделения на капиллярных колонках различной длины.
(Метод 1.) При газохроматографическом (ГХ-ДИП) анализе разделение проводили на кварцевой капиллярной колонке с неподвижной фазой (НФ) НР-FFAP (Free Fatty Acide Phase, эфир полиэтиленгликоля и терефталевой кислоты). Размеры колонки: 25 м x 0,32 мм, толщина пленки НФ 0,52 мкм.
Температурная программа: 45˚С (2мин); 10 С/мин; 190˚С Давление на входе в колонку - 40 КПа. Объем вводимой пробы 0,2 - 0,8 мкл при делении потока 1/10.
(Метод 2.) При ГХ-МС анализе использовали колонку HP-FFAP длиной 50 м, внутренним диаметром 0,20 мм, толщина пленки НФ 0,33 мкм. Температурная программа: 50˚С (2 мин); 10 С/мин; 190˚С (20 мин).
Скорость потока газа-носителя (гелий) составляла 1 мл/мин. Пробу (1 мкл) вводили в режиме с делением потока 1/15.
Внутренний стандарт. В качестве внутреннего стандарта использовали циклогексанол, который добавляли к анализируемым пробам до концентрации 30 мг/л (к 100 мкл пробы добавляли 3 мкл раствора 0,1% циклогексанола в этаноле).
При ГХ-ДИП анализе идентификацию определяемых веществ проводили по времени удерживания индивидуальных компонентов. Для идентификации определяемых веществ были приготовлены модельные смеси (в этаноле), содержащие компоненты спиртных напитков (высшие спирты, эфиры, жирные кислоты, альдегиды, кетоны) и некоторые легкие растворители. При ГХ-МС анализе идентификацию проводили по времени удерживания эталонного компонента и по масс-спектру анализируемого соединения, что особенно актуально в случае хроматографических наложений определяемых веществ.
Были отмечены следующие случаи наложений или неполного разделения хроматографических пиков: 1) диметиловый эфир этиленгликоля/изо-пропиловый спирт/этанол/бензол, 2) этиленгликоль/этилдеканоат/масляная кислота, 3) пропионовая кислота/2,3-бутандиол, 4) метанол/изопропилацетат/метилэтилкетон, 5) этилформиат/метилацетат, 6) октанол-1/бензальдегид.
Количественный анализ проводили с использованием внутреннего стандарта. В качестве внутреннего стандарта выбрали циклогексанол, как компонент, не характерный для спиртных напитков. Предел обнаружения, определенный по циклогексанолу составлял 0,1 мг/л для ГХ-ДИП и 0,05 для ГХ-МС анализа (в режиме полного сканирования).
Метод ГХ-ДИП использовали для предварительного анализа, метод ГХ-МС использовали для подтверждения результатов количественного анализа и контроля правильности идентификации компонентов. При ГХ-МС использовали колонку HP-FFAP с большей разделяющей способностью. Разделяющую способность колонок оценивали экспериментально по полноте разделения пары веществ бензальдегид/октанол-1, обладающих близкими временами удерживания [7, 8].
Оценка токсичности образцов самогона проводилась с помощью экспресс-метода (тест-объект - сперма крупного рогатого скота) и стенда для испытаний спиртов и водок на токсичность [1, 6]. Регистрируемая тест-функция – подвижность сперматозоидов, которая изменяется (снижается или увеличивается) в присутствии токсических агентов. При отклонении величины токсичности испытываемого образца от величины токсичности раствора эталонного этилового спирта за пределы допустимого (нормативного) отклонения образец признается токсичным. Подготовка проб, вносимых в кювету со сперматозоидами, проводилась с учетом содержания этанола в исследуемых образцах самогона. Общее количество подвергнутых анализу образцов – 66.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Химико-токсикологическое исследование крепких алкогольных напитков домашнего изготовления (самогон) из разных регионов России.
Нужный В.П., Савчук С.А., Каюмов Р.И..
Ключевые слова: алкогольные напитки домашнего изготовления, самогон, химический состав алкогольных напитков, токсичность алкогольных напитков.
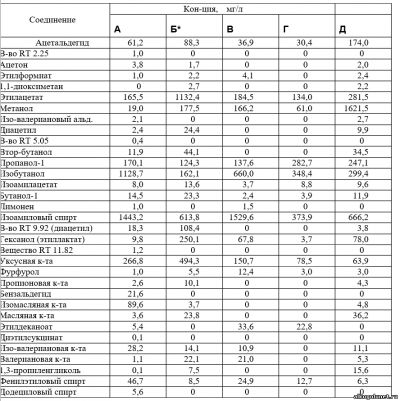
Примечание: * - по органолептическим показателям напиток низкого качества.
Читайте также:

