Хондропротекторы своими руками
Добавил пользователь Владимир З. Обновлено: 17.09.2024
Важнейшее отличие хрящевой ткани от костной, отсутствие внутри хряща нервов, кровеносных сосудов и лимфатических путей.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармацевтического факультета Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Клетки хрящевой ткани — хондроциты (греч. chondros — хрящ, cytus — клетка) не будут делиться, если не произойдет патологических изменений в микроокружении.
Нормальное состояние хондроцитов зависит от "насосного эффекта", связанного с сжатием и растяжением хряща при движениях. Основными компонентами межклеточного вещества соединительной ткани являются минеральные вещества, вода, гиалуроновая кислота, хондроитинсульфаты, протеогликаны. Хондроциты используют глюкозамин как строительный материал для синтеза специфических компонентов хрящевой ткани сустава. При недостатке глюкозамина в составе синовиальной жидкости образуется недостаток хондроитинсульфата, что ухудшает ее качество и может вызвать хруст в суставах.
Универсальным предшественником и строительным материалом хрящевых тканей и всех необходимых суставных смазок является глюкозамин. Глюкозамин восстанавливает ферментативные процессы в клетках суставного хряща, принимает участие в биосинтезе гиалуроновой кислоты, протеогликанов, аминогликанов, гликозаминогликанов. Глюкозамин способствует регенерации суставной сумки и нормализует продукцию внутрисуставной жидкости (густой эластичной массы, заполняющей полость суставов). Глюкозамин восстанавливает хрящевые поверхности суставов и отвечает за эластичность хрящевой ткани. Гликозаминогликаны — высокополимерные линейные биополимеры — образуются путем деполимеризации гиалуроновой кислоты под действием ферментов гиалуронидаз. Гликозаминогликаны в свободном виде не встречаются, они входят в состав межклеточного вещества соединительной ткани и являются обязательными компонентами межклеточного матрикса, играют важную роль в межклеточных взаимодействиях, образуют соединительнотканный матрикс, а также содержатся в костях и синовиальной жидкости. Одна его молекула способна удерживать 200–500 молекул воды, при этом образуются вязкие растворы, с белками образуются муциновые сгустки. Протеогликаны необходимы для общей регенерации хрящевой ткани и выполняют функцию связывания экстрацеллюлярной воды, катионов, отвечают за циркуляцию воды в синовиальной жидкости (ввод и вывод ее обратно), играют роль межтканевых прослоек и служат смазочным материалом в суставах.
Хондроитинсульфат стимулирует синтез протеогликанов и коллагена II типа, выступает как катализатор анаболических и ингибитор катаболических процессов. Хондроитин подавляет активность специфических ферментов (гиалуронидазы, эластазы, лизосомальных) и реакционно-свободных радикалов, вызывающих повреждение и/или разрушение соединительной ткани. Хондроитин способствует отложению кальция в костях, сохраняет воду внутри хряща в виде водных полостей, что создают хорошую амортизацию, поглощает удары и повышает прочность соединительной ткани. Применение хондроитина значительно ускоряет анаболические и сильно замедляет катаболические реакции. Он обладает выраженным анальгезирующим эффектом, снимая боли в суставах при движении и в состоянии покоя.
В нашем организме специфические компоненты ткани сустава вырабатываются в достаточном количестве, но с возрастом их концентрация уменьшается, что приводит к разрушению хрящевой ткани из-за замедления в ней репаративно-регенеративных процессов. Деятельность хондроцитов способствует увеличению массы хряща изнутри (интерстициальный рост) и совместно с хондробластами позволяет регенерировать поврежденные хрящи.
Хондроитинсульфат, глюкозамин, гиалуронат натрия обладают важнейшими физическими свойствами — вязкостью и упругостью, когезионными (сохраняют определенную форму) и обволакивающими качествами. Ускоренный процесс старения снижает образование не только глюкозамина, но и других основных компонентов суставного хряща, уменьшает количество синовиальной жидкости, и суставы теряют свою эластичность, упругость, становятся жесткими, грубыми и хрупкими.
Самыми известными препаратами для восстановления хрящевой ткани являются те, которые имеют в своем составе глюкозамин и хондроитин. При применении препаратов, в состав которых они входят, уменьшаются дегенеративные изменения в суставах и улучшается их подвижность. При их применении нормализуется выработка внутрисуставной жидкости, ускоряется образование костной мозоли и улучшается подвижность суставов. Они обладают противовоспалительной активностью и обезболивающим действием, уменьшается болезненность и увеличивается подвижность пораженных суставов. Восстанавливается структура суставов, эластичность суставных поверхностей и их объем, устраняются боли, связанные с гипермобильностью сустава и остеоартрозом. При совместном применении с НПВС усиливается противовоспалительное действие.
Важно! Хондропротекторы помогают главным образом на ранних стадиях заболевания, когда не утратилась способность к восстановлению и/или в период ремиссии, при ослаблении обострений болезни. Максимальный эффект хондропротекторного действия на ткань хряща развивается очень медленно и от начала лечения может пройти несколько месяцев. Курс лечения необходимо обязательно повторять. При разрушении хряща хондропротекторы неэффективны, таким больным показаны только хирургические методы лечения.
Основные препараты глюкозамин сульфата выпускаются под торговыми наименованиями: Глюкозамин максимум — таблетки, Дона — таблетки и раствор 200 мг/мл — 2 мл для в/м введения, Эльбона — 200 мг/мл — 2 мл раствора в ампулах для в/м введения. Курс применения 6 месяцев с последующими повторами. Препараты обладают противовоспалительным и обезболивающим действием, восполняют эндогенный дефицит глюкозамина, стимулируют синтез протеогликанов и гиалуроновой кислоты, увеличивают проницаемость суставной капсулы, восстанавливают ферментативные процессы в клетках синовиальной мембраны и суставного хряща. Способствуют фиксации серы в процессе синтеза хондроитинсерной кислоты, тормозят развитие дегенеративных процессов в суставах, восстанавливают их функцию, уменьшают суставные боли.
Основные препараты хондроитинсульфата выпускаются под торговыми названиями: Структум, Хондроитин–АКОС — капсулы 250 мг, Хондроксид — таблетки. Хондроитина сульфат натрия (Артра хондроитин) выпускается в капсулах, применяют по 250 мг по 2 капсулы 2 раза в сутки, по 500 мг 2 раза в сутки и 750 мг — по 1 или 2 капсулы в сутки в зависимости от тяжести заболевания. Хороший лечебный эффект достигается при применении препарата не менее 6 месяцев. Период действия препарата после его отмены – 3–5 месяцев. Продолжительность повторных курсов лечения устанавливается врачом индивидуально. Высокомолекулярный мукополисахарид хондроитинсульфат выпускается в виде лиофилизата д/приготовления раствора под ТН Артрадол Эльбона, Хондроитина сульфат, Хондролон, вводится в/м при остеоартрозе периферических суставов и позвоночника. Начальная доза составляет 100 мг и вводится через день. При хорошей переносимости дозу увеличивают до 200 мг, начиная с четвертой инъекции. Курс лечения составляет 25–35 инъекций. При необходимости возможно проведение повторных курсов лечения (через 6 месяцев). Хондроитин улучшает фосфорно–кальциевый обмен в хрящевой ткани, облегчает нормальное отложение кальция в костной ткани, ускоряет процессы ее восстановления, тормозит процессы дегенерации хрящевой и соединительной ткани. Хондроитинсульфаты, обладая структурной схожестью с гепарином, потенциально могут препятствовать образованию фибриновых тромбов в синовиальном и субхондральном микроциркуляторном русле.
Глюкозамин гидрохлорид + хондроитин сульфат натрия (Артра); глюкозамин + хондроитин (Глюкозаминхондроитин комплекс); глюкозамин + хондроитина сульфат + ибупрофен (Терафлекс Адванс); глюкозамин + хондроитин (Терафлекс, КОНДРОнова) — капсулы. Комплексные средства защищают хрящевой матрикс от ферментативного расщепления и повреждающего действия свободных радикалов и предотвращают процессы разрушения хряща. Стимулируют регенерацию хрящевой ткани, поддерживают вязкость синовиальной жидкости. Облегчают симптомы заболевания, проявляя умеренное противовоспалительное действие.
Важно! При применении таблеток, покрытых пленочной оболочкой, могут возникать аллергические реакции, легкие нарушения функции ЖКТ (метеоризм, запор, диарея). Комплексные препараты противопоказаны детям до 15 лет и их не рекомендуется применять беременным и в период лактации!
ПРЕПАРАТЫ МЕСТНОГО ДЕЙСТВИЯ
Глюкозамин (Хондроксид максимум) — крем, хондроитина сульфат (Хондроксид) — мазь, гель, хондроитина сульфат (Хондроитин–АКОС) — 5% мазь.
Глюкозамин + гидролизат коллагена (Коллаген ультра) — гель, крем, глюкозамин 2,5% + хондроитина сульфат 5% (Хондроглюксид) — гель д/наружного применения, глюкозамин + хондроитина сульфат (КОНДРОнова) — мазь, хондроитина сульфат + мелоксикам (Хондроксид форте) — крем и др.
Нанесение 2–3раза в сутки мази или геля тонким слоем на поврежденный участок поражения облегчает симптомы остеоартроза, ослабляет боль, увеличивает подвижность суставов и уменьшает потребность в дополнительном применении противовоспалительных средств. Препараты всегда впитывается быстро и без остатка. Курс лечения обычно составляет от 2 недель до 2 месяцев, при необходимости курс повторяют.
ХОНДРОПРОТЕКТОРЫ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ
Румалон — гликозаминогликан–пептидный комплекс, содержит экстракт хрящей и мозговой ткани молодых животных. Препарат уменьшает активность ферментов, способствующих разрушению хрящевой ткани сустава и восстанавливает подвижность суставов. Выпускается в виде раствора для в/м введения 2,5 мг —1 мл или 2,5 мг и 5 мг —2 мл. Препарат Румалон отпускается по рецепту.
Алфлутоп представляет собой биоактивный концентрат из мелкой морской рыбы. Препарат содержит мукополисахариды, аминокислоты, пептиды, макроэлементы: магний, калий, кальций, железо, медь и цинк. Угнетает активность гиалуронидазы и нормализует биосинтез гиалуроновой кислоты, активирует процессы обмена веществ в тканях хряща. Предотвращает разрушение макромолекулярных структур тканей, восстанавливает интерстициальные ткани и ткани суставного хряща. Выпускается в форме раствора д/инъекций в ампулах по 1 мл, содержащем 100 мкг биоактивного концентрата. Раствор вводят в/м 1 мл в сутки. Курс — 20 инъекций, повторяют через 6 месяцев.
Важно! Препарат противопоказан при беременности и в период лактации.
Артепарон — препарат получен из легких и трахеальных хрящей быков, содержит глюкозоаминогликаны, уроновые кислоты и гексозамин. Выпускается 0,05 г действующих веществ в 1 мл раствора в ампулах. Вводят в/м 1 мл 2 раза в неделю в течение 2 месяцев, далее 2 раза в месяц (4 месяца) 8 инъекций. Внутрисуставное введение 1 мл 2 раза в неделю в течение 3 недель. Курс — 2 раза в год.
ХОНДРОПРОТЕКТОРЫ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ
Артроз — это заболевание суставов, которое носит хронический характер. В суставном хряще происходят дегенеративные изменения, то есть, он постепенно разрушается.
Все начинается с легкого хруста в суставах при сгибании конечностей, на который мало кто обращает внимание. Затем возникает боль при движении. Когда болезнь набирает обороты, то сустав теряет свою подвижность, а боли становятся нестерпимыми. К сожалению, многие оттягивают лечение и обращаются за помощью уже на последних стадиях. Артроз, как и любое другое заболевание, намного лучше поддается лечению на начальном этапе. В этом случае возможно не только снять воспаление и боль, но и полностью восстановить хрящевую ткань.
Для восстановления суставов при артрозе и других заболеваниях опорно-двигательной системы были разработаны специальные препараты – Хондропротекторы. Они не просто уменьшают болевые ощущения, но и способствуют активизации процессов по восстановлению хрящевой ткани суставов, воздействуя на причину изнутри снимая воспаление.
Причины возникновения артроза и его особенности
У этого заболевания есть несколько причин, по которым оно возникает. К ним относятся:
нарушение гормонального фона и обмена веществ;
плохое кровоснабжение суставов;
При артрозе происходит разрушение коллагена и протеогликанов (сложных белков), из которых состоит хрящ. Постепенно он становится менее эластичным, затем начинает трескаться, обнажая кость. Хрящ перестает выполнять свою функцию — амортизацию и равномерное распределение нагрузки во время движения. Обнаженная кость травмируется, в хрящевой ткани появляются костные разрастания. На последних стадиях лечение артроза хондропротекторами, то есть, медикаментами, может быть уже неэффективным, и потребуется оперативное вмешательство.
Статистика показывает, что от артроза страдает от 6 до 12% населения. С каждым десятилетием это заболевание делает инвалидами все больше людей. При этом, женщины страдают от него в два раза чаще, хотя к 65-ти годам разницы уже практически нет. К этому возрасту больше половины людей уже страдают от артроза.
В группу риска попадают не только пожилые, но и профессиональные спортсмены и танцоры. От артроза страдают те, кто имеет проблему искривленного позвоночника, лишнего веса, а также любительницы высоких каблуков.
Хондропротекторы при артрозе
Эта группа препаратов помогает регенерировать тканям хряща, останавливает дегенеративные изменения в его структуре, улучшает подвижность, устраняет болевые ощущения. Помогают хондропротекторы при артрозе коленных, тазобедренных, а также суставов позвоночника, стоп и кистей. Препараты увеличивают количество смазки в них, без которой полноценная работа конечностей просто невозможна.
Действующими веществами хондропротектороы являются хондроитин и глюкозамин, а также гиалуроновая кислота, которая используется для инъекций в суставы. Компонент хондроитин позволяет улучшить обмен веществ в хрящевой ткани, стимулирует выработку коллагена. Клетки начинают активно регенерировать, а синовиальная жидкость ускоренно выделяться. Глюкозамин, который также выходит в состав применяющихся хондропротекторов при артрозе суставов, снимает воспаление, подавляет ферменты, негативно воздействующие на выработку гиалуроновой кислоты и коллагена. Вещества в хондропротекторах могут быть, как животного (лососевые, креветки, моллюски), так и растительного происхождения (бобовые, соя или авокадо).
Все препараты данной группы отличаются накопительным эффектом. Поэтому моментального действия ожидать не стоит. Курс лечения длится довольно долго. Его продолжительность зависит от выбранного препарата, а также степени заболевания, и составляет 3 – 5 месяцев. Через полгода врачи рекомендуют повторить курс лечения, чтобы достичь более стойкого эффекта.
При комплексном подходе, хондропротекторы при артрозе не только эффективно борются с заболеванием, но и положительно влияют и на весь организм в целом. Они улучшают обмен веществ, устраняют спазмы и отечность, выводят шлаки, повышают иммунитет и нормализуют давление.
Лечение артроза хондропротекторами эффективно только в том случае, если в суставе нет серьезных разрушений, которые приводят к необратимым процессам. Если самовосстановление хрящевой ткани невозможно, то следует прибегнуть к хирургическому вмешательству.
Формы выпуска хондропротекторов
Современный фармацевтический ранок предлагает препараты в разных формах выпуска:
в виде гелей и мазей для местного применения;
таблеток, капсул и порошков для перорального применения;
растворов для инъекций, которые вводятся внутримышечно или внутрисуставно.
На второй стадии даже лучшие хондропротекторы при артрозе в таблетках или мазях не дадут желаемого результата. Тут помогут внутримышечные инъекции такими препаратами, как Артрадол. Его основной компонент — хондроитина сульфат, моментально и полностью всасывается в кровь. Препарат относится к лекарствам нового поколения. Он эффективно восстанавливает хрящевую ткань, усиливает выработку суставной жидкости, улучшая подвижность суставов и снимая боль. Курс лечения составляет около месяца, через полгода его повторяют. На данный момент это лучший хондропротектор при артрозе. Пройденный курс лечения подкрепляют приемом таблеток и нанесением мазей.
При запущенном артрозе помогают инъекции, которые вводятся в сам сустав. В них также входят глюкозамин, хондроитин или гиалуроновая кислота.
Классификация хондропротекторов при артрозе
Данные препараты можно классифицировать по давности лечения артроза хондропротекторами в медицинской практике:
первого поколения, которые становятся все менее эффективными;
второго поколения — хондропротекторы при артрозе суставов комплексного воздействия, в которые входит глюкозамин и хондроитин;
третьего поколения — препараты, которые отличаются самой высокой степенью очистки и максимально действенным сочетанием компонентов.
К препаратам новейшего поколения, которые считаются одними из лучших хондропротекторов при артрозе, относится Артрадол.
Противопоказания к применению хондропротекторов при артрозе суставов
Многолетний опыт врачей и фармацевтов показал, что хондропротекторы при артрозе суставов показывают прекрасные результаты и действительно способны облегчить течение болезни или даже полностью устранить проблему. Они достаточно безопасны и эффективны. Но, несмотря на это, как и любые другие препараты, хондропротекторы при артрозе имеют ряд противопоказаний. К ним относятся:
непереносимость одного или нескольких компонентов, которые входят в состав лекарственного средства;
почечная недостаточность в тяжелой форме;
фенилкетонурия (наследственное заболевание), если в составе препарата присутствует аспартам;
плохая свертываемость крови, тромбофлебит;
заболевания пищеварительной системы, если в составе хондропротекторов при артрозе есть НПВС (нестероидные противовоспалительные вещества);
возраст до 15 лет;
Хондропротекторы при артрозе суставов — высокоэффективное лечение и обязательная составляющая комплексной терапии. С их помощью можно победить это сложное заболевание, от которого страдает немалое количество людей, и предотвратить серьезные проблемы со здоровьем в будущем.
Высокая безопасность препаратов позволяет использовать их даже тем, кто страдает от разнообразных тяжелых и хронических заболеваний. Какие хондропротекторы при артрозе подействуют лучше, решает врач. Заниматься самолечением крайне опасно для здоровья. А вот обеспечить достойную профилактику заболевания должен каждый сам для себя. Помните, что благополучие ваших суставов, как и всего организма в целом, зависит только от вас. Относитесь к здоровью внимательно, вовремя обращайтесь к докторам и следуйте их рекомендациям.
При появлении или обострении остеоартроза и симптомов, которыми он сопровождается, возникает логичный вопрос – какому средству отдать предпочтение, чтобы затормозить разрушение суставов, уменьшить дискомфортные ощущения и болевой синдром. Какова разница между средствами, представленными на полках аптек и на что именно обращать внимание в их составе?
Остеоартроз и его лечение
Согласно МКБ-10, заболевание называют остеоартритом. Это поражение преимущественно крупных суставов – чаще всего тазобедренного и коленного. Но это не исключает вовлечения и более мелких суставов, например, в области кисти.
Группа средств, применяемых для борьбы с изменениями в суставах при остеоартрите, называется хондропротекторами. Это компоненты, которые используются как строительный материал для обновления, улучшения структуры хрящевой ткани. Хрящи покрывают поверхности костей, образующих сустав, амортизируя его при движениях и обеспечивая полноценное скольжение движущихся частей. Поражение хряща при остеоартрите ведет к нарушению структуры и функции суставов и появлению симптомов, характерных для заболевания. Прием хондропротекторов помогает затормозить развитие остеоартроза, оказывая влияние не только на симптомы, но и на пусковые механизмы.
Хондропротекторы бывают в разных формах выпуска:
o Раствор для внутримышечных инъекций – рецептурный препарат, который назначается врачом;
o Таблетки или капсулы;
o Гели или мази для наружного применения.
В составе могут быть как одно действующее вещество, так и комбинация: два, три активных компонента.
На сегодняшний день есть три наиболее изученных хондропротектора:
· комплекс NEM ® – хондпропротектор нового поколения;
Рассмотрим подробнее эти вещества.
Комплекс NEM ® для суставов
Комплекс NEM ® является натуральным источником необходимых для суставов веществ – гликозаминогликанов. Они составляют матрикс хрящевой ткани. В составе комплекса содержатся хондроитина сульфат, эластин, гиалуроновая кислота, коллаген. Эти вещества обеспечивают формирование поддерживающего каркаса. Кроме того, комплекс содержит минералы – магний, кальций [8,9].
На протяжении 15-летнего периода изучения эффективности комплекса NEM® в свет вышли 16 экспериментальных и клинических исследований. Они опубликованы в разных странах – Италии, США, Германии, Канаде, Турции [10]. По данным научных работ определено, что NEM ® обладает противовоспалительным [11], иммуномодулирующим [12] действиями, помогает замедлять процессы разрушения [13].
Основные эффекты комплекса NEM ® :
· снижение уровня соединений, которые провоцируют воспалительный процесс [8];
· уменьшение выраженности боли в области суставов, спровоцированной физическими нагрузками;
· снижение интенсивности болевого синдрома, а также скованности на фоне остеоартрита [14];
· улучшение гибкости, подвижности [15];
· торможение, уменьшение выраженности возрастных изменений хрящевой ткани при остеоартрите [16];
Во время изучения комплекса NEM ® был доказан высокий профиль его безопасности [17].
Хондроитина сульфат для суставов
Вещество, которое составляет матрикс хряща, его каркас. Это один из наиболее подробно изученных хондропротекторов. Его прием включен в клинические рекомендации по лечению остеоартрита, разработанные отечественными и европейскими профессиональными ассоциациями 1. Организм использует хондроитин как строительное сырье, необходимое для обновления хряща и восстановления его повреждения. За счет достаточного поступления хондроитина можно поддерживать необходимую вязкость внутрисуставной жидкости, тормозить активность ферментов – гиалуронидазы, эластазы, разрушающих структуру хряща. Плюс ко всему, хондроитин обладает обезболивающим свойством, подавляя концентрацию соединений, провоцирующих воспаление и боль [5,6].
За счет комплексного действия прием хондроитина помогает [5,6]:
· уменьшить интенсивность боли и снизить потребность в обезболивающих;
В средствах для суставов хондроитина сульфат может быть как единственным компонентом, так и сочетаться с другими соединениями.
Глюкозамин для суставов
Естественное соединение, необходимое для производства синовиальной жидкости, особенно таких ее составляющих как протеогликаны и гиалуроновая кислота. Эффективность этого вещества подтверждена в ходе проведения многочисленных исследований.
Глюкозамин помогает [7]:
· уменьшить интенсивность болевых ощущений;
· тормозит активность процессов разрушения в хряще;
· стимулирует синтез полисахаридов, которые присутствуют в составе суставной жидкости в нормальных условиях.
Нередко в составе комплексов комбинируются несколько составляющих: глюкозамин, хондроитин и другие хондропротекторы, что взаимно усиливает их эффект.
Капсулы МУКОСАТ ®*
Все три описанных компонента входят в состав капсул МУКОСАТ ® . Это средство относят к хондропротекторам нового поколения. Состав капсул дополнен экстрактом корня гарпагофитума (его еще называют мартинией душистой) и марганцем.
Экстракт корня гарпагофитума – это изученное специалистами природное противовоспалительное вещество. Его применение помогает снижать выраженность болевых ощущений и улучшать подвижность [18,19].
Марганец для суставов помогает в защите и обновлении хряща, также наш организм использует этот минерал для выработки коллагена [20].
Капсулы МУКОСАТ ® могут применяться как дополнение в комплексной схеме при остеоартрозе и остеохондрозе [21].
Компоненты капсул способствуют [21]:
· уменьшению боли и воспаления;
· защите хрящевой ткани суставов и позвоночника.
Подробную информацию, в том числе схему и режим приема, можно посмотреть в инструкции по применению капсул МУКОСАТ ® .

* БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА. НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ ПРЕПАРАТОМ.
*Содержание комплекса NEM® эксклюзивно только в капсулах Мукосат ®
2. Kloppenburg M, Kroon FP, Blanco FJ, et al2018 update of the EULAR recommendations for the management of hand osteoarthritis Annals of the Rheumatic Diseases 2019;78:16-24.
3. Olivier Bruyère et al. An updated algorithm recommendation for the management of knee osteoarthritis from the European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (ESCEO), Seminars in Arthritis and Rheumatism, Volume 49, Issue 3, 2019, Pages 337-350.
4. Федеральные клинические рекомендации по диагностике и лечению остеоартроза. Ассоциация ревматологов России. 2016
5. Мезенова Т.В. Форсифицированная терапия остеоартрита: расширяя границы возможного. Хирургия. Журнал им. Н.И. Пирогова. 2018;(5): 91-95
8. Наумов А.В., Ховасова Н.О., Ткачева О.Н. Хондропения в авангарде эпидемии остеоартрита: от старения суставов к клиническому манифесту болезни // Лечащий врач, 2018. № 12. С. 69-69.
9. Ruff KJ, DeVore DP, Leu MD and Robinson MA. (2009) Eggshell Membrane: A Possible New Natural Therapeutic For Joint & Connective Tissue Disorders. Results From Two Open-label Human Clinical Studies. Clinical Interventions in Aging, 4:235-240.
10. URL.: stratumnutrition Дата доступа 07.04.2021
12. Ruff KJ. Eggshell membrane hydrolyzates activate NF-κB in vitro: possible implications for in vivo efficacy. J Inflamm Res. 2015.
14. Ruff KJ, Winkler A, Jackson RW, DeVore DP and Ritz BW. (2009) Eggshell Membrane in the Treatment of Pain and Stiffness from Osteoarthritis of the Knee: A Randomized, Multicenter, Double Blind, Placebo Controlled Clinical Study. Clinical Rheumatology, 28:907-914.
15. Brunello E and Masini A. (2016) NEM® Brand Eggshell Membrane Effective in the Treatment of Pain and Stiffness Associated with Osteoarthritis of the Knee in an Italian Study Population. International Journal of Clinical Medicine, 7:169-175
17. Ruff KJ, Endres JR, Clewell AE, Szabo JR and Schauss AG. (2012) Safety evaluation of a natural eggshell membrane-derived product. Food and Chemical Toxicology, 50:604-611.
18. Ribbat J.M., Schakau D. Tratamiento de los dolores crónicos activos en el sistema de locomoción // Natura Med. — 2001. — V. 16, № 3. — P. 23-30.
19. Chrubasik J.E., Roufogalis B.D., Chrubasik S. Evidence of effectiveness of herbal anti-inflammatory drugs in the treatment of painful osteoarthritis and chronic low back pain // Phytother. Res. — 2007. — V. 21. — P. 675-683.
20. Delmas P. D. Treatment of postmenopausal osteoporosis. The Lancet. 2002;359(9322):2018–2026. doi: 10.1016/s0140-6736(02)08827-x
21. Биологическая активная добавка к пище Мукосат® капсулы. Свидетельство о государственной регистрации №RU. 77.99.88.003.Е.001059.03.18 от 15.03.2018 г.
Оценена эффективность нового европейского хондропротектора в комбинированной терапии остеоартроза (ОА) различной локализации I–II стадии. В исследование были включены 358 больных с ОА коленных и тазобедренных суставов, а также полиостеоартрозом. Согласно
Experience of applying a new European chondroprotector in patients with stage 1–2 osteoarthritis in general medical practice T. N. Kargaeva
The effectiveness of the new European chondroprotector in combined therapy in the 1–2 stage of osteoarthritis (OA) of different localization was estimated. The study included 358 patients with knee and hip joint OA, as well as polyosteoartrosis. According to the study, all patients experienced a decrease in the severity of pain, a decrease in need for analgesics, an increase in functional activity and improvement in the quality of life. The drug is well tolerated, and patients demonstrated high adherence to treatment.
ОА является наиболее частым заболеванием суставов. На долю ОА приходится 60–70% всех заболеваний суставов, артрозом болеют 10–20% населения [4]. При этом доля пациентов с ОА неуклонно растет, предполагается, что к 2020 г. ОА станет четвертой причиной инвалидности [5]. ОА представляет серьезную социально-экономическую проблему, так как значительно ухудшает качество жизни больных. ОА является одной из основных причин преждевременной потери трудоспособности, уступая в этом только ишемической болезни сердца.
При ОА происходит нарушение устойчивости суставного хряща к механической нагрузке. Баланс обмена хрящевой ткани смещается в сторону усиления катаболических процессов. Изменения суставного хряща способствуют ухудшению его биомеханических свойств, что отрицательно влияет на подлежащую костную ткань, вызывая нарушение обменных процессов, повышение внутрикостного давления, развитие субхондрального склероза и остеофитоза. С деполимеризацией гиалуроновой кислоты (ГК) связывают ухудшение вязко-эластических свойств синовиальной жидкости при ОА [6].
Согласно современной классификации препаратов, используемых в лечении ОА [7], их подразделяют на следующие группы:
1) симптом-модифицирующие препараты быстрого действия (НПВС, ацетаминофен, опиоидные анальгетики, кортикостероиды, миорелаксанты и др.). Эти препараты купируют основные клинические симптомы, такие как боль и воспаление;
2) структурно-модифицирующие препараты замедленного действия, или хондропротекторы.
Эти препараты обладают хондромодифицирующим действием. Они способны оказывать влияние на воспаление и метаболические процессы в хрящевой ткани и, таким образом, — предупреждать деградацию суставного хряща.
Среди структурно-модифицирующих препаратов, применяемых для лечения ОА, наибольшая доказательная база имеется для хондроитина сульфата (ХС) и глюкозамина сульфата, уровень доказательности 1А [8].
Другим веществом с доказанным хондропротективным действием является ГК. Она играет ряд ключевых ролей в трофике хряща и, улучшая свойства синовиальной жидкости, облегчает скольжение суставных поверхностей [1, 9].
Также известно, что прием коллагена II типа увеличивает подвижность суставов, уменьшает выраженность болевого синдрома у больных остеоартритом [10].
В связи с этим представляется интересным изучить эффективность хондропротекторных препаратов, содержащих в своем составе коллаген II, хондроитин, глюкозамин и ГК при ОА различной локализации на начальных стадиях заболевания. Такой препарат недавно появился на российском фармацевтическом рынке и называется Флексиново.
Флексиново — хондропротектор европейского производства, который содержит комбинацию структурно-модифицирующих компонентов замедленного действия, чья эффективность подтверждена с позиций доказательной медицины. Действующие вещества (мг): гидролизованный коллаген II типа — 300,0; хондроитина сульфат (в том числе 200 мг из акулы) — 240,0; глюкозамина сульфат из ракообразных (D-glucosamine sulfate 2 KCl) — 105,0; L-аскорбиновая кислота (витамин С) — 40,0; гиалуроновая кислота (Nutrihyl) — 24,0; экстракт корня имбиря (Zingiber officinalis) — 10,0.
Задачи исследования
1) Оценить эффективность лечения остеоартроза различной локализации I–II стадии хондропротектором Флексиново.
2) Оценить безопасность и переносимость терапии Флексиново у больных остеоартрозом различной локализации I–II стадии.
Целью данного исследования было изучение возможностей терапии хондропротекторами пациентов, страдающих остеоартрозом различной локализации I–II стадии.
Материал и методы
В исследование были включены 358 больных ОА различной локализации I–II стадии.
Критерии включения:
1) наличие одного из следующих симптомов:
- боль и крепитация в коленных суставах;
- утренняя скованность ≤ 30 мин;
2) наличие болевого синдрома, требующего медикаментозной терапии (40 мм и более по визуальной аналоговой шкале (ВАШ));
3) длительность суставного синдрома не более 10 лет.
Критерии исключения:
- высокая воспалительная активность;
- достоверные признаки иного ревматического заболевания;
- наличие язвы слизистой желудка или двенадцатиперстной кишки в стадии обострения;
- тяжелая сопутствующая патология.
С учетом вышеизложенных критериев в исследование включено 358 пациентов. Из них ОА коленных суставов имели 210 (59%) больных, полиостеоартроз — 97 (27%) больных и ОА тазобедренных суставов — 51 (14%) пациент (рис. 1).
Средний возраст пациентов составил 54,5 ± 2,02 года. Длительность заболевания была в среднем 6,7 ± 1,24 года.
Диагноз ОА устанавливался согласно критериям Альтмана (1991 г.). Для определения рентгенологической стадии артроза использовали классификацию Келлгрена и Лоурсена (1957 г.).
Все 358 больных получили комплексную терапию, включающую cимптом-модифицирующие препараты быстрого действия (парацетамол/НПВС). В качестве cтруктурно-модифицирующего препарата замедленного действия пациенты получали Флексиново по 1 таблетке в день на протяжении 3 месяцев. Эффективность терапии оценивалась по динамике боли в суставах по ВАШ, функциональному индексу тяжести Лекена на протяжении 3 месяцев. Дополнительно оценивалось количество пациентов, полностью отказавшихся от приема обезболивающих препаратов.
Результаты исследования
Начиная с 1-го месяца лечения больные всех трех групп стали отмечать уменьшение боли и других клинических признаков заболевания, но достоверно более значимые изменения показателей наблюдались в 1-й группе.
При анализе полученных результатов лечения в группе больных c ОА коленных суставов, получавших Флексиново по 1 таблетке 1 раз в сутки в течение 3 месяцев, отмечается уменьшение боли при движении по ВАШ к 3-му месяцу наблюдения с 7,44 ± 1,51 до 3,3 ± 0,96. В этой же группе наблюдалось значительное уменьшение боли в покое по ВАШ с 3,44 ± 0,74 до 1,12 ± 0,31. Функциональный индекс Лекена в этой группе пациентов уменьшился с 6, 6 ± 1,19 до 4,35 ± 0,49.
Во 2-й группе больных с полиостеоартозом также отмечалась положительная динамика: уменьшение боли при движении по ВАШ с 7,52 ± 3,7 до 3,7 ± 0,96 к 3-му месяцу наблюдений. В покое боль во 2-й группе уменьшилась с 3,37 ± 0,81 до 1,41 ± 0,54. Функциональный индекс Лекена в этой группе пациентов уменьшился с 6,5 ± 1,36 до 4,5 ± 0,51.
В 3-й группе больных с ОА тазобедренных суставов индекс боли при движении уменьшился с 8,6 ± 1,37 до 4,24 ± 0,98, а индекс боли в покое с 3,44 ± 0,72 до 2,5 ± 0,81 к 3-му месяцу наблюдения. При этом функциональный индекс Лекена также уменьшился с 6,8 ± 1,23 до 5,3 ± 0,81.
Таким образом, во всех трех группах через 3 месяца лечения наблюдалось значительное снижение индекса боли по ВАШ при движении (рис. 2) и в покое (рис. 3).
Индекс Лекена после трех недель приема Флексиново уменьшился во всех трех группах, однако наиболее значимое снижение этого показателя было отмечено в группе ОА коленных суставов (рис. 4).
Флексиново позволил уменьшить или полностью отменить прием традиционных анальгетиков у пациентов всех трех групп.
Через 3 месяца после начала терапии 23% пациентов принимали анальгетики по требованию, а 77% пациентов полностью отказались от приема обезболивающих препаратов (рис. 5).
Препарат переносился хорошо. Пациенты продемонстрировали высокую приверженность к терапии. Побочных эффектов при приеме Флексиново выявлено не было.
Выводы
- Применение Флексиново по 1 таблетке 1 раз в день в течение 3 месяцев в комплексной терапии пациентов с ОА коленных суставов, ОА тазобедренных суставов и полиостеоартозе уменьшает выраженность болей, потребность в обезболивающих препаратах. Повышает функциональную активность и качество жизни больных.
- Флексиново хорошо переносится. Применение Флексиново по 1 таблетке 1 раз в день в течение трех месяцев является безопасным в плане развития побочных эффектов.
Таким образом, полученные данные подтверждают эффективность Флексиново в комплексной терапии ОА крупных суставов и целесообразность его применения в общеврачебной практике.
Литература
- Ревматология: национальное руководство / Под ред. Е. Л. Насонова, В. А. Насоновой. М.: ГЭОТАР-Медиа, 2008. С. 573–588.
- Peat G., McCarney R., Croft P. Knee pain and osteoarthritis in older adults: a review of community burden and current use of primary health care // Ann Rheum Dis. 2001; 60; 91–97.
- Хитров Н. А. Многоликость и коморбидность остеоартроза: пути лечения // Медицинский совет. 2014. № 10. С. 3–6.
- Светлова М. С. Подходы к лечению остеоартроза коленных суставах на ранних стадиях заболевания // Медицинский совет. 2012. № 2. С. 3–9.
- Галушко Е. А., Большакова Т. Ю., Виноградова И. Б. и др. Структура ревматических заболеваний среди взрослого населения России по данным эпидемиологического исследования // Науч.-практич. ревмат. 2009; 1: 11–17.
- Ананьева Л. П. Симптоматическая терапия боли при ревматических заболеваниях // Consilium medicum. 2002. Т. 4. № 8. С. 416–425.
- Чичасова Н. В. Лечение боли у больных остеоартрозом различной локализации // Лечащий Врач. 2014. № 7. С. 2–7.
- Jordan K. M., Arden N. K., Doherty M. EULAR recommendations 2003: an evidence based approach to the management of knee osteoarthritis: report of a task force of the Standing Committee for International Clinical Studies Including Therapeutic Trials (ESCISIT) // Ann Rheum Dis. 2003; 62: 1145–1155.
- Лучихина Л. В. Артроз. Ранняя диагностика и патогенетическая терапия. М.: Медицинская энциклопедия. 2001. 139 с.
- Trentham D. E., Dynesius-Trentham R. A., Orav E. J. et al. Full text of Harvard study effects of oral administration of type II collagen on rheumatoid arthritis // Science. 1993. Vol. 261. P. 1727–1730.
Т. Н. Каргаева, кандидат медицинских наук
ГБУЗ ГП № 218, Москва
Опыт применения нового европейского хондропротектора у пациентов с остеоартрозом 1-2 стадии в общеврачебной практике/ Т. Н. Каргаева
Для цитирования: Лечащий врач № 7/2018; Номера страниц в выпуске: 46-49
Теги: боль, воспаление, заболевания суставов, поражение хряща
Справедливости ради надо заметить, что вертебро-неврологические заболевания – это мультидисциплинарная проблема, решение которой требует участия многих специалистов, таких как нейрофизиологи, неврологи, альгологи, кинезиологи, мануальные терапевты, травматологи-ортопеды. Связано это, в основном, с тем, что дорсопатии являются многофакторными и полиэтиологическими заболеваниями.
В клинической практике врачей-неврологов в настоящее время формируется парадоксальная тенденция: количество методов и способов диагностики болевых расстройств увеличивается ежегодно, но при этом также возрастает терапевтическая резистентность данных расстройств и их распространенность в популяции.
При этом парадоксальной становится ситуация: расходы на лекарственную терапию боли в спине растут быстрее, чем расходы на обращения в отделения экстренной медицинской помощи, ведение стационарных и амбулаторных больных [Altman R., 2009].
Считается, что дорсопатия по характеру вовлечения структур имеет практически всегда следующие компоненты: мышечный – 100%, фасциально-связочный – 75%, суставной – 50% и лишь дискогенный компонент – 2,5% [Иваничев Г.А., 2010].
Большой интерес в понимании причин развития дорсопатий вызывает теория многофакторности развития, согласно которой для данного заболевания необходима генетическая предрасположенность, а для его проявлений – воздействие различных средовых факторов. В настоящее время к наиболее изученным факторам риска возникновения дорсопатий и их неврологических проявлений относят: женский пол, средний возраст, травму позвоночника в анамнезе, наследственность, тяжелые и несбалансированные физические нагрузки, длительное нахождение в вынужденной и нефизиологической позе, монотонную работу, курение, ожирение, неудовлетворенность профессиональной деятельностью и т.д.
Несмотря на все разнообразие факторов, практически во всех теориях развития дорсопатий фигурируют два основных аспекта: декомпенсация в трофических системах и перегрузки позвоночно-двигательных сегментов (ПДС). Локальные перегрузки ПДС возникают под воздействием как экзогенных (перегрузки в быту, на производстве), так и эндогенных (врожденные особенности функционирования мышечно-связочного аппарата) факторов. Все это является еще и предопределяющим условием для разрушающего воздействия на хрящевую ткань, с вовлечением как межпозвонковых дисков, так и межпозвонковых суставов.
Хрящевая ткань представляет собой разновидность соединительной ткани и внешне напоминает гель. Толщина хряща составляет 1–7 мм и зависит от типа сустава и его функциональной нагрузки. Суставной хрящ представляет собой высокоспециализированную хрящевую ткань, покрытую надхрящницей, которая выполняет в организме две важнейшие функции – обеспечивает скольжение суставных поверхностей, а также равномерно распределяет нагрузку при воздействии механических факторов, снижая тем самым травмирующий эффект при движении.
В межпозвоночных дисках, подвижных сочленениях находится волокнистая, или фиброзная, хрящевая ткань. Ее межклеточное вещество содержит параллельно направленные коллагеновые пучки, которые составляют до 97%, постепенно разрыхляющиеся и переходящие в гиалиновый хрящ. Кроме коллагеновых волокон ее межклеточное вещество, или внеклеточный матрикс, состоит из основного вещества, включающего до 70% воды, гиалуроновой кислоты и протеогликанов – около 10–20%. Целостность этой матрицы, соответственно, определяет биомеханические свойства суставного хряща. Структура протеогликана обеспечивает очень высокую гидрофобность, что в сочетании с низкой вязкостью делает его идеальной молекулой для противодействия нагрузке на сустав.
Хрящ не имеет нервных окончаний и сосудов. Его питание осуществляется пассивно из синовиальной жидкости и сосудов подлежащей кости, которая носит название субхондральная кость. Поэтому, по мере старения организма, в хрящевой ткани уменьшаются концентрация протеогликанов и связанная с ними гидрофильность ткани. Ослабляются процессы размножения хондробластов и молодых хондроцитов.
Ряд авторов считают, что дегенеративная болезнь диска и артроз фасеточных суставов являются главными компонентами формирования остеоартроза позвоночника.
У пожилых пациентов (чаще, чем в популяции) боль в спине может быть обусловлена невертеброгенными причинами. Заболевания внутренних органов сопровождаются в ряде случаев отраженной болью в спине. Необходимо дифференцировать с заболеваниями почек и мочевыводящих путей, поджелудочной железы, ретроверсией и опущением матки, объемными и воспалительными процессами в малом тазу и т.д. И в случае возможных данных заболеваний требуется принципиально иное лечение.
Лечение неспецифических болей в спине
Учитывая, что врач часто сталкивается с затруднениями в оценке эффективности и объективизации результатов лечения, начнем с клинических критериев эффективности лечения:
Использование данных рекомендаций позволяет наглядно демонстрировать динамику состояния пациента в процессе лечения, что дает возможность и врачу, и, что немаловажно, пациенту (учитывая психологические аспекты) видеть результаты проведенного лечения. Прежде чем приступать к лечению, необходимо вспомнить нецелесообразные методы:
- чередование приема НПВП, анальгетиков и др.;
- неадекватные комбинации препаратов;
- внутривенное введение анестетиков (новокаин, лидокаин);
- системное введение кортикостероидов;
- одно- или двукратное применение чрескожных лекарственных форм;
- локальное введение сложных комбинаций препаратов.
Пациенту необходимо дать адекватную информацию о заболевании и убедить его в доброкачественности состояния.
В рекомендациях Европейского симпозиума, посвященного проблеме боли в спине, важное место выделено советам по активизации больных в период острой боли (это положение имеет доказательную базу А). В случаях без компрессии корешка постельный режим не должен превышать 48 ч. С точки зрения доказательной медицины ранняя активизация больных в момент периода острой боли дает:
- быстрый регресс боли;
- оптимальные условия для реституции поврежденных тканей (мышц, сухожилий, межостистых связок, диска и др.);
- быстрейшее выздоровление;
- предупреждение инвалидизации.
Постельный режим отрицательно сказывается на результатах терапии.
Двигательный рацион должен расширяться постепенно, в начальный период с ограничением физической активности (поднятие тяжестей, наклоны, длительное сидение и т.д.). Необходимо научить пациента правильно совершать движения. Раннее возвращение к привычному для больного уровню двигательной активности способствует более быстрому купированию боли и предупреждает ее хронизацию. Предикторами хронизации болевого синдрома являются [Valat J. et al., 2000]:
- наличие корешковых нарушений;
- длительное пребывание на постельном режиме;
- избыточные физические нагрузки;
- психосоциальные факторы (эмоциональные): ощущение беспомощности, безвыходности и т.д.
Учитывая мировой опыт, комбинированную анальгетическую терапию боли рекомендуют применять многие официальные медицинские организации, в частности ВОЗ, Американская ассоциация боли, дополняя при этом ее введением хондропротективных препаратов.
Хондропротекторы
Это препараты, обладающие симптом-модифицирующим действием (уменьшают боль и способствуют улучшению функции суставов и позвоночника) и структурно-модифицирующим эффектом (задерживают или приостанавливают прогрессирование дегенеративно-дистрофического процесса). Данная группа препаратов включена в рекомендации российских и зарубежных руководств по лечению остеоартроза и иных дегенеративно-дистрофических заболеваний.
Принимая во внимание родство патогенетических механизмов дегенеративных процессов позвоночника и крупных суставов, в настоящее время в базисную терапию стали все чаще включать препараты, обладающие хондропротективной активностью.
На основании международных критериев выделено несколько химических соединений, используемых для лечения остеоартроза крупных и мелких суставов, в т.ч. позвоночника.
Препараты со структурно-модифицирующими свойствами:
- Глюкозамина сульфат.
- Хондроитина сульфат.
- Комбинированные препараты хондроитин сульфат + глюкозамин.
- Неомыляемые вещества сои и авокадо.
- Биоактивный концентрат из мелкой морской рыбы.
- Препараты гиалуроновой кислоты.
- Стронция ранелат.
- Имбирь (стандартизованный препарат экстракта Zingler officinale и Alpinia galanga).
- Эстрогены.
Наиболее изученными на сегодняшней день являются хондроитина сульфат и глюкозамин.
Хондроитина сульфат – гетерогенная группа соединений, имеющих различную молекулярную массу и удельный вес. Особенностью хондроитина является его способность сохранять воду в толще хряща в виде водных полостей, создающих хорошую амортизацию и поглощающих удары, что в итоге повышает прочность соединительной ткани.
Все группы были стратифицированы по возрастному, гендерному признакам и соматотипам. При формировании групп был применен способ случайного распределения пациентов (рандомизация). Общими критериями включения для всех групп являлись: наличие мышечно-рефлекторных проявлений дорсопатий различных отделов позвоночника, подострый период заболевания.
Общие критерии исключения: наличие органических заболеваний нервной системы, психических заболеваний, травм головного мозга и позвоночника в анамнезе, соматические заболевания в стадии декомпенсации. Дополнительные критерия исключения для группы пациентов: секвестрированные грыжи и грыжи дисков более 8 мм; выраженная гипермобильность, спондилолистезы более 5 мм; наличие деструктивных изменений в телах позвонков.
В исследовании для группы пациентов были использованы диагностические критерии Международной классификации болезней 10-го пересмотра (МКБ-10) (ВОЗ, 1984).
Возрастной диапазон обследуемых варьировал от 35 до 55 лет включительно, что соответствовало второй группе зрелого возраста. По характеру трудовой деятельности больные распределились следующим образом: лица, занимающиеся физическим трудом, – 23,1%, служащие – 76,9%. Анализ занятости больных показал, что гиподинамия, статические нагрузки, позозависимые положения, работа за компьютером, профессиональные и психоэмоциональные перегрузки в последние годы выходят на ведущее место среди причин развития заболеваний позвоночника и мягких тканей.
Разделение пациентов на группы по способу введения хондроитина сульфата (Хондрогард):
- 1-я группа (30 пациентов). Хондрогард был назначен ежедневно по 2,0 мл, с разделением этой дозы на 2 инъекции паравертебрально внутримышечно. Курс лечения продолжался 10 дней. Плюс к этому назначена традиционная фармакотерапия.
- 2-я группа (30 пациентов) получала Хондрогард по 2,0 мл внутримышечно ежедневно на протяжении 10 дней. Дополнительно – традиционная фармакотерапия.
- 3-я группа. Традиционная фармакотерапия.
Все пациенты неоднократно в течение предыдущих лет принимали лечение: амбулаторно, стационарно, а также проходили санаторно-курортное лечение.
Интенсивность болевого синдрома оценивалась по визуальной аналоговой шкале – ВАШ (Association for the Study of Pain, 1986). Количественная оценка миогенного болевого синдрома осуществлялась с помощью балльной оценки по Хабирову.
Оценивались обзорные рентгенограммы отделов позвоночника. Для уточнения патологических изменений костных структур позвоночника и изучения структурных изменений в межпозвонковых дисках, спинном мозге проводилась МРТ.
Методика введения препарата. В первый день для определения чувствительности и переносимости вводилось 100 мг (1 мл) Хондрогарда. Доза распределялась на 2 точки инъекций, расположенные в паравертебральных зонах. В последующие дни препарат вводился в дозе 200 мг (2,0 мл) в 4 точки. Выбор точек введения зависел от локализации болевого синдрома и определялся с помощью исследования вертеброневрологического статуса и пальпации триггерных точек. Пример введения в триггерные точки представлен на рисунке 1.
Рис. 1. Точки введения препарата:1 – шейный отдел; 2 – поясничный отдел; 3 – точки введения КПС
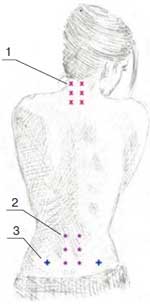
Необходимо отметить, что препарат вводился внутримышечно, что обеспечивало его быстрое распределение в регионарном кровотоке. Как известно, при внутримышечном введении он обнаруживается в крови в значительных концентрациях уже через 30 мин. после инъекции. Максимальная концентрация (Сmах) Хондрогарда в плазме достигается через 1 ч, затем постепенно снижается в течение 2 сут. Однако выбор точек, наиболее приближенных к патогенной зоне, обеспечивает максимальную концентрацию именно в синовиальной жидкости пораженных суставов.
Хондрогард накапливается, главным образом, в хрящевой ткани суставов. Синовиальная оболочка не является препятствием для проникновения препарата в полость сустава.
В экспериментах показано, что через 15 мин. после внутримышечной инъекции хондроитина сульфат обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Сmах достигается через 48 ч.
При введении Хондрогард можно сочетать с анестетиками, например с раствором новокаина 0,25% – 10 мл, что обеспечивает дополнительный обезболивающий эффект. В таком случае дополнительно комплекс препаратов можно вводить в точки максимальной болезненности, которые выявляются у каждого пациента.
Курс терапии Хондрогардом зависит от степени выраженности изменений и может составлять от 10 до 20 паравертебральных внутримышечных инъекций, которые проводятся через день.
Следует отметить, что введение препарата Хондрогард не сопровождалось серьезными нежелательными явлениями. Препарат обладает высоким профилем безопасности, что подчеркивается рекомендациями EULAR, которая рассматривает хондроитина сульфат в качестве одного из самых безопасных лекарственных препаратов терапии остеоартроза. Местные побочные явления (небольшие гематомы в месте введения препарата, болезненные уплотнения в месте инъекции, чувство жара после инъекции) возникали редко и никогда не приводили к отказу пациента от продолжения лечения.
Результаты
Все пациенты хорошо переносили терапию. Из побочных явлений были выявлены только геморрагии в месте инъекций у 3 пациентов.
- В первой группе в среднем к 3–4 сут. пациенты отметили уменьшение болей по ходу позвоночника, а также скованности по утрам.
- К 9–10-м суткам пациенты этих групп отметили увеличение подвижности пораженных суставов и позвоночника, а также уменьшение крепитации при движении.
- Во второй группе эффект от проводимой терапии пациенты стали отмечать к 6–7-му дню лечения.
- На 10-й день все пациенты отмечали также значительное уменьшение боли, утренней скованности и увеличение подвижности.
- В третьей группе пациенты также отметили улучшение состояния, пройдя десятидневный курс традиционной фармакотерапии, но уменьшение болевого синдрома отмечали лишь на 9-й день, при этом сохранялась утренняя скованность и лишь незначительное увеличение объема движений в позвоночнике.
Выводы
Хондроитина сульфат (Хондрогард) целесообразно вводить паравертебрально и (или) локально возле крупного сустава (внутримышечно), что позволяет быстрее и эффективнее достигать его максимальных концентраций в региональном кровотоке пораженных участков опорно-двигательного аппарата, а это приводит к укорочению сроков нетрудоспособности и повышению эффективности лечения.
Читайте также:

