Как сделать укол онкобольному
Обновлено: 06.07.2024
Онкологические заболевания могут вызывать боль. Она значительно снижает качество жизни и терпеть ее не нужно. Тем более, что в арсенале врачей есть разные виды обезболивающих препаратов. Но на практике часто оказывается, что доступ к обезболиванию ограничен.
Причины боли
Откуда возникает боль при онкологическом заболевании? Часто причина боли — сама опухоль. Она может поражать кости, мягкие ткани, кожу, внутренние органы, сдавливать магистральные сосуды и нервы, вызывать кишечную непроходимость, нарушать отток желчи и мочи.
Например, при канцероматозе брюшины (опухолевые узлы на брюшине — прим. авт.) поражается тонкий слой клеток, который покрывает все органы брюшной полости. Брюшина очень чувствительный орган, и люди с канцероматозом всегда испытывают боль. Многие онкологические пациенты мало двигаются, что приводит к трофическим язвам и пролежням, которые тоже вызывают боль. Еще боль может быть связана с проводимым лечением — операцией, химио- или лучевой терапией, — поясняет Сергей Савчук.
 |
У каждого своя
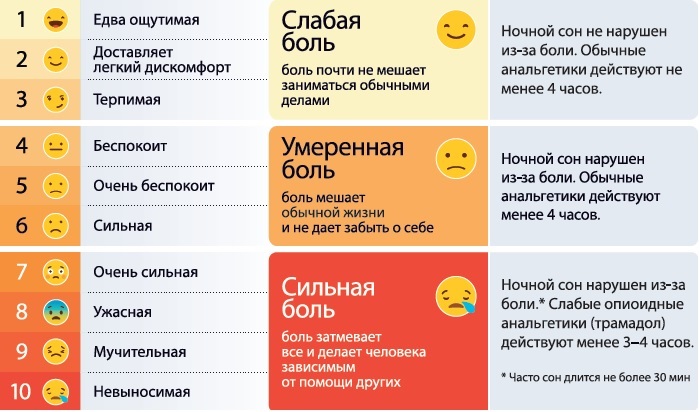
Боль, как любое ощущение, субъективна. То есть интенсивность боли может измерить только тот, кто ее чувствует. Для оценки боли есть специальные шкалы. На приеме врач может попросить пациента оценить свою боль по 10-балльной шкале, где 0 — полное отсутствие боли, а 10 — максимально возможная боль, которую человек не может терпеть.
В соответствии с этой шкалой работает лестница обезболивания. Если боль от 1 до 3, то нужно использовать нестероидные противовоспалительные средства (НПВС), например, ибупрофен. Если до 7, то сильнодействующие препараты — слабые опиоидные анальгетики (трамадол). Препараты выбора при боли выше 7 — наркотические анальгетики (морфин). Сильнодействующие и наркотические обезболивающие пациент может получить только по рецепту, — поясняет Алексей Ильюхов.
Алексей работает специалистом по паллиативной медицине, большая часть его деятельности связана с подбором обезболивания для пациентов с онкологическими заболеваниями.
 |
Всемирная организация здравоохранения рекомендует при назначении обезболивающих придерживаться следующих принципов:
Орально — предпочтение обезболивающим в форме таблеток.
По часам — препарат нужно принимать через фиксированные промежутки времени, не дожидаясь, когда возникнет боль.
Индивидуально — врач подбирает обезболивание с учетом особенностей организма пациента и сопутствующих заболеваний.
С вниманием к деталям — врач должен предупредить пациента обо всех возможных побочных эффектах и о том, как их можно предотвратить.
На практике эти принципы почти не соблюдаются. И пациентам с онкологическими заболеваниями часто очень сложно получить адекватное обезболивание.
Один на один
У отца Светланы из Красноярска рак желудка. После отказа в лечении из-за перенесенного инсульта и сопутствующих заболеваний его направили в поликлинику по месту жительства — мужчина нуждался в обезболивании.
Участковый терапевт назначила НПВС в уколах, довольно быстро средство перестало помогать. Врач выписала рецепт на Трамадол — ни о каком подборе дозы и речи не было. Не предупредили о возможных побочных эффектах. Начались запоры. Папа очень страдал и слег. Вмешалась пандемия, врача вызвать домой стало практически невозможно, без осмотра по телефону выписывали рецепты и оставляли в регистратуре поликлиники. Мы сказали, что состояние стало хуже, смогла прийти участковый врач, и хотя папа ей сказал, что оценивает боль на 3 (он тогда больше от запора страдал), нам выписали наркотическое обезболивающее тоже без плавного перехода сразу три раза в день, — рассказывает Светлана.
По словам женщины, все проблемы случились из-за невозможности найти общий язык с врачом:
Терапевт придерживалась своей схемы, не слышала нас, вернее, не хотела слышать. Назначение всегда было одно для любого препарата — три раза в день, хотя в аннотации к препарату написано — два раза в день, через 12 часов. Дозы сразу были большие. В 21 веке в городе-миллионнике, краевом центре, мы остались один на один со своими проблемами, как будто живем в глухой деревне со стареньким фельдшером, — сетует Светлана.
Путь получения рецепта на обезболивающие очень тернист. Часто пациента сначала направляют к онкологу в районную поликлинику. Онколог осматривает человека и выдает консультативное заключение. В нем должно быть указано, что у пациента болевой синдром или что он нуждается в адекватном обезболивании. Дальше врач-онколог отправляет пациента к участковому терапевту за рецептом. Терапевт выписывает рецептурный бланк, и пациент едет в специальную аптеку, где по рецепту получает лекарство.
Зачастую этот путь занимает много времени, потому что на любом из этапов что-то может пойти не так. Во-первых, к онкологу довольно сложно попасть с улицы — нужна запись или направление. Может так получиться, что поликлиника, где есть онколог, не совпадает с адресом регистрации пациента, и ему приходится ехать в поликлинику по месту жительства, чтобы попасть к участковому терапевту. Терапевты очень неохотно идут на то, чтобы выписать рецепт человеку, не относящемуся к его участку, — объясняет Сергей Савчук.
Однако Анна Повалихина уточняет, что такой долгий путь необязателен — терапевт может выписать рецепт самостоятельно или по согласованию с врачебной комиссией. Такое согласование необходимо, если пациент получает наркотические или психотропные препараты первый раз, и проводится, только если это установлено приказом главврача конкретной медицинской организации.
Алексей Ильюхов приводит другие примеры трудностей:
Терапевт может сказать: “Ой, я столько не выпишу”. Или: “Ой, вы знаете, у нас в поликлинике принято, чтобы на рецепте еще руководитель расписался, но его сейчас нет. Приходите завтра”.
Следующая на очереди аптека. Рецепт идет в определенную аптеку — не все работают с наркотическими анальгетиками.
Человек приезжает за лекарством в аптеку и запросто может столкнуться с ситуацией, когда этого препарата в аптеке нет. Или есть, но немного другой, например, в другой дозировке. Тогда ему препарат не выдают. Он разворачивается, едет ко мне назад, и я выписываю ему новый рецепт. И пациент опять едет в аптеку. А она уже закрылась. На практике мы звоним сначала в аптеку, находим нужный препарат, бронируем его и информацию об аптеке даем пациенту, — перечисляет Алексей Ильюхов.
Врач-терапевт, которая лечит папу Светланы, несколько раз делала ошибки, выписывая рецепт. Мама Светланы ехала в аптеку за лекарством, а потом назад в поликлинику — переписывать рецепт.
Часто проблемы возникают у тех пациентов, которые не могут передвигаться и прийти в поликлинику на очный прием.
Терапевт, вызванный на дом, может сказать, что не в его компетенции — определять, нуждается ли онкопациент в обезболивании. Онкологи домой приходят крайне редко — в амбулаторном звене их мало, они физически не успевают ходить по вызовам. Я во всех выписках пишу, что пациент должен быть обеспечен адекватным обезболиванием, даже если пока оно ему не нужно. Это должно сократить путь получения обезболивания в случае необходимости на один шаг, — комментирует Сергей Савчук.
Законный драгдилер
Откуда возникают эти трудности? По словам Анны Повалихиной, одна из причин — нормативная зарегулированность: оборот наркотических лекарственных препаратов регламентируется несколькими федеральными законами, многочисленными постановлениями Правительства РФ и приказами федеральных органов исполнительной власти. Медицинским и фармацевтическим работникам непросто самостоятельно разобраться, как применять на практике этот массив нормативных правовых актов.
Алексей Ильюхов видит эту причину иначе:
Врачи боятся выписывать наркотики. Самое главное, что влияет на ситуацию с обезболиванием — государство смотрит на себя, как на карательный орган, который должен меня, врача, постоянно проверять и ущучивать. Я условно законный драгдилер, и за мной нужно следить, а еще лучше — отнять у меня препараты, чтобы наркоман (пациент) наркотики не получил ни в каком виде. Количество вводных таково, что выписывая наркотические обезболивающие, ты что-то скорее всего нарушишь. Живешь в ощущении, что за тобой в любой момент могут прийти.
 |
Мы решили получить второе мнение, и нам порекомендовали другой наркотический анальгетик. При этом рецепт на первый наркотик мы уже успели получить. Когда мы попросили выписать новое лекарство, то выслушали угрозы, что к нам и в поликлинику придет наркоконтроль: “Пейте то, что вам выписали”. Правда, в итоге новый рецепт нам все же написали. Эти таблетки очень подошли папе.
По словам Алексея, мешают работе и мифы в головах коллег-врачей:
Некоторые, например, считают, что наркотики нужны только в самом крайнем случае, потому что зависимость сразу, и вообще от них умирают быстрее, поэтому людей, как правило, недообезболивают, предлагают потерпеть. Еще огромная проблема — мы не умеем небольно обезболивать. Трамадол в ряде учреждений, в том числе в детских стационарах будут колоть в мышцу. Стандартная доза 5 мл — это много и больно. А можно сделать укол в вену или дать таблетку. Если речь идет о ребенке, то он будет до последнего терпеть и не говорить, где болит, чтобы ему не сделали еще больнее.
Незначительные изменения
По словам Анны Повалихиной, в последние годы требования, касающиеся обезболивания наркотическими средствами, упростились. В частности:
— не нужно больше возвращать упаковки (ампулы, флаконы) от использованных в медицинских целях наркотических и психотропных лекарственных препаратов.
— срок действия рецепта на наркотические и психотропные лекарственные препараты увеличился с 10 до 15 дней.
— закреплены назначение и выписка наркотических и психотропных лекарственных препаратов не только пациентам с выраженным болевым синдромом, но и с нарушением сна, судорожными состояниями, тревожными расстройствами, фобиями, психомоторным возбуждением.
— увеличено предельно допустимое количество отдельных наркотических и психотропных лекарственных препаратов для одного рецепта.
 |
Но Алексей говорит, что изменения не очень значительные:
Самые строжайшие расстрельные рецепты (на наркотические обезболивающие — прим. ред.) онкологическим пациентам стали выдавать не онкологи, а терапевты районных поликлиник. Упрощаются требования к оформлению рецепта. Однако тут есть ловушка: рецепт принимает аптека, но “дама в окошке” может не знать последних введений. Нам разрешили хранить эти рецепты не в сейфе — небольшой запас мы можем хранить в запирающемся ящике. Насколько это сделало легче нашу жизнь?
Обещают сделать электронные рецепты по примеру больничных листов. Это хорошо, но не уверен, что эта штука сразу заработает с наркотическими анальгетиками — куда девать завод, который делает эти рецепты, и что делать с кладовщиками, которые хранят запас рецептов?
Куда обращаться пациенту, если отказывают в обезболивании или текущее обезболивание не убирает болевой синдром?
На какие законодательные инициативы можно опираться, чтобы отстаивать свои права?
Анна Повалихина выделяет основные:
Для пациентов, нуждающихся в паллиативной помощи, назначение обезболивающих лекарственных препаратов, в том числе наркотических, закреплено пунктом 24 Положения об организации оказания паллиативной помощи, утвержденного Приказами Министерства здравоохранения РФ и Министерства труда и социальной защиты РФ от 31 мая 2019 г. N 345н/372н.
Что делать медикам, если они хотят разобраться в тонкостях назначения наркотических препаратов?
Очень хороший месяц
С новой схемой обезболивания наш дорогой больной прожил очень хороший месяц: встал с постели, гулял, даже на даче побывать успел. К сожалению, сейчас ситуация ухудшилась. Но мы понимаем, что болезнь прогрессирует и ухудшения неизбежны, — заключает Светлана.

Родственники, социальные работники или любые другие доверенные лица (например, друзья).
- Перед выпиской рецепта на НС первично ли, повторно ли врач обязан осмотреть пациента. Соответственно, больной может и в устной форме сказать врачу, кто будет получать за него в поликлинике рецепт и лекарственный препарат в аптеке.
- Согласно законодательству, при первичном оформлении получения НС в поликлинике или при замене кандидатуры, получающего лекарственный препарат, на получающего в поликлинике заполняется форма, где отражены паспортные данные получающего, адрес проживания, степень родства по отношению к пациенту. Эта форма подклеивается в карточку. В г. Москве это Приложение 22 к Приказу №1077 от 11.12.2015 г.
- Доверенному лицу обязательно иметь при себе СВОЙ паспорт и копию паспорта пациента.
- Желательно (но не обязательно!), чтобы у доверенного лица было на руках заявление на получение наркотических обезболивающих от пациента.
- Соцработник по закону имеет право отказаться от получения сильнодействующих препаратов для больного.
Как получить обезболивающие при выписке из стационара или хосписа
При выписке пациента медработники обязаны:
- При наличии у медучреждения лицензии на работу с наркотическими и психотропными веществами выдать пациенту препарат на срок до пяти дней из запасов стационара, либо выписать рецепт для получения обезболивающего лекарства в аптеке, к которой прикреплена медицинская организация.
- При отсутствии соответствующей лицензии медработники обязаны связаться с поликлиникой по месту жительства пациента и сообщить руководству территориальной поликлиники для принятия решения об обеспечении пациента с хроническим болевым синдромом НС и проведения дальнейшего планового обезболивания в установленном порядке.
Действия сотрудников скорой помощи при обезболивании онкобольных
- Если по каким-либо причинам пациент не может самостоятельно провести обезболивание, это обязана сделать бригада скорой помощи, используя средства пациента.
- Если боль не снимается ненаркотическими препаратами, используются наркотические средства бригады скорой помощи (в рамках оказания скорой медицинской помощи в неотложной форме). В каждой бригаде такие средства есть.
- Скорая делает запись о проведении обезболивания в карте вызовов, заведующий подстанцией информирует руководство территориальной поликлиники для принятия решения об обеспечении пациента наркотическим средством и проведения дальнейшего планового обезболивания в установленном порядке.
Что делать, если возникли трудности с назначением обезболивающего
В случае затруднений при получении рецепта на наркотическое обезболивающее по месту жительства следует обратиться за помощью по телефонам горячих линий Минздрава и Росздравнадзора.
- Горячая линия Минздрава РФ: 8 800 200 03 89
- Горячая линия Росздравнадзора по обезболиванию: 8 800 550 99 03
- Горячая линия по вопросам оказания паллиативной помощи: 8 800 700 84 36
Телефоны в Москве:
- Единая справочная служба города Москвы (в том числе по вопросам доступности и качества бесплатной медицинской помощи): 8 495 777 77 77
- Дирекция по координации деятельности медицинских организаций города Москвы: 8 495 318 00 11
- Дирекция по обеспечению деятельности государственных учреждений здравоохранения Троицкого и Новомосковского административных округов (ТиНАО): 8 499 347 06 16
Мы составили небольшую памятку с последовательностью действий для пациента с болью, её можно посмотреть, скачать и распечатать.


Рис. 1 | Принципы ВОЗ по применению анальгетиков для обезболивания при раке: a) согласно уровню боли b) перорально с) по часам d) индивидуальный подход и е) внимание к деталям. (ВОЗ 1986)
Острая онкологическая боль
- Ассоциированная с опухолью: патологический перелом, обструкция или перфорация полого органа, перфорация верхней полой вены.
- Ассоциированная с противоопухолевой терапией: мукозит, головная боль, ладонно-подошвенный синдром, миалгия и артралгия.
- Ассоциированная с радиотерапией: мукозит, боль в костях, нейропатия.
- Острая послеоперационная боль.
Хроническая онкологическая боль
- Ассоциированная с опухолью:
- боль в костях — метастазы, инфильтрация в костный мозг;
- боль в мягких тканях — головная боль, лицевая боль, плевральная боль;
- висцеральная боль — увеличение печени, хроническая кишечная непроходимость, боль в промежности.
- Невралгия черепных нервов: глоссофарингеальная невралгия, невралгия тройничного нерва.
- Плексопатии: плечевая, пояснично-крестцовая и шейная.
- Радикулопатии: пояснично-крестцовая, шейная и грудная.
- Нейропатия: паранеопластическая сенсорная нейропатия.
- Боль, ассоциированная с химиотерапией: аваскулярный некроз, компрессионные переломы позвонков, периферическая нейропатия.
- Хирургическая боль: лимфедема, постторакотомическая боль, фантомная боль после ампутации, постмастэктомическая боль.
- Боль, ассоциированная с радиотерапией: цистит, энтерит или проктит, остеорадионекроз и переломы; болезненные вторичные злокачественные новообразования, плечевая и пояснично-крестцовая плексопатии.
- Боль, ассоциированная с гормональной терапией: артралгии, миалгии, диспареуния, гинекомастия, остеопоротические компрессионные переломы.
Опиоиды связываются с опиоидными рецепторами ноцицептивного пути, чтобы уменьшить передачу импульсов и восприятие боли в соматосенсорной коре. Препараты опиоидов включают морфин, оксикодон, гидрокодон, трамадол, гидроморфон, оксиморфон, фентанил, бупренорфин и метадон [2].
Морфий. Считается препаратом номер один при боли, связанной с онкопатологией, главным образом потому, что он является относительно более распространенным и доступным, но не более эффективным, чем другие опиоиды [3].
Метадон. Использование и титрование метадона является сложной задачей и должно осуществляться профессионалами с высоким уровнем знаний, например, специалистами в области паллиативной помощи и обезболивания [3].
Бупренорфин. Были высказаны опасения по поводу эффективности бупренорфина из-за его частичной агонистической активности, что может приводить к снижению обезболивающего эффекта и увеличивать вероятность побочных эффектов при более высоких дозах. Некоторые исследования показали, что этот препарат безопасен и эффективен при лечении хронической боли, связанной с раком [4], и предложили его в качестве альтернативы морфину, оксикодону и фентанилу [5]. Препараты бупренорфина для парентерального применения, а также низкодозированные трансдермальные препараты бупренорфина одобрены для лечения хронической боли онкологического генеза средней и тяжелой степени [6].
Пациентам необходимо иметь доступ как к опиоидам замедленного высвобождения, так и к лекарствам немедленного действия для купирования эпизодов острой сильной боли. Препаратами выбора обычно являются таблетированные формы с пролонгированным высвобождением в связи с возможностью назначения пациентам более низких дозировок, более длительным анальгетическим эффектом и меньшим влиянием на сон по сравнению с препаратами немедленного высвобождения, однако их стоимость может ограничивать возможности пациентов по их приобретению [3].
Также опиоиды с разной скоростью высвобождения действующего вещества имеют различные побочные эффекты. Препараты с немедленным высвобождением сильнее действуют на лимбическую систему, быстрее вызывают эйфорию, чем препараты с пролонгированным высвобождением. Опиоидные анальгетики пролонгированного действия могут быть рассмотрены для лечения пациентов с хронической онкологической болью, в том числе с немедицинским использованием опиоидов в анамнезе [2].
Трансдермальный путь введения препаратов (фентанил, бупренорфин) используется у пациентов, которые не способны принимать лекарственные средства внутрь. Подкожный путь применяется у пациентов, которые не могут получать опиоиды пероральным или трансдермальным путем. Внутривенный способ введения следует учитывать при необходимости титрования опиоидов или с целью быстрого обезболивания. Введение опиоидов ректально также может быть эффективно, но ограничивается доступностью соответствующих препаратов и желанием пациента [3].
Ингаляционные опиоиды и опиоиды для внутривенного введения попадают в кровоток и проникают через гематоэнцефалический барьер быстрее. Было доказано, что применение лекарств путем ингаляций и внутривенных инъекций ассоциировано с увеличением риска возникновения расстройств, связанных с употреблением психоактивных веществ, и передозировки [11].
Клиницистам следует выбирать минимальную эффективную дозу опиоида, которая будет вызывать желаемую анальгезию с незначительными или отсутствующими побочными эффектами. Многочисленные исследования показали, что назначения высоких доз опиоидов (обычно > 100 мг в день) связаны с повышенным риском злоупотребления [12] и/или передозировки у пациентов как с хронической онкологической болью, так и с другими видами хронического болевого синдрома [13]. В рекомендациях Центра по контролю и профилактике заболеваний США по части лечения неонкологической боли сказано, что врачи должны избегать применения дозировок > 90 мг в день [9]. Однако дозовые и временные пределы не всегда подходят для пациентов с хронической онкологической болью, которым часто требуются повышенные дозы в течение длительных периодов времени [2].
К побочным эффектам опиоидов относятся запоры, тошнота и рвота, зуд, седация, опиоидная нейротоксичность и угнетение дыхания. Побочные эффекты, связанные с опиоидами, можно контролировать путем уменьшения дозы, применения опиоидов другой группы, изменения пути введения или симптоматического устранения побочных эффектов. Одновременное использование антигистаминных препаратов, анксиолитиков или габапентиноидов для лечения симптомов, сопутствующих боли, может усиливать опиоидную токсичность [2].
Адъювантные анальгетики, включая противосудорожные средства, такие как амитриптилин и габапентин, считаются особенно эффективными при нейропатической боли, но их необходимо тщательно подбирать для предотвращения усиления побочных эффектов со стороны центральной нервной системы при одновременном применении с опиоидами. Габапентин при нейропатической боли стоит использовать с осторожностью: необходимы дополнительные исследования для оценки эффективности и безопасности этого препарата. НПВС и ацетаминофен могут использоваться в качестве опиоид-сберегающих средств при боли в костях при отсутствии противопоказаний [2].
Пациенты подвергаются повышенному риску передозировки опиоидами в ранний период начала опиоидной терапии или позже — вследствие развития толерантности к опиоидам. Пациенты с эпизодами немедицинского использования опиоидов и психическими расстройствами, связанными с употреблением психоактивных веществ в анамнезе, чрезвычайно уязвимы в плане развития передозировки данными препаратами после периода воздержания: при сохранении постоянного желания употребления опиоидов, они утрачивают чувствительность к ним, которая ранее препятствовала седации и угнетению дыхания. Потеря толерантности к опиоидам обычно происходит в течение нескольких дней после прекращения приема препарата, в то время как тяга, связанная с немедицинским применением опиоидов и расстройствами, связанными с употреблением психоактивных веществ, может сохраняться месяцы и годы [10].
Большинство руководств по назначению опиоидов [9,14,15] поощряют оптимизированное использование неопиоидных и адъювантных анальгетиков [3,14,15].
Назначение налоксона
Налоксон — опиоидный антагонист короткого действия, используемый как антидот при передозировке опиоидами, помогающий снизить риск угнетения дыхания; может быть полезен для пациентов с риском эпизодов немедицинского использования опиоидов [2].
Механизм
Ноцицептивная информация о повреждении периферических тканей передается через афферентное нервное волокно к дорсальному рогу спинного мозга, где он образует синапс со вторым нейроном и далее позволяет импульсу перемещаться вверх по спинному мозгу. Затем нейрон второго порядка образует синапс с нейроном третьего порядка в таламусе, который, наконец, отправляет информацию в соматосенсорную кору, что приводит к восприятию интенсивности боли [7]. В дополнение к этому основному спиноталамическому пути ноцицептивный импульс также передается по другим путям, что приводит к возбуждению и/или нарушению сна, отрицательным эмоциям, связанными с наличием боли и планированием лечения [8] (Рис. 2).

В процессе восприятия боли и связанных с ней эффектов задействовано четыре общих неврологических пути. Опухолевая ткань и воспаление стимулируют ноцицепторы в периферической ткани, генерируя ноцицептивный импульс. Этот импульс затем передается через афферентные нервы к дорсальному рогу спинного мозга. Импульс обычно следует по основному пути вдоль спиноталамического тракта и проецируется в соматосенсорную кору, что приводит к восприятию интенсивности и выраженности боли. Импульс может также передаваться по путям лимбической системы, что приводит к негативным эмоциям, связанным с наличием боли. Передача по пути ретикулярной активирующей системы приводит к возбуждению и нарушению сна, а передача по префронтальному пути к коре приводит к тревожности и озабоченности.
Экспрессия μ-опиоидных рецепторов обнаруживается во всей нервной системе, включая периферию, спинной мозг, таламус, соматосенсорную кору, средний мозг и лимбическую систему, и опиоиды связываются с любым μ-опиоидным рецептором, который они обнаруживают. Стимуляция μ-опиоидного рецептора в вентральной области покрышки среднего мозга и прилежащего ядра в вентральном стриатуме приводит к выделению дофамина, опиоидных пептидов и серотонина (Рис. 3) [8].

Рис. 3 | Концептуальная модель эффектов воздействия опиоидов на ноцицептивные и неноцицептивные пути.
Опиоиды стимулируют μ-опиоидные рецепторы (MOR) в ноцицептивном пути, что приводит к быстрому снижению передачи ноцицептивного импульса при боли. Со временем медленное высвобождение возбуждающих аминокислот приводит к развитию толерантности и гипералгезии. Стимуляция MOR в лимбическом пути приводит к быстрому высвобождению нейротрансмиттеров (включая дофамин, опиоидные пептиды и серотонин), которые вызывают чувство эйфории и/или удовольствия. Со временем и вследствие отсутствия опиоидов становятся активными пути, приводящие к высвобождению нейротрансмиттеров, таких как кортикотропин-рилизинг-фактор, норадреналин и динорфин, вызывающих дисфорию и/или дистресс
Расстройство, вызванное употреблением психоактивных веществ определяется 11 диагностическими критериями, охватывающими четыре основные области: признаки нарушения контроля, социальные нарушения, рискованное использование и фармакологические критерии. Расстройство, связанное с употреблением психоактивных веществ может быть классифицировано как легкое (2–3 критерия), среднее (4–5 критериев) или тяжелое (≥ 6 критериев) [16].
Поведение, ассоциированное с немедицинским использованием опиоидов (НМИО) [2]:
Текущий мониторинг
Научно обоснованные рекомендации по безопасному назначению опиоидов у пациентов с онкологической болью ограничены [9,14,15]. Американское общество онкологии разработало рекомендации по лечению боли у людей, переживших рак [14], а Национальная всеобщая онкологическая сеть США выпустила рекомендации по лечению боли, связанной с раком у взрослых [17]. Существующие данные предлагают универсальный подход к мерам предосторожности, состоящий из первоначального скрининга всех пациентов с раковой болью, которым требуются опиоиды, с использованием инструментов для оценки риска [2].
Пациентам, имеющим высокий риск немедицинского использования опиоидов, потребуется усиленный мониторинг. До начала приема опиоидов врачи должны информировать пациентов о потенциальных рисках, преимуществах, альтернативах и возможных побочных эффектах, связанных с опиоидной терапией, а также информировать их о безопасных методах использования, хранения и утилизации опиоидов [14]. Выбор, начальная дозировка и поддерживающие дозы опиоидов должны быть адаптированы к индивидуальным особенностям пациента, таким как уровень интенсивности боли и наличие почечной или печеночной дисфункции [15]. Четкий план прекращения лечения опиоидами следует заранее обсудить с пациентом, если этиология боли предполагает ожидаемое время ее прекращения, например, связанный с лечением оральный мукозит у пациентов, перенесших трансплантацию стволовых клеток или лучевую терапию при раке головы и шеи [2].
Программы мониторинга отпускаемых по рецепту лекарств
Принятие мер
Меры, которые обычно применяются для решения проблем немедицинского применения опиоидов включают в себя следующее: четкое изложение шагов, которые необходимо предпринять при повторном несоблюдении режима приема лекарств, сокращение временного интервала между последующими получениями добавок для для обеспечения более частого и бдительного мониторинга, ограничения количества опиоидов и дозы пополнения, отмена опиоидов, когда это возможно, обращение к специалисту по боли, паллиативной медицине, психическому здоровью или наркомании для совместного ведения [15]. Информирование в отношении безопасного использования, хранения и утилизации опиоидов должно быть обеспечено как пациентам, так и лицам, осуществляющим уход за ними. Конечной целью опиоидной терапии у пациентов с эпизодами немедицинского употребления опиоидов является достижение приемлемого обезболивания, улучшение физической и психосоциальной функции и минимизация осложнений с целью оптимизации соотношения риск-польза для обеспечения безопасного использования опиоидов [2].

a) Универсальный скрининг включает в себя опросы и использование инструментов оценки риска (CAGE — опросник для оценки риска, SOAPP — скрининг необходимости опиоидов для пациентов с болью, ОRТ — инструмент оценки опиоидного риска).
b) Усиленный мониторинг включает использование программ контроля отпускаемых по рецепту лекарств, выборочные анализы мочи на наркотики и тщательное наблюдение за поведением для выявления патологических признаков, связанных с употреблением опиоидов.
c) Немедицинское использование опиоидов (см. Поведение, ассоциированное с немедицинским использованием опиоидов)
d) Дополнительные стратегии включают в себя уменьшение временного интервала между контрольными исследованиями для повторных назначений, ограничение количества опиоидов и дозы добавок, установление ограничений, отмена опиоидов при первой возможности, обращение к специалисту для дальнейшего ведения.
НМИО — немедицинское использование опиоидов.
У пациентов с поздней стадией рака развивается ряд физических и психологических симптомов, и боль часто лечится в контексте множества сопутствующих проблем, таких как усталость, тошнота, эмоциональное расстройство и делирий. Более половины людей, замеченных в немедицинском применении опиоидов, получали опиоиды по рецепту от друга или родственника бесплатно, а 11 % покупали опиоиды у тех же лиц [18]. После эпидемии передозировки опиоидами были сделаны призывы к клиницистам пересмотреть практику назначения опиоидов пациентам в конце жизни. Для безопасного назначения опиоидов пока нет регламентированных условий, но, возможно, стоит обеспечить свободный законный доступ к опиоидам определенным лицам с неизлечимыми заболеваниями [2].
Перед тем, как сделать внутримышечную инъекцию, следует хорошо подготовиться. Проверьте лекарство и шприц. Он должен быть подходящего объема! Затем помойте руки и вытрите их чистым полотенцем.

Следующие действия
Для начала необходимо найти большую миску, тарелку или лоток и протереть ее поверхность спиртом. Это будет ваша специальная емкость для размещения в ней рабочего инструментария.
- Помещение пациента на диван (кровать) для расслабления мышц. Освещение должно быть хорошим.
- Надевание стерильных перчаток. Их обрабатывают спиртом.
- Приготовление ватных тампонов, смачивание их в спирте. Можно использовать спиртовые медицинские салфетки.
- Открывание упаковки со шприцем. Ампула обрабатывается спиртом. Если набор лекарства осуществлялся чрез резиновую крышку. Иглу необходимо заменить.
- Переворачивание шприца вверх и выпускание капли раствора для выпускания воздуха. в верхнюю часть мысленно нарисованного большого креста, разделяющего ягодицу. Это важно сделать для того, чтобы не повредить нерв.
- Протирание антисептиком места для инъекции (от центра).
- Размещение иглы под углом 90 к телу.
- Уверенное и быстрое движение иглой вниз, в ягодицу (треть иглы остается снаружи).
- Медленное введение лекарства. Шприц не должен дергаться! Держите его одной рукой. Другая рука давит на поршень.
- Вытаскивание иглы (одно движение) и прижимание ранки спиртовой салфеткой.
После всей процедуры необходимо обязательно закрыть иглу колпачком и вымыть руки. Утилизируйте использованные инструменты в тщательно закрытой коробочке!
Приобретайте медикаментозные препараты и шприцы самого высокого качества от солидных производителей в социальной сети аптек Столички.
Читайте также:

