Как сделать трансплантацию сердца
Обновлено: 06.07.2024
В Российской Федерации 7 % взрослых людей страдают хронической сердечной недостаточностью (ХСН). Ежегодно, даже в условиях лечения в специализированном стационаре, умирает до 12 % больных с клинически выраженной ХСН. Единственное, что может помочь пациенту в терминальной стадии этого заболевания, — трансплантация сердца.
Не все нуждающиеся в операции доживают до ее проведения, но с тех пор как 46 лет назад бригада доктора Кристиана Барнарда провела первую в мире пересадку сердца от человека к человеку, у них по крайней мере появилась надежда на выздоровление.
История вопроса
Успехи трансплантологии связаны с развитием двух независимых сфер медицины: совершенствованием хирургической техники и методов анестезии с одной стороны, и достижениями иммунологии и фармакологии — с другой. Первое обеспечило удачное проведение операций, а второе — благополучное протекание послеоперационного периода.
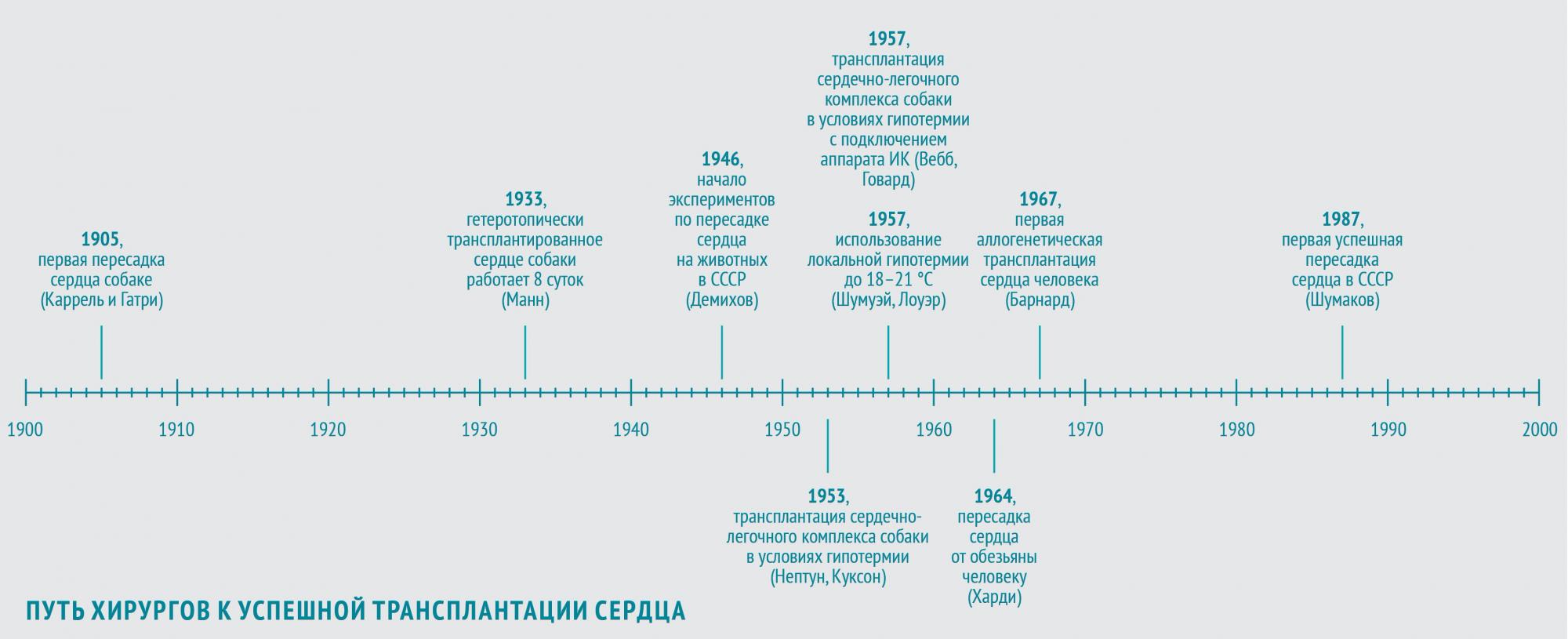
Первые шаги
Однако широкий интерес идея трансплантации органов вызвала лишь спустя 300 лет, когда хирурги массово приступили к практическим опытам. Вновь столкнувшись с проблемой отторжения, они обогатили медицину тремя важными выводами: межвидовые пересадки органов (ксенотрансплантации) всегда неуспешны; пересадки между представителями одного вида (аллогенетические трансплантации) в большинстве случаев тоже, причем повторные пересадки органов между одними и теми же донорами и реципиентами ускоряли отторжение; если между донором и реципиентом было кровное родство, вероятность благоприятного исхода операции значительно увеличивалась, причем пересадка собственных органов (аутотрансплантация) почти всегда были удачна.
Первая описанная в литературе успешная трансплантация датируется II веком нашей эры: индийский хирург Шушрата произвел пересадку кожи в ходе ринопластики.
А в III веке, если верить хроникам римской католической церкви, святые Дамиан и Косма пересадили потерявшему ногу от гангрены римскому дьякону Юстиниану конечность недавно умершего эфиопа.
Собачье сердце
В 1905 году в череде опытов по пересадке органов очередь дошла и до сердца. Первую трансплантацию сердца собаки-донора на сосуды шеи собаки-реципиента осуществили хирург, биолог и патофизиолог Алексис Каррель и физиолог Шарль Гатри, американцы французского происхождения. Донорское сердце проработало 2 часа.
В 1933 году американский физиолог Фрэнк Манн с коллегами повторил опыт Карреля и показал возможность функционирования гетеротопически (то есть размещенного в нетипичном месте) трансплантированного сердца собаки вплоть до 8 суток (собственное сердце собаки оставалось на месте и продолжало работать).
В ногу со временем шли и советские хирурги. Наиболее весомый вклад в экспериментальные основы трансплантации сердца в СССР внес Владимир Петрович Демихов. С 1946 по 1955 год он в нескольких сотнях экспериментов разработал 24 (!) варианта хирургической техники гетеротопической трансплантации сердца в грудную клетку. В некоторых опытах донорское сердце эффективно обеспечивало кровообращение собаки-реципиента в течение более чем 15 часов.
Борьба с ишемией
Самой явной проблемой, вставшей на пути хирургов, стала ишемия: в условиях недостаточного кровотока повреждались и ткани реципиента, и донорские сердца. Трансплантацию невозможно провести в сжатые сроки, поэтому хирурги и анестезиологи стали искать способы, позволяющие продлить время операции. Так были разработаны методы управляемой гипотермии и спроектированы аппараты искусственного кровообращения (ИК).
Управляемая гипотермия позволяет снизить кровопотерю, а также продлить время операции без повышения риска ишемизации тканей.
В 1953 году американские хирурги Уилфорд Нептун и Брайан Куксон с коллегами выполнили первую трансплантацию сердечно-легочного комплекса собаки в условиях глубокой гипотермии (во время операции в комнате поддерживалась температура порядка минус 4 °С).
В 1957 году американцы Уильям Вебб и Хизер Говард повторили этот эксперимент, подключив собаку-реципиента к аппарату ИК. Позднее они сообщили о пересадке в тех же условиях изолированного сердца. Они накладывали девять анастомозов между аортой, легочной артерией, легочной и полой венами. Правда, этот трансплантат профункционировал всего 7 часов.
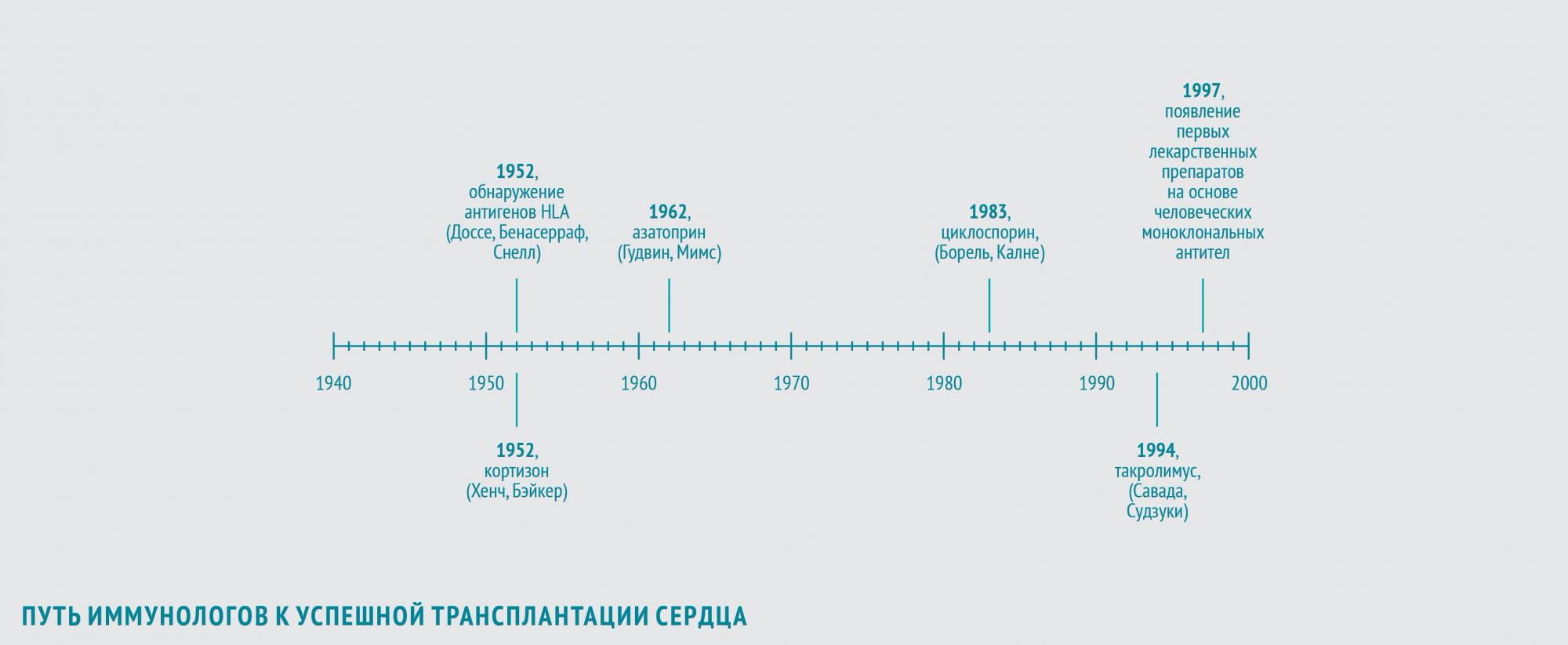
Причины отторжения
В 1952 году иммунологи Жан Доссе (Франция) и Барух Бенасерраф (США) вместе с генетиком Джорджем Снеллом (США) обнаружили, что важнейшие антигены, участвующие в отторжении трансплантата, – антигены главного комплекса гистосовместимости (HLA). За это открытие в 1980 году они были удостоены Нобелевской премии.
Существует порядка 150 вариантов антигенов HLA, и у каждого человека на мембранах клеток присутствует по шесть вариантов таких антигенов. Следовательно, возможно более триллиона их комбинаций – вероятность существования двух людей с одинаковыми комплексами HLA-антигенов близка к нулю, конечно, если они не однояйцевые близнецы. Идеально, если у донора и реципиента наблюдается несовпадение лишь одного антигена из шести. Операции проводят и в том случае, если не совпадают два, однако при этом увеличивается риск развития иммунологического отторжения.
На практике определение совместимости тканей — гистотипирование — осуществляется по лимфоцитам крови.
Немалую роль в отторжении трансплантата могут сыграть и антитела в организме реципиента (например, появившиеся из-за предшествующего переливания цельной крови). Взаимодействуя с антигенами эндотелия сосудов, пронизывающих трансплантат, они инициируют систему комплемента и каскад реакций, приводящий к закупорке сосудов.
Иммуносупрессия
Первыми веществами, которые начали использовать для подавления иммунного ответа, стали кортикостероиды.
В 1948 году американский врач Филип Хенч, применив кортизон в лечении ревматоидного артрита, показал, что препарат обладает выраженным противовоспалительным действием. В 1952 году американский хирург Роджер Бэйкер с коллегами продемонстрировал, что кортизон может использоваться и для иммуносупрессии после трансплантации.
В 1962 году американцы Уиллард Гудвин и Мэтт Мимс впервые использовали азатиоприн — иммуносупрессивный препарат, обладающий наибольшей активностью в отношении Т-лимфоцитов, для предотвращения острого отторжения трансплантированной почки. Пациентам с пересаженным сердцем также планировалось назначать азатиоприн в сочетании с кортикостероидами.
Очередь человека
Человеку сердце было впервые пересажено в 1964 году. Джеймс Харди с коллегами трансплантировали сердце крупного шимпанзе, весившего более 43 кг, больному 68 лет с тяжелой формой ИБС в терминальной стадии прогрессирующей сердечной недостаточности. Вначале трансплантат работал удовлетворительно, однако через час после отключения аппарата ИК развилась острая сердечная недостаточность, обусловленная объемной перегрузкой трансплантата, и больной погиб.
В СССР первая успешная трансплантация сердца была осуществлена в 1987 году знаменитым врачом-трансплантологом академиком АМН СССР Валерием Ивановичем Шумаковым (1931–2008).
Успех первого клинического опыта увлек медицинское сообщество, и к решению задачи трансплантации сердца обратились хирурги всего мира. Однако большинство пациентов умирало вскоре после проведения операции, и интерес исследователей начал угасать: если в 1968 году было проведено 100 трансплантаций сердца, то в 1970 — всего 18. Главной причиной смерти оставалось отторжение пересаженных органов.
Лишь четверо из прооперированных в период с 1967 по 1973 год прожили с новым сердцем дольше года; с 1974 по 1983 год годичная выживаемость увеличилась до 60 %, а вот пятилетняя составила лишь 21 %.
Иммунологи и фармакологи берутся за дело
В 1983 году увенчались успехом клинические исследования нового иммуносупрессора — циклоспорина, нерибосомного полипептида, получаемого из почвенных грибов вида Beauveria nivea. Его выделили в 1970 году в рамках программы по скринингу новых антибиотиков. В 1972 году бельгийский иммунолог Жан-Франсуа Борель открыл способность циклоспорина ингибировать культуру лимфоцитов при отсутствии общего цитостатического эффекта. В конце 70-х британский хирург Рой Калне провел первые испытания эффективности циклоспорина после трансплантации сердца и почек на экспериментальных животных. Его внедрение в широкую практику открыло новую эру в трансплантации сердца, поскольку позволило значительно продлить жизнь пациентов после трансплантации. В 1994 году было одобрено использование для послеоперационной терапии еще одного нового иммуносупрессора — такролимуса (FK-506) из группы макролидов, продуцируемого актиномицетом Streptomyces tsukubaensis. В 1987 году японские иммунологи Шиничи Савада и Джен Судзуки в экспериментах in vitro обнаружили, что такролимус в 100 раз активнее циклоспорина подавляет пролиферацию Т-лимфоцитов. В исследованиях на крысах, собаках и приматах, проводившихся с 1988 по 1993 год, такролимус обеспечивал профилактику отторжения трансплантата в дозах в 10–100 раз более низких, чем циклоспорин, и с меньшим количеством побочных эффектов. Впрочем, модификации циклоспорина, разработанные в то же время, обладали аналогичными преимуществами.
В настоящее время используется трехкомпонентная схема иммуносупрессивной терапии: циклоспорин А или такролимус в сочетании с метилпреднизолоном и микофенолата мофетилом (цитостатиком, который наиболее эффективен в отношении лимфоцитов). Препараты антилимфоцитарных антител (ALG, ATG, ОКТ-3) применяются в качестве вводной терапии, а также при выраженных признаках отторжения или стероид-резистентном отторжении.
Современная статистика
На сегодняшний день в мире проведено уже более 15000 трансплантаций сердца. 10-летняя выживаемость пациентов составляет около 50 %. Самая большая летальность — в первый год после операции (в разных клиниках – от 15 до 25 %). Основные причины смерти — инфекционные заболевания и саркома Капоши, развивающиеся на фоне иммуносупрессивной терапии.
Описаны и счастливые случаи, когда пациенты с трансплантированным сердцем прожили более 25 лет. Мировым рекордсменом стал Тони Хьюзман — пациент клиники при Стэнфордском университете. Его прооперировали в 1978 году, показанием послужила дилатационная кардиомиопатия. После трансплантации он прожил 30 лет и умер в 51 год от рака кожи.
В мире ежегодно выполняется от 2,7 до 4,5 тысяч трансплантаций сердца. Из них в России — всего около 100 операций. Лидер по количеству трансплантаций — США: там проводится до двух тысяч пересадок сердца ежегодно.
Показания для проведения операции по пересадке сердца
Диагноз:
- кардиомиопатии различного генеза;
- доброкачественные опухоли сердца;
- неоперабельные врожденные пороки сердца (например, гипоплазия левого желудочка).
Клинико-функциональная характеристика пациентов:
- хроническая сердечная недостаточность III-IV ФК по NYHA, резистентная к медикаментозной терапии;
- фракция выброса ЛЖС 7 см;
- конечно-диастолическое давление ЛЖС > 20 мм рт. ст.
- сердечный индекс (CI) 2 );
- рефрактерность желудочковых тахиаритмий;
- ожидаемая выживаемость потенциального реципиента без трансплантации сердца 15 мм рт. ст., общее легочное сопротивление (ОЛС) > 5 ед. Вуда, систолическое давление в легочной артерии более 60 мм рт. ст.);
- острые инфекционные заболевания и/или обострение хронических;
- необратимая полиорганная недостаточность;
- злокачественные новообразования в анамнезе;
- тромбофлебит;
- системные заболевания;
- ожирение (> 30 % должной массы тела);
- психические заболевания, алкоголизм, наркомания;
- недисциплинированность в приеме медикаментов, несоблюдение больничного режима.
Относительные противопоказания
- активный диффузный миокардит;
- инсулинозависимый сахарный диабет;
- язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения;
- нарушение мозгового кровообращения в анамнезе;
- инфицирование вирусами гепатита С и гепатита В;
- атеросклероз сосудов нижних конечностей;
- ограниченная поддержка семьи.
Задачи на будущее
Интересная методика, позволяющая продлить жизнь ожидающим пересадку сердца пациентам с дилатационной кардиомиопатией, разработана в 2002 году специалистами Научного центра хирургии РАМН во главе с доктором медицинских наук Алексеем Коротеевым. Его команда успешно опробовала на практике следующую методику: после курса интенсивной кардиотерапии больному делают спиральную томографию, чтобы создать точную трехмерную компьютерную модель сердца. Затем по индивидуальному муляжу шьется сетка из специального полиэфирного материала – дакрона. В ходе последующей операции сетку надевают на живое сердце, что препятствует дальнейшей дилатации.
До сих пор актуален поиск эффективной терапии послеоперационных осложнений. Большинство из них (инфекции, саркома Капоши, поражение почек и печени, а также быстрое развитие атеросклероза коронарных сосудов трансплантата) развиваются из-за постоянного использования иммуносупрессоров.

Трансплантация сердца – процедура, при которой хирург удаляет сердце пациента и замещает его донорским. Во время операции механический насос заставляет кровь циркулировать по телу, в то время как хирург занимается пересадкой здорового сердца от недавно умершего донора.
Хирург присоединяет донорское сердце к основным кровеносным сосудам и подключает к нему провода, которые будут временно контролировать сердцебиение. Вся процедура занимает несколько часов.
Чтобы предотвратить отторжение донорского сердца, хирург даёт пациенту сильные медикаменты (иммунодепрессанты) сразу после операции. Подобные препараты пациенту будет необходимо принимать еще некоторое время.
2. Реабилитация после операции
Что ожидать после операции по пересадке сердца?
После операции по пересадке сердца процесс восстановления схож с другими операциями на сердце.
Скорее всего, вы проведёте пару недель в больнице. В некоторых случаях вам понадобиться больше времени в зависимости от того, как будет оценено состояние вашего здоровья и будут ли осложнения после операции. В больнице вы начнёте программу реабилитации при болезнях сердца. Ваши лечащие врачи будут проверять, приживается ли донорское сердце в вашем организме.
Реабилитация после пересадки сердца
Программа реабилитации поможет вам восстановиться после пересадки сердца и вновь стать активным.
Донорское сердце может реагировать на нагрузку по-разному. Пульс не будет расти так, как раньше. Сердцебиение будет приходить в норму также по-другому. Это происходит потому, что некоторые нервные связи, отвечавшие за контроль сердца, были разрезаны в ходе операции.
3. Показания к операции по пересадке сердца
Операция по пересадке сердца проводится тогда, когда сердце перестаёт работать и пациент находится на грани жизни и смерти. Трансплантация сердца также проводится, если у пациента серьёзная болезнь сердца и наилучшие прогнозы на выздоровление даёт только операция. Пациенту может быть рекомендована пересадка сердца, если у него:
- Терминальная стадия сердечной недостаточности, ишемическая болезнь сердца, кардиомиопатия или врожденный порок сердца.
- Низкие шансы прожить дольше оного года без пересадки сердца.
- Отсутствие любых других серьёзных медицинских причин, снижающих продолжительность жизни.
- Если лечащий врач считает, что пересадка сердца увеличит продолжительность и качество жизни.
В некоторых медицинских центрах кандидаты на пересадку сердца должны представить доказательства того, что они отказались от курения и/или не злоупотребляют алкоголем продолжительное время (4-6 месяцев), перед тем как их поставят в очередь на трансплантацию.
4. Риски при пересадке сердца
Основные риски операции по пересадке сердца включают в себя:
Отторжение донорского сердца. Чтобы проверить организм пациента, хирурги регулярно проводят биопсию тканей сердца, а также эхокардиографию, электрокардиографию или анализ крови.
Если организм пациента отторгает сердце, то прописываются дополнительные лекарства (иммунодепрессанты или стероиды), которые подавляют иммунную систему, чтобы она приняла донорское сердце. У этих лекарств могут быть побочные эффекты, самые серьёзные из которых – различные инфекции и развитие рака.
Атеросклероз артерий, который мог появиться в донорском сердце. Обычно это осложнение и одновременно - важный ограничительный фактор, который влияет на продолжительность жизни.
О чём стоит подумать
После пересадки сердца вы должны следовать строгим правилам жизни, в которые входит ежедневный приём лекарств и регулярный медицинский уход. Под медицинским уходом подразумевается постоянные анализы (биопсия) тканей пересаженного сердца в целях предотвращения отторжения.
Кандидаты на пересадку получают сердце в соответствии с датой постановки на учёт и серьёзностью заболевания. Также не стоит забывать о том, что количество донорских органов ограничено.
Как это работает
Для людей, прошедших необходимые тесты, операция по пересадке сердца обычно очень успешна. Примерно 9 из 10 человек живут как минимум год после операции. Примерно половина – более десяти лет.
У большинства людей повышается качество жизни после операции. Они активны, ведут общественную жизнь и возвращаются к работе.
Актуальность проблемы развития трансплантации сердца (ТС) заключается в широкой распространенности заболеваний сердца, приводящих к хронической сердечной недостаточности (ХСН), а следовательно, в большом количестве пациентов, нуждающихся в этапном лечении ХСН , в том числе и в ТС .
Статистика ХСН в России такова:
- В 2002 году в РФ насчитывалось 8,1 миллионов человек с диагнозом ХСН , из которых 3,4 миллиона имели III–IV ФК по NYHA.
- Смертность больных в течение одного года с клинически выраженной ХСН (III-IV ФК) достигает 26–29 %, то есть за один год в РФ умирает от 880 до 986 тысяч больных с ХСН .
Показания и противопоказания к трансплантации сердца для отбора больных на лист ожидания
Показания к трансплантации сердца
Диагноз:
- Кардиомиопатии различного генеза
- Доброкачественные опухоли сердца
- Неоперабельные врожденные пороки сердца (ВПС).
- Хроническая сердечная недостаточность III-IV ФК по NYHA, резистентная к медикаментозной терапии.
- ФВ ЛЖС 7 см.
- КДД ЛЖС > 20 мм рт. ст.
- CI 15 мм.рт.ст., ОЛС > 5 ед. Вуда, систолическое давление в легочной артерии более 60 мм рт. ст.).
- Острые инфекционные заболевания и/или обострение хронических.
- Необратимая полиорганная недостаточность.
- Злокачественные новообразования в анамнезе.
- Тромбофлебит.
- Системные заболевания.
- Ожирение (> 30% должной массы тела).
- Психические заболевания, алкоголизм, наркомания.
- Недисциплинированность в приеме медикаментов, несоблюдение больничного режима.
Относительные противопоказания
- Активный диффузный миокардит.
- Инсулино-зависимый сахарный диабет.
- Язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения.
- Нарушение мозгового кровообращения в анамнезе.
- Инфицирование вирусами HDV и HCV.
- Атеросклероз сосудов нижних конечностей.
- Ограниченная поддержка семьи.
Мы будем рады сотрудничеству в помощи больным с тяжелой сердечной недостаточностью.

Еще недавно декомпенсированная сердечная недостаточность считалась смертным приговором. Однако сегодня, когда медицина шагнула вперед, появились методики пересадки сердца, у пациентов появился шанс на жизнь. Но, несмотря на весь прогресс, трансплантация сердца до сих пор считается сложной, высокотехнологичной операцией, требующей тщательной подготовки.
Показания к трансплантации сердца
Для трансплантологов важен внимательный подбор реципиента – пациента, которому будет пересажено сердце. В первую очередь рассматривают тех людей, которым уже не помогают лекарства, но которые смогут вернуться к активной жизни, если у них будет здоровый орган. Показаниями для операции являются:
- фракция выброса левого желудочка менее 20%;
- Na в сыворотке крови менее 135 мэкв\л;
- давление заклинивая в легочной артерии более 25 мм .рт.ст.;
- уровень норадреналина в плазме крови более 600 пкг\мл;
- кардиоторакальный индекс более 0,6;
- снижение максимального VO 2 менее 10 мл\кг\мин.
Важно, чтобы эти показатели оставались сохранными при максимально возможной медикаментозной поддержке. При приведенных показателях прогноз однолетней выживаемости без пересадки сердца составляет менее 50%.
Подготовка пациента к операции
Трансплантация сердца – сложное вмешательство, требующее тщательной подготовки. Пациент проходит многоступенчатое обследование, прежде чем принимается решение о возможности пересадки органа. Необходимо:
- тщательно собрать анамнез заболевания;
- выполнить рентгенографию органов грудной клетки;
- пройти нагрузочный тест на максимальное потребление кислорода ( VO 2);
- сдать ряд анализов на инфекции для исключения гепатитов, ВИЧ и ряда других заболеваний, которые могут стать противопоказанием;
- сдать рутинные анализы мочи, крови для оценки общего состояния организма;
- пройти зондирование сердца с тонометрией правых отделов (необходимо, чтобы исключить легочную гипертензию, которая выступит противопоказанием к трансплантации);
- сдать анализ для оценки человеческого лимфоцитарного антигена ( HLA );
- пройти ЭКГ, ЭхоКГ.
При обследовании могут быть выявлены как абсолютные, так и относительные противопоказания, исключающие постановку пациента в лист ожидания донорского сердца.
Техника трансплантации
Не всем пациентам из-за декомпенсации заболевания есть возможность сразу выполнить трансплантацию. Если состояние больного неудовлетворительное, могут использовать:
- Фармакологический мост к трансплантации – методику, при которой при помощи лекарственных средств (в основном инфузионные ионотропные средства) доводят состояние больного до удовлетворительного.
- Механический мост к трансплантации – методику, основанную на моно- или бивентрикулярном обходе желудочков или применении искусственного сердца в предоперационном периоде.
Операция идет в условиях налаженного искусственного кровообращения. Трансплантацию могут выполнить гетеротопично или ортотопично. В первом случае донорское сердце размещают под сердцем пациента, не удаляя последнее. Эта методика применяется при выраженной гипертензии в малом кругу кровообращения. В прочих случаях донорское сердце заменяет собственный орган пациента.
Послеоперационный период
После операции пациент находится под наблюдением врача в течение длительного промежутка времени. В этот период подбирается иммуносупрессивная терапия с помощью гормонов и цитостатиков, благодаря которой удается избежать процессов отторжения, оценивается состояние послеоперационной раны, корректируются осложнения, если они возникают.
В первый месяц после операции раз в 1,5-2 недели выполняют биопсию миокарда. Это необходимо, чтобы оценить состояние донорского сердца. Со временем эта процедура проводится все реже.
Мировой опыт и цены
Как показывает практика, пересаженное сердце при соблюдении всех медицинских рекомендаций, способно без перебоев работать в течение 5-7 лет. Однако процессы старения в донорском органе идут быстрее, чем в собственном, а потому рано или поздно пациент отметит возвращение всех симптомов сердечной недостаточности.
Реальная практика пересадки сердца в разных значительно отличается. В некоторых странах данные операции совсем не проводятся, потому что не урегулированы на законодательном уровне. В других странах такие операции четко регламентируются и к ней могут прибегнуть, как жители самой страны, так иностранные граждане. Например, в Республике Беларусь органная трансплантация осуществляется в соответствии с законом, в основе которого лежит "презумпция согласия": забор органа у донора может быть осуществлен после констатации смерти мозга, если пожелания обратного не выражены пациентом до смерти. Орган может быть использован в дальнейшим нуждающимся пациентам.
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
Тимур Абдулнаимович Халилулин, профессор:
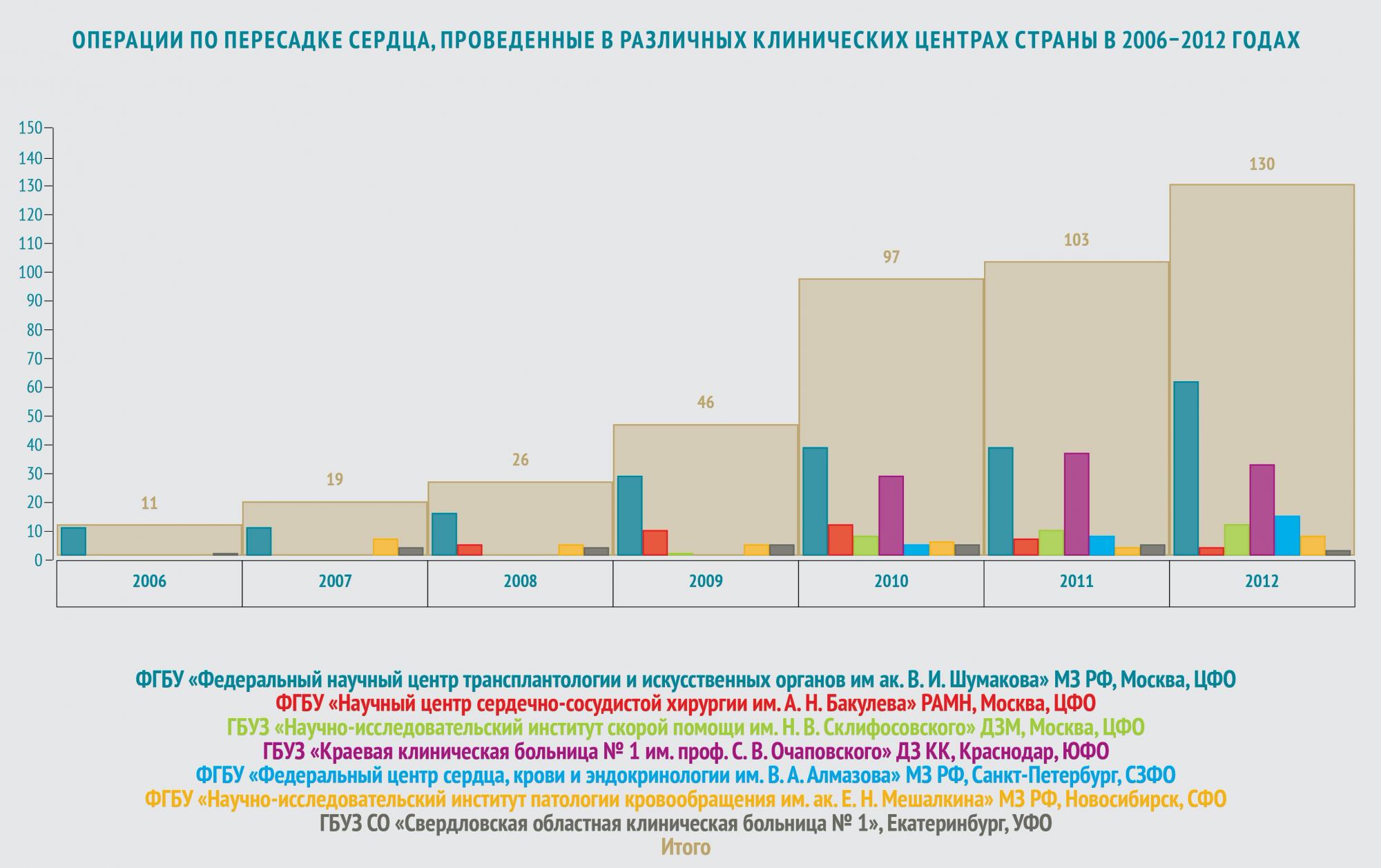
Лидером за последние годы по объему выполненных оперативных вмешательств является Федеральный центр трансплантологии и искусственных органов имени академика Шумакова. Опыт нашего центра позволяет говорить о существенном увеличение объемов пересадки сердца за последние годы, и такая тенденция имеет ежегодный прирост. За прошлый год нам удалось выполнить больше 60 трансплантаций сердца. В этом году за неполные пять месяцев выполнено уже более 30-ти пересадок сердца, это приблизительно столько же, сколько в 2011-м году. Это говорит о том, что в этом году, скорее всего, объемы по трансплантации сердца прошлого года мы существенно превысим.
Полученные результаты позволяют добиться того, что по объемам трансплантации сердца сейчас мы уже попадаем в десятку крупнейших кардиохирургических центров мира. В среднем же большинство центров за рубежом выполняют от 10 до 19 трансплантаций сердца. В этом году, увеличив объем трансплантаций сердца до более 70-ти трансплантаций в год, мы надеемся попасть в тройку лидирующих кардиохирургических центров мира по объему трансплантаций сердца.
Какова предтрансплантационная патология у пациентов, которые находятся в листах ожидания? Как за рубежом, так и у нас, это преимущественно пациенты двух основных нозологий – это ишемическая болезнь сердца, ее осложненное течение, это дилатационная кардиомиопатия. То есть те патологии, которые приводят к развитию тяжелой застойной сердечной недостаточности. Однако стоит отметить, что за последние годы выросло количество к повторной ре трансплантации сердца – за рубежом и у нас это около 2-3% от всех выполняемых оперативных вмешательств. Это уже те пациенты, которые ранее, много лет назад перенесли трансплантацию сердца и у них возникли возможные осложнения после операции – это болезнь коронарных артерий пересаженного сердца, персистирующее острое отторжение клеточного антител-обусловленного типа. Эти пациенты с прогрессирующей сердечной недостаточностью уже попали повторно в лист ожидания на пересадку сердца, и им повторно была выполнено оперативное вмешательство. Происходит это в связи с тем, что увеличивается количество трансплантаций сердца, и все больше пациентов могут рассчитывать не только на трансплантацию сердца, но и на повторное ее применение.
Увеличиваются объемы трансплантации сердца как правило за счет многих критериев. Во-первых, за счет расширения показаний, за счет увеличения возраста реципиентов сердца, возраста донора, утяжеления пациентов, находящихся в листе ожидания. В частности, ранее мы предполагали, что средний возраст пациентов будет в районе 30-35 лет. И преимущественно это были пациенты с дилатационной кардиомиопатией, которая характерна для более молодого возраста. Сейчас же за счет того, что у многих пациентов в листе ожидания присутствует ишемическая болезнь сердца, это могут быть уже оперированные ранее пациенты, которым выполнена резекция аневризмы, аортокоронарное шунтирование. Возраст пациентов возрастает уже, в среднем, до 40 с лишним лет. Это могут быть и пациенты более возрастной группы – это могут быть пациенты и 60-ти, и 70-ти лет. Процент пациентов, которым выполняется подобное оперативное вмешательство в последние годы, увеличивается. Увеличивается количество тяжелых пациентов в листе ожидания. Пациенты градуируются по статусу UNOS на несколько категорий. Категория со статусом 1А и 1В – это наиболее тяжелая когорта пациентов, которые требуют помимо медикаментозной терапии еще и введения внутривенно инотропных препаратов, а часть из них требует механической поддержки кровообращения с помощью различных систем вспомогательного кровообращения ЭКМО, имплантируемого искусственного желудочка, и так далее. Порядка трети пациентов в листе ожидания – от 25% до 35% находится именно на такой медикаментозной или механической поддержке сердца. Это обеспечивает достаточно высокую тяжесть пациентов в листе ожидания. Но тем не менее результаты, о которых мы поговорим чуть позже, позволяют говорить о хорошей эффективности выполнения подобных вмешательств.
Расширение возможностей трансплантации сердца возможно за счет увеличения возраста доноров, которых используют для трансплантации сердца. Это доноры с диагнозом смерти мозга, и их средний возраст также возрастает. Сейчас он составляет более 35 лет в среднем. Это могут быть и пациенты более старшей возрастной группы, около 50-ти лет при условии наличия сохранного трансплантата без сложной некорригируемой патологии, которая бы не позволила эффективно работать трансплантату уже после операции.
В плане расширения показаний к трансплантации сердца можно использовать и донорские сердца с возможной корригируемой патологией. Один из таких вариантов – например, использование донорских сердец с корригируемой митральной недостаточностью. Например, это расщепление передней створки митрального клапана с наличием регургитации. Когда перед операцией, перед началом имплантации донорского сердца фактически в тазике производится реконструкция митрального клапана, и затем это сердце уже имплантируется пациенту. Это один из возможных вариантов расширения возможностей трансплантологии. С хорошим результатом пациент после подобной трансплантации был выписан домой, и сейчас уже больше года прошло после операции, и чувствует себя хорошо, без сложностей и проблем.
Каковы результаты проводимых оперативных вмешательств? Насколько эффективно они сказываются на качестве и длительности жизни пациентов? В среднем, период жизни пациентов после трансплантации сердца составляет 10-12 лет. Это общие сводные зарубежные и российские данные. У нас, по данным наших исследований пятилетняя выживаемость актуарная близка к 80%. Это говорит о действительно хороших результатах. Но эти результаты должны быть сопряжены еще с высоким качеством жизни, которое может обеспечить трансплантация сердца пациентам с исходно тяжелой застойной сердечной недостаточностью высокого функционального класса.
Среди обследованных нами пациентов после трансплантации сердца мы отметили, что уровень физической активности восстанавливается практически у 90% пациентов после трансплантации сердца. Это исследование было выполнено с помощью шкалы Карновского. И характерно, что к году и к третьему году после трансплантации сердца данный функциональный статус у пациентов остается сохранным. Принципиально важно, что более 80% пациентов в состоянии вести нормальную деятельность, не требуют ухода за собой к концу первого года после трансплантации сердца. Это хороший, эффективный результат.
Как меняется качество жизни больных после трансплантации сердца? Как мы видим, до трансплантации сердца физическое функционирование, социальные, психоэмоциональные аспекты качества жизни пациентов сильно страдают. И по данным опросника sf-36 они действительно находятся на нижних пороговых значениях. После трансплантации сердца, к году, уровень их физического функционирования, психоэмоциональный статус восстанавливается до значений, близких значению здоровых пациентов. Это говорит о весьма высокой эффективности. Принципиально важным здесь является восстановление физического качества жизни, практически до 90% пациентов, это возможность работать и трудиться, которую имеют около 40% пациентов после выполнения подобных оперативных вмешательств.
Итак, хочется сказать о том, что трансплантация сердца является оправданной стратегией лечения пациентов в аспекте того, что с помощью ее можно достичь высокой физической и социальной реабилитации пациентов после операции. Но дело все в том, что выживаемость пациентов после трансплантации сердца ограничена рядом возможных осложнений. Такие осложнения могут быть как в раннем послеоперационном периоде, так и в достаточно позднем.
Ранние послеоперационные осложнения после трансплантации сердца касаются как правило первичной дисфункции трансплантата, которая может развиться в первый послеоперационные часы и дни после операции. Здесь ее коррекция возможна как правило с помощью механических систем вспомогательного кровообращения либо усиления инотропной поддержки. Возможны инфекционные осложнения как бактериальной, так и вирусной природы на фоне иммуносупрессий, и, безусловно, острое отторжение.
В отдаленные сроки чаще всего мы сталкиваемся с болезнью коронарных артерий пересаженного сердца. И это особая патология у больных с трансплантируемым сердцем, которая серьезно ограничивает выживаемость пациентов после этих оперативных вмешательств. Кроме того, в отдаленные сроки возможно развитие также отторжений, инфекционных осложнений. Это как правило вирусные инфекции, герпес-группы и цитомегаловирусные инфекции и онкообразования.
Коснемся наиболее часто возникающих из них. За последние годы за счет изменения протоколов иммуносупрессии у пациентов после трансплантации сердца, количество эпизодов острого отторжения как клеточного, так и антител-обусловленного типа стало существенно меньше. И сейчас это около 25%. Ранее – до 50% пациентов переносили эпизоды клеточного и антител-обусловленного отторжения разной степени тяжести. Другим, наиболее важным отторжением, с которым мы сталкиваемся и, наверное, одним из самых интересных – это болезнь коронарных артерий пересаженного сердца. Это патология, которая имеет некоторое сходство с ишемической болезнью сердца и некоторые общие факторы риска с ИБС. Однако основной патогенез развития данного заболевания связан с иммунной патологией, с применением иммуносупрессантов и развитием иммуно-обусловленного поражения коронарных артерий. Существует несколько типов поражений коронарного русла. Одним из наиболее легких в плане лечения типом поражений коронарных сосудов является тип А, когда имеются дискретные, проксимальные стенозы коронарных артерий, подобные тем, которые встречаются при ишемической болезни сердца. На слайде мы видим пациентку 21-го года после трансплантации сердца. На второй год после трансплантации сердца выполнена коронарография и выявлен стеноз в проксимальном сегменте передней межжелудочковой ветви. Далее с помощью стентирования удалось восстановить эффективный кровоток по передней межжелудочковой ветви и добиться хорошего результата в восстановлении функции сердца.
Но так, к сожалению, бывает далеко не всегда. При типах поражения С, когда имеет место дистальное, окклюзирующее поражение коронарного русла возможности ангиопластики, к сожалению, остаются исчерпанными. Вот, в частности, пациент, у которого на первом году выполнена коронарография после операции. Мы видим хорошее коронарное русло. И справа от вас вы видите коронарограмму через три года после трансплантации сердца, где имеет место дистальное, окклюзирующее поражение коронарных артерий, говорящее, в общем-то, о бесперспективности лечения с помощью ангиопластики. И единственный вариант возможного здесь лечения – это продолжение медикаментозной коррекции у пациента, использование плазмаферезов, модификации иммуносупрессии. И если нарастает сердечная недостаточность, то повторная трансплантация сердца.
В связи с этим разрабатываются различные протоколы, подходы в лечении пациентов с болезнью коронарных артерий пересаженного сердца. И основную роль играет, конечно же, профилактика развития подобных осложнений. Одним из возможных аспектов дальнейшего изучения факторов риска как острого отторжения, так и болезни коронарных артерий пересаженного сердца является изучение факторов риска болезни коронарных артерий пересаженного сердца. Одним из таких факторов риска являются биомаркеры при развитии васкулопатии трансплантата. Это известные вам биомаркеры РАРР-А, sCD40L, PLGF, которые являются также маркерами нестабильного течения атеросклероза у пациентов с ишемической болезнью сердца. Их исходно высокий уровень, превышающий пороговые значения, выявленный до трансплантации сердца, является прогностическим маркером в развитии острого отторжения и васкулопатии трансплантата. Подобные биомаркеры применяются в практике изучения факторов риска до трансплантации сердца.
Терапия пациентов после трансплантации сердца сочетает в себе несколько компонентов. Это, прежде всего, иммуносупрессивный компонент, который включает в себя базовую иммуносупрессию, а также индукционную иммуносупрессию. Индукционная рассчитана на введение препаратов в раннем послеоперационном периоде и предназначена для того чтобы купировать ранние острые отторжения у пациентов с пересаженным сердцем. Далее пациент переходит на базовую иммуносупрессию, которая включает в себя несколько компонентов. Это по нашей практике такролимус, метилпреднизолон и препараты микофеноловой кислоты.
Индукционная иммуносупрессия как правило включает в себя базиликсимаб и метилпреднизолон. Такова терапия, которая предназначена для лечения пациентов в плане иммуносупрессий. В плане кардиологической терапии это использование препаратов, которые направлены на профилактику кардиологических осложнений – это прежде всего препараты группы ингибиторов АПФ, антагонисты кальция и статины.
Среди последних хочется отметить интересный аспект в плане не только их гиполипидемического действия, но и принципиально важное их действие, которое в настоящий момент активно изучается – это влияние на снижение уровня маркеров, которые мы обсуждали ранее: РАРР-А, sCD40L, PLGF. Нами показано, что применение одного из статинов Розувастатина у данной группы пациентов сразу после трансплантации сердца позволяет добиться значимого снижения уровня sCD40L и РАРР-А, исходно высоких до трансплантации сердца, до значений, соответствующих нормальным показателям. Это позволяет рассчитывать на уменьшение факторов риска развития после трансплантационных осложнений в ранние и отдаленные сроки у пациентов. Но для этого еще требуются дополнительные исследования.
Кроме того среди других нелипидных эффектов, которые нами были отмечены – это влияние на уровень С-реактивного белка. Достигнуто достоверное снижение уровня сразу после трансплантации сердца, в течение первых трех месяцев. Кроме того, показана хорошая эффективность применения подобной терапии у пациентов после трансплантации сердца. Уровень цистатина С не менялся после трансплантации сердца у этих пациентов на фоне применения статинов в комбинации с иммуносупрессивными препаратами.
Таким образом, хочется отметить, что терапия пациентов с пересаженным сердцем должна включать в себя несколько комбинаций препаратов. Конечно, безусловно, основной является иммуносупрессивная терапия, и основными будут являться протоколы, применяемые в иммуносупрессии и их модификации, чтобы увеличить качество и продолжительность жизни пациентов. Но тем не менее существенно важным остается использование и препаратов, которые предназначены для профилактики кардиологических осложнений. Здесь на первое место должны выступать, конечно же, статины, которые имеют не только нелипидный эффект, не только гиполипидемический эффект, но и нелипидные эффекты, подобные тем, которые были описаны.
Читайте также:

