Как сделать реакцию вюрца
Обновлено: 07.07.2024
2\u04412\u043d5br+ 2na (\u0442\u0430\u043a\u0436\u0435 \u043f\u043e\u0441\u0442\u0443\u043f\u0430\u0435\u043c \u043a\u0430\u043a \u0438 \u0432 \u043f\u0440\u0435\u0434\u044b\u0434\u0443\u0449\u0435\u043c \u043f\u0440\u0438\u043c\u0435\u0440\u0435) =c4h10 (\u0438\u0437 \u0431\u0440\u043e\u043c\u043c\u0435\u0442\u0430\u043d\u0430 \u043f\u043e\u043b\u0443\u0447\u0438\u043b\u0438 \u0431\u0443\u0442\u0430\u043d)+2nabr">]" data-testid="answer_box_list">
Реакция вюрца заключается в том что идет удвоения из хлорэтана или бромметана получить алканы. всегда прибавляется натрий. например 2сн3cl + 2na ( перед хлор метан ставим 2,чтобы сделать удвоение)=c2h6(с помощью удвоения мы получили этан) +2nacl
2с2н5br+ 2na (также поступаем как и в предыдущем примере) =c4h10 (из бромметана получили бутан)+2nabr
Новые вопросы в Химия
5.27. Массовая доля метанола в водном растворе ранна 40 %. Определите объемную долю (в процентах) метанола. Плотность метанола равна 0,8 г/мл, воды г/ … мл. Изменением объемов при смешивании пренебречь.
Вычисли массу бромоэтана, который можно получить из технического этанола массой 25г. содержащий примеси, массовая доля которых составляет 8%
Вычисли массу этанола, который можно получить из технического этена объемом 44,8л (н. у), если он содержит примеси этана, объемная доля которых состав … ляет 2%
Наведіть приклади використання процесів горіння. а) у засобах транспорту. б) у паливній енергетиці. в) у піротехніці
. Вычислите массу сульфата натрия, образовавшегося при реакции 5,5 г оксида натрия с серной кислотой.
РЕАКЦИЯ ВЮРЦА – химическая реакция, позволяющая получать простейшие органические соединения – предельные углеводороды.
Сама реакция Вюрца заключается в конденсации алкилгалогенидов под действием металлического Na, Li или реже K:
2RHal + 2Na ® R–R + 2NaHal.
Иногда ее трактуют как взаимодействие RNa или RLi с R'Hal.
Реакция была открыта французским химиком-органиком Шарлем Вюрцем (Wurtz Charles (1817–1884) в 1855 при попытке получения этилнатрия из хлористого этила и металлического натрия.
Несмотря на то, что реакция Вюрца приводит к образованию новой углерод-углеродной связи, она нечасто применяется в органическом синтезе. В основном с ее помощью получают предельные углеводороды с длинной углеродной цепью, особенно она полезна при получении индивидуальных углеводородов большой молекулярной массы, и, как видно из приведенной схемы, для получения заданного углеводорода следует брать только один алкилгалогенид, так как при конденсации двух алкилгалогенидов получается смесь всех трех возможных продуктов сочетания. Поэтому если используется алкилгалогенид и натрий, реакцией Вюрца можно получить только углеводороды с четным количеством атомов углерода. Наиболее успешно реакция Вюрца протекает с первичными алкилйодидами. Очень низкие выходы целевого продукта получают при использовании метода Вюрца для вторичных алкилгалогенидов. Реакцию обычно проводят в диэтиловом эфире. Использование углеводородов в качестве растворителей уменьшает селективность реакции.
Однако если использовать заранее приготовленное металлоорганическое соединение, например алкиллитий, то можно получить и несимметричные продукты конденсации:
RLi + R'Hal ® R – R' + LiHal
В обоих случаях реакция сопровождается образованием большого количества побочных продуктов за счет побочных процессов. Это иллюстрирует пример взаимодействия этиллития с 2-бромоктаном:
В этом случае 3-метилнонан и ряд побочных продуктов в указанных молярных соотношениях образуются как продукт реакции Вюрца.
Кроме натрия, в реакции Вюрца использовались такие металлы, как серебро, цинк, железо, медь и индий.
Реакция Вюрца успешно применяется для внутримолекулярных конденсаций для построения карбоциклических систем. Так из 1,3-дибромпропана под действием металлического цинка и йодида натрия (в качестве промотора реакции) может быть получен циклопропан:
Можно построить и другие напряженные карбоциклические системы. Например, из 1,3-дибромадамантана, используя натрий-калиевый сплав, может быть получен 1,3-дегидроадамантан:
А взаимодействие 1-бром-3-хлор-циклобутана с натрием приводит к бициклобутану:
Известен ряд разновидностей реакции Вюрца, получивших свои собственные названия. Это реакция Вюрца – Фиттига и реакция Ульмана. Первая заключается в конденсации алкил- и арилгалогенида под действием натрия с образованием алкилароматического производного. В случае реакции Ульмана в конденсацию обычно вводят арилйодиды, а вместо натрия используют свежеприготовленную медь, эта реакция позволяет с высоким выходом получать различные биарильные производные, в том числе, и несимметричные, содержащие заместитель в одном из ароматических ядер:
Как полагают, механизм реакции Вюрца состоит из двух основных стадий:
1) образование металлоорганического производного (если использется металл, а не заранее приготовленное металлоорганическое соединение):
RHal + 2Na ® R–Na + NaHal,
2) взаимодействие образовавшегося, в данном случае, натрийорганического соединения с другой молекулой алкилгалогенида:
RHal + R–Na ® RR + NaHal.
В зависимости от природы R и условий проведения реакции вторая стадия процесса может протекать по ионному либо по радикальному механизму.
Вацуро К.В., Мищенко Г.Л. Именные реакции в органической химии. М., 1976
Шабаров Ю.С. Курс органической химии. М., Химия, 1998
ВЮРЦА РЕАКЦИЯ
ВЮРЦА РЕАКЦИЯ, конденсация алкилгалогенидов под действием Na (реже - Li или К) с образованием предельных углеводородов:
2RHal + 2Na -> R—R + 2NaHal,
где Hal - обычно Br или I. При использовании в р-ции разл. алкилгалогенидов (RHal и R'Hal) образуется трудноразделяемая смесь всех возможных продуктов (R—R, R'—R', R'—R).
Вюрца реакция легко протекает, если алкилгалогенид имеет большую мол. массу, а галоген связан с первичным атомом С. Процесс проводят при низких т-рах в сольватирующих р-рителях. Так, в ТГФ р-ция осуществляется быстро и с хорошим выходом уже при — 80 °С.
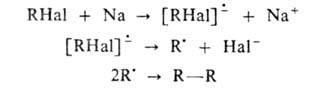
Предполагается, что механизм р-ции включает образование ион-радикалов и радикалов:
Однако факт обращения конфигурации нек-рых оптически активных алкилгалогенидов (напр., 2-хлороктана в р-ции с Na) не исключает возможности гетеролитич. механизма.
Р-ция открыта Ш. Вюрцем в 1855 и используется гл. обр. для получения углеводородов с длинной углеродной цепью. В др. случаях, особенно при получении несимметричных ал-канов, применяют разл. модификации Вюрца реакции, рассмотренные ниже.
Для синтеза жирноароматич. соед. используют модификацию Фиттига (р-цию Вюрца-Фиттига):
ArHal + RHal + 2Na -> Ar—R + 2NaHal
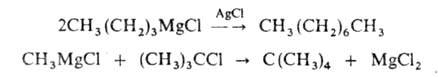
Р-ция открыта Р. Фиттигом в 1855. Часто с хорошим выходом образуются алканы с использованием реактива Гриньяра, напр.:
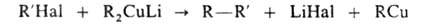
Несимметричные предельные углеводороды получают, используя медьорг. соед.:
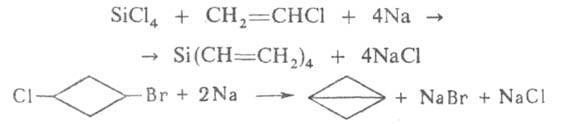
Р-цию, подобную Вюрца реакции, используют для синтеза элементоорг. соед. и бициклич. соед., напр.:
Реакция Вюрца имеет ограниченное применение, поскольку она приводит к соединению двух алкильных групп и, таким образом, к алкану с большим числом атомов углерода, чем в исходных веществах. Таким образом
можно получить этан из бромистого метила, н-бутан из бромистого этила и 2,3-диметилбутан из бромистого изопропила
Реакция Вюрца пригодна только для синтеза симметричных алканов Например, этим методом нельзя получить с хорошим выходом пропан. Если натрий реагирует со смесью бромистого метила и бромистого этила, то действительно образуется пропан; но он будет в смеси с этаном, образовавшимся при соединении двух метальных групп, и н-бутаном, образовавшимся из двух этильных групп. Значительное количество реагентов расходуется на образование ненужных продуктов; кроме того, возникает проблема разделения. Следовательно, реакция Вюрца непригодна для синтеза несимметричных алканов различные алкильные группы).
Хотя многие реакции простых алкилгалогенидов можно распространить и на более сложные галогенсодержащие соединения, это не относится к реакции Вюрца. Металлический натрий — очень реакционноспособное вещество, и он будет реагировать не только с галогеном, но и с любой другой группой, которая может быть в более сложном соединении. Например, реакцию Вюрца нельзя применять для соединений, в которых, кроме галогена, имеется НО-группа, поскольку натрий будет реагировать с гидроксильной группой быстрее, чем с галогеном (разд. 16.6).
Механизм реакции Вюрца сложный и до конца еще не выясиен, но ясно, что в реакции сначала образуется натрийорганическое соединение, аналогичное магнийорганическому соединению, описанному выше,
которое затем реагирует со второй молекулой алкилгалогенида
(Реактив Гриньяра менее реакционноспособен, чем натрийорганическое соединение: он реагирует только с некоторыми очень реакционноспособными органическими соединениями.)
Читайте также:

