Как сделать лабораторную работу по химии 8 класс
Добавил пользователь Alex Обновлено: 04.10.2024
Образовательная цель: знать названия предметов лабораторного оборудования; освоить приемы обращения с лабораторным оборудованием.
Развивающая цель: мышление через постановку вопросов в ходе работы и ответы на вопросы.
Воспитательная цель: воспитывать коммуникативные отношения при работе в паре согласно инструкции; соблюдать дисциплину при выполнении работы.
Оборудование: лабораторный штатив, спиртовка, посуда: пробирки, колбы, химические стаканы; фильтры, воронки, прибор для получения газов.
Включить учащихся в деятельность
2.Познакомится с планом работы
1.Записывает тему урока.
2.Участвует в обсуждении темы.
Учащиеся готовы к работе.
2.Практическая работа №1.
Знать названия предметов лабораторного оборудования; освоить приемы обращения с лабораторным оборудованием.
Знать названия предметов лабораторного оборудования; освоить приемы обращения с лабораторным оборудованием.
1.Чертят таблицу в тетради.
Таблица в тетради.
2.1.Читают правила техники безопасности при работе в химической лаборатории на с.174 в учебнике.
2.2.Сравнивают с правилами в инструкции.
2.4.Раписываются в журнале по ТБ.
Ознакомлены с правилами по ТБ.
3.1.Изучают устройство лабораторного штативы.
3.2.Выполняют задание, указанное в инструкции.
3.3.Делают схематический рисунок и подписывают части.
В таблице заполнены графы.
Выполняют описанные в ней действия.
Собран штатив и закреплена пробирка.
В таблице заполнены графы.
В таблице заполнены графы.
Соотнести цель с результатами работы на уроке.
Соотнести цель с результатами работы на уроке.
Определить своё место в уроке и оценить свою деятельность.
Результат соответствует цели урока.
Оценить деятельность учащихся
Выставляют оценки в карту знаний.
1.Устная оценка деятельности всех учащихся.
2.Практическая работа оформлена в тетрадях.
Инструкция для учащихся:
1.Прочитай инструкцию по технике безопасности при работе в химической лаборатории на с.174-175.
2.Обсудите вопросы, возникшие после чтения. Сформулируйте их для учителя. Задайте вопросы учителю.
3.Распишитесь в журнале по ТБ.
4.Начертите таблицу в тетради.
6.Сделайте схематический рисунок и подпишите части.
10.Сделайте вывод по итогам работы.
Название этапа работы
Рисунок и название частей оборудования.
Приемы работы с лабораторным оборудованием.
Приемы работы с лабораторным штативом
1.Винт, закрепляющий муфту находится справа от стержня штатива, а стержни лапки укреплялись бы так, чтобы их поддерживал не только винт, но и муфта.
2.Пробирку закрепляют ближе к горлышку.
3.Пробирка укреплена правильно, если ее можно повернуть в лапке без больших усилий.
Приемы работы со спиртовкой
1.Нельзя зажигать спиртовку от другой горящей спиртовки.
2.Гасят спиртовку накрывая ее колпачком с боку.
Приемы работы с посудой.
1.Высота столбика жидкости при перемешивании растворов в пробирке не должна превышать 2 см.
2.Запрещается встряхивать пробирку, закрывая отверстие пальцем.
3.Фильтр перед употреблением смачивают.
4.В чашку наливают 1/3 объёма для выпаривания.
5.Проверить прибор на герметичность.
Вывод: освоил приемы работы с лабораторным оборудованием.
Полный текст материала Практическая работа по химии №1 "Приемы обращения с лабораторным оборудованием"; 8 класс смотрите в скачиваемом файле.
На странице приведен фрагмент.
Спасибо за Вашу оценку. Если хотите, чтобы Ваше имя
стало известно автору, войдите на сайт как пользователь
и нажмите Спасибо еще раз. Ваше имя появится на этой стрнице.

Есть мнение?
Оставьте комментарий
Упражнения на технику чтения и понимания прочитанного
Тонкости и секреты работы в Яндекс.Почте
Как работать с детьми с СДВГ в обычном классе?
0 Спам
0 Спам
0 Спам
Елена Ивановна, пожалуйста, не забывайте указывать в файле материала сведения о себе как об авторе материала.
Отправляя материал на сайт, автор безвозмездно, без требования авторского вознаграждения, передает редакции права на использование материалов в коммерческих или некоммерческих целях, в частности, право на воспроизведение, публичный показ, перевод и переработку произведения, доведение до всеобщего сведения — в соотв. с ГК РФ. (ст. 1270 и др.). См. также Правила публикации конкретного типа материала. Мнение редакции может не совпадать с точкой зрения авторов.
Для подтверждения подлинности выданных сайтом документов сделайте запрос в редакцию.
О работе с сайтом
Мы используем cookie.
Публикуя материалы на сайте (комментарии, статьи, разработки и др.), пользователи берут на себя всю ответственность за содержание материалов и разрешение любых спорных вопросов с третьми лицами.
При этом редакция сайта готова оказывать всяческую поддержку как в публикации, так и других вопросах.
Если вы обнаружили, что на нашем сайте незаконно используются материалы, сообщите администратору — материалы будут удалены.
ГДЗ к рабочей тетради по химии за 8 класс Габриелян О.С. можно скачать здесь.
ГДЗ к тетради для оценки качества знаний по химии за 8 класс Габриелян О.С. можно скачать здесь.
ГДЗ к контрольным и самостоятельным работам по химии за 8 класс Павлова Н.С. можно скачать здесь.
ГДЗ к тетради для лабораторных опытов и практических работ по химии за 8 класс Габриелян О.С. можно скачать здесь.
ГДЗ к контрольным работам по химии за 8 класс Габриелян О.С. можно скачать здесь.
ГДЗ к контрольным и проверочным работам по химии за 8 класс Габриелян О.С. можно скачать здесь.
ГДЗ к рабочей тетради по химии за 8 класс Микитюк А.Д. можно скачать здесь.
ГДЗ к учебнику по химии за 8 класс Габриелян О.С. (Просвещение) можно скачать здесь.

Бесплатное участие. Свидетельство СМИ сразу.
До 500 000 руб. ежемесячно и 10 документов.
Является первой практической работой, на которой изучаются правила техники безопасности при работе в химической лаборатории. Ребята научатся работать с лабораторным штативом, нагревательным прибором, изучат их строение и назначение составляющих частей. Изучат строение пламени. Ознакомятся с некоторой химической посудой. Оборудование: лабораторный штатив, нагревательный прибор, спички, пробирка, химический стакан, колба, фарфоровая чашка, воронка, прибор для получения газов, аппарат Кирюшкина, сетка для нагревания.
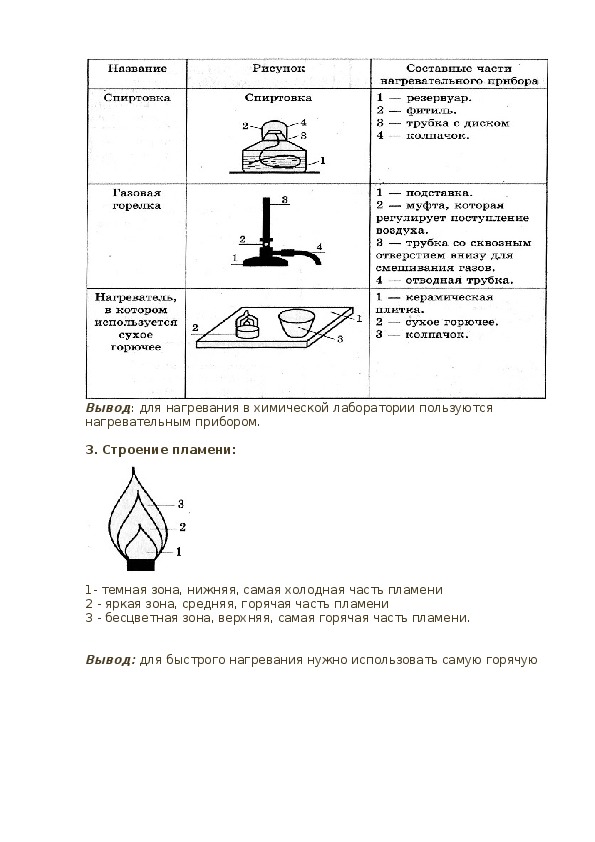
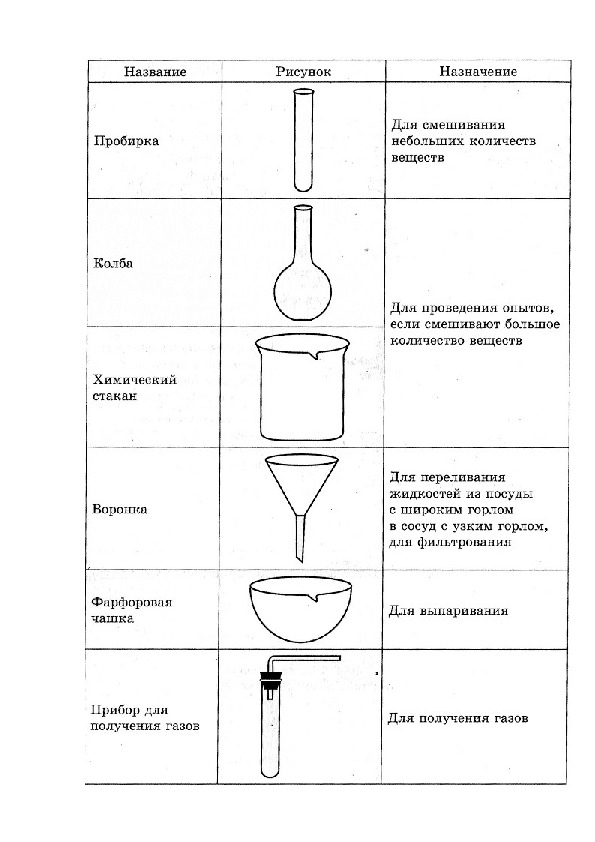
Практическая работа №1 Химия 8 класс (к учебнику Габриеляна О.С.) Приемы обращения с лабораторным оборудованием Цель: изучить правила техники безопасности при работе в химической лаборатории. Научиться работать с лабораторным штативом, нагревательным прибором, изучить их строение и назначение составляющих частей. Изучить строение пламени. Ознакомиться с некоторой химической посудой. Оборудование: лабораторный штатив, нагревательный прибор, спички, пробирка, химический стакан, колба, фарфоровая чашка, воронка, прибор для получения газов, аппарат Кирюшкина, сетка для нагревания. Порядок выполнения работы. I. Правила техники безопасности при работе в химической лаборатории. II. Лабораторное оборудование 1. Лабораторный штатив Вывод: лабораторный штатив используется для закрепления химической посуды и установки во время выполнения эксперимента. 2. Нагревательные приборы Вывод: для нагревания в химической лаборатории пользуются нагревательным прибором. 3. Строение пламени: 1- темная зона, нижняя, самая холодная часть пламени 2 - яркая зона, средняя, горячая часть пламени 3 - бесцветная зона, верхняя, самая горячая часть пламени. Вывод: для быстрого нагревания нужно использовать самую горячую часть пламени. 4. Посуда Выво : для работы в химической лаборатории пользуютс я разнообразной посудой, собирают различные прибор Общий вывод из работ ы были изуче ы правила техники безопасности при работе в химическо й лаборатории, работа с лабораторным штативом, нагревательны м прибором, строение пламени, виды и назначение химической посуд : в ходе выполнения практической работ
Практическая работа №1 Химия 8 класс (к учебнику Габриеляна О.С.) на тему "Приемы обращения с лабораторным оборудованием" (8 класс, химия)

Практическая работа №1 Химия 8 класс (к учебнику Габриеляна О.С.) на тему "Приемы обращения с лабораторным оборудованием" (8 класс, химия)

Практическая работа №1 Химия 8 класс (к учебнику Габриеляна О.С.) на тему "Приемы обращения с лабораторным оборудованием" (8 класс, химия)
Практическая работа №1 Химия 8 класс (к учебнику Габриеляна О.С.) на тему "Приемы обращения с лабораторным оборудованием" (8 класс, химия)

Практическая работа №1 Химия 8 класс (к учебнику Габриеляна О.С.) на тему "Приемы обращения с лабораторным оборудованием" (8 класс, химия)
Практическая работа №1 Химия 8 класс (к учебнику Габриеляна О.С.) на тему "Приемы обращения с лабораторным оборудованием" (8 класс, химия)


Бесплатный просмотр. Свидетельства участникам
для аттестации за минуту.
Ознакомление с коллекцией солей.
Ознакомьтесь с коллекцией выданных вам образцов солей. Запишите их формулы, охарактеризуйте физические свойства, в том числе и растворимость в воде. Рассчитайте относительные молекулярные (молярные) массы солей, а также массовые доли образующих их элементов. Найдите массу 2 моль каждой соли.
Решение
Допустим ученикам выдали: хлорид натрия (NaCl) и карбонад кальция ( $СаСО_$ ).
Хлорид натрия (NaCl)
| Свойства | Значение |
|---|---|
| Состояние | Твёрдые кристаллы |
| Плотность | 2,165 г/ $см^3$ |
| Температура плавления | 800,8 ℃ |
| Температура кипения | 1465 ℃ |
| Цвет | белая |
| Растворимость в воде | растворима |
| Теплопроводность и электропроводность | Проводит тепло и электрический ток |
Молекулярная масса соли равна сумме относительных атомных масс элементов, входящих в состав соли, с учётом их количества. То есть молекулярная масса хлорида натрия равна:
M (NaCl) = 1 * Ar (Na) + 1 * Ar (Cl) = 1 * 23 + 1 * 35,5 = 58,5 г/моль.
Массовые доли натрия и хлора в соли равны:
$ ω (Na) = \frac = \frac = 0,39$ или 39 %.
$ ω (Cl) = \frac = \frac = 0,61$ или 61 %.
Найдём массу двух моль соли.
m = n * M;
m (NaCl) = 2 * 58,5 = 117 г.
Карбонад кальция ( $СаСО_$ ).
| Свойства | Значение |
|---|---|
| Состояние | Твёрдые кристаллы |
| Плотность | 2 . 74 г/ $см^3$ (кальцит), 2 . 83 г/ $см^3$ (арагонит) |
| Температура плавления | 825 ℃ (кальцит), 1339 ℃ (арагонит) |
| Температура разложения | 900 − 1000 °C |
| Цвет | белая |
| Растворимость в воде | нерастворима |
| Теплопроводность | низкая теплопроводность |
Молекулярная масса карбонад кальция равна:
M ( $СаСО_$ ) = 1 * Ar (Ca) + 1 * Ar (C) + 3 * Ar (O) = 1 * 40 + 1 * 12 + 3 * 16 = 100 г/моль.
Массовые доли кальция, углерода и кислорода в соли равны:
$ ω (Са) = \frac
$ ω (С) = \frac
$ ω (O) = \frac
Найдём массу двух моль соли.
m = n * M;
m ( $СаСО_$ ) = 2 * 100 = 200 г.
Читайте также:

