Как сделать кристалл из льда
Обновлено: 07.07.2024
Кристаллы всегда привлекают внимание своей красотой, натуральностью и необычностью. Такими характеристиками обладают не только природные виды камней, но и искусственно созданные. Многие рукодельницы, начинающие химики задаются вопросом, как вырастить кристалл из соли в домашних условиях? Давайте разберемся с этой задачей, а также узнаем, что необходимо для создания такой красоты, как ускорить процесс роста, что добавить к раствору, чтобы получился яркий синий или голубой камень.
Что понадобится для выращивания кристаллов в домашних условиях
Чтобы в домашних условиях вырастить настоящий кристалл, необходима специальная посуда и соответствующий раствор. Процесс очень длительный, поэтому за считанные дни может ничего не получиться. Рост камня зависит от многих факторов: насыщенности раствора, температуры и влажности воздуха, вида соли, используемой для кристалла, основания. Для успешного выращивания такой красоты нужно подготовить:
- Емкость, где будет произрастать соляной кристалл (размеры могут быть любыми, все зависит от желаемой величины камня). Важен материал, из которого выполнена посуда. Он не должен окисляться в соленой воде и отдавать цвет.
- Поваренная соль (которая используется в домашнем обиходе).
- Палка, чтобы мешать раствор (из дерева или стекла).
- Фильтровальная бумага белого цвета или салфетки.

Как быстро вырастить кристалл из поваренной соли и воды
Задаваясь вопросом, как вырастить кристалл из соли, приготовьтесь, что для этой задачи вам понадобиться от 3 недель до 6-7 месяцев, в зависимости от желаемого размера итогового изделия. Полученный камень будет очень ломким, поэтому не стоит к нему прикасаться руками. Чтобы сохранить надолго такой шедевр, покройте изделие прозрачным лаком. Рассмотрим пошаговый процесс приготовления кристалла из поваренной соли:
- Возьмите небольшую емкость, желательно прозрачную.
- Смешайте чистую дистиллированную воду комнатной температуры с солью. Второго ингредиента насыпайте много, пока перемешивание с жидкостью не станет затруднительным. После насыщения раствора поставьте данную посуду на водяную баню, и растопите в ней соль до получения однородной массы.
- С помощью плотной марли или салфетки процедите жидкость, чтобы отделить от нее твердые примеси.
- Далее возьмите обыкновенную белую нить, привяжите к ней небольшой кристаллик соли и опустите к охлажденной жидкости. Если такого камешка нет, возьмите любой пластмассовый твердый предмет, предварительно замоченный в приготовленной воде и высушенный.
- На второй край нитки привяжите перекладину (к примеру, карандаш, линейку или ручку), которая будет шире горлышка выбранной посуды. Этот предмет будет фиксироваться на емкости с соленой водой, чтобы маленький кристаллик на нити был в подвешенном состоянии.
- Накройте полученную конструкцию бумагой, салфетками или тканью и поставьте на то место, где наименее заметны перепады температуры.
- Если выбранная емкость прозрачная, то легко проследить, какими темпами растет кристалл соли. Если так размеров не видно, время от времени можете поднимать нитку с камнем и проверять. Но не прикасайтесь пальцами к нему и не цепляйте камень о края конструкции.
- Через месяц изделие увеличится в размерах и станет размером как минимум с фасоль.
- Подождав еще немного (месяца 2), вы обнаружите, что камень стал диаметром около 3-4 см.
- Если размер кристалла вас устраивает, достаньте его, протрите сухими салфетками и покройте прозрачным лаком (для ногтей или другим). Когда вещество высохнет, камень можно будет брать в руки и любоваться.
Цветной кристалл: голубой или синий своими руками
Как вырастить кристалл из соли синего цвета? Только с использованием специальных пищевых красителей, которые могут дать не яркий оттенок. При смешивании соли и воды, туда же стоит добавить небольшое количество синего цвета. Когда молекулы начнут соединяться, кристалл приобретет необычный голубой оттенок. Для выращивания ярко синего камня придется иметь дело с медным купоросом.
Купить данное вещество вы можете в любом магазине для садоводов и дачников. С ним необходимо делать те же действия, что и с солью. Но поскольку химический состав медного купороса может быть опасен для здоровья, раствор рекомендуется убрать в недоступное для детей и животных место. Вот пошаговый процесс создания темно-синего кристалла:
- Насытьте дистиллированную воду медным купоросом так, чтобы он перестал растворяться.
- Нить опустите в жидкость на несколько часов, чтобы на ней образовался набор красивых кристалликов. Выберите наилучший среди них, остальные уберите обратно.
- Опустите нить с маленьким кристаллом в насыщенный раствор так, чтобы он не касался стенок. В течение нескольких недель или месяцев камень приобретет синий цвет невероятной красоты.
- Покройте изделие специальным прозрачным лаком, чтобы обезопасить от обветривания.
Как сделать большой белый кристалл из морской соли
При использовании классического варианта выращивания кристаллов, их делают из поваренной соли, которая используется в пищу. Этот продукт в больших количествах присутствует на полках любого продуктового магазина и стоит совсем недорого. Но из каких солей выращивать кристаллы лучше? Морская соль тоже подойдет для поставленной цели. Разница в том, каким получится результат.
Для получения необычных шедевров природы, нужно в одну емкость поставить выращивать кристалл из поваренной соли, а в другую – из морской. Во втором случае скорость роста может быть больше, так же как и плотность полученного камня. Внешний вид кристаллов тоже может отличаться, но только незначительно, поскольку молекулы морской и поваренной соли практически одинаковы.
Чтобы сделать крупный кристалл белого цвета из морской соли, воспользуйтесь таким способом:
- Приготовьте прозрачный стакан (или стеклянную банку) для будущего процесса.
- Растворите в теплой родниковой воде большое количество морской соли, процедите жидкость через плотную ткань или марлю.
- Влейте насыщенный раствор в выбранный стакан.
- Возьмите один кристалл морской соли, привяжите к нему нить и опустить в емкость с полученной жидкостью на несколько недель или месяцев.
- Когда размер камня будет таким, как вам нужно, выньте его, просушите салфетками и покройте лаком.
- Получив белый камень, окрасить его в другой цвет вы не сможете, поскольку пищевые краски будут стекать со стенок. Единственный выход для получения яркого оттенка камня – добавлять пигмент прямо в раствор, из которого будет расти кристалл.
- Если в процессе роста камня уровень жидкости снизится до минимума, влейте в емкость раствор такой же консистенции.
Фото и картинки кристаллов красивой и необычной формы
Когда через несколько месяцев у вас получится необычной красоты кристалл, вы обязательно захотите показать изделие друзьям, знакомым и сфотографировать его. Вот поэтому интернет уже полон фотографиями таких необычных камней. Они разные по форме: квадратные, прямоугольные, круглые и древовидные. Есть и оригинальные цвета кристаллов из соли: желтые, синие, голубые, красные. Посмотрите ниже подборку фотографий самых оригинальных вариантов солевых камней, выращенных дома.


Видео-инструкция: выращиваем дома из обычной соли
Чтобы уяснить все важные моменты выращивания кристаллов из соли, посмотрите видео с мастер-классами от экспертов в данном деле. В таких обучающих материалах часто демонстрируются разамеры полученных камней на разных стадиях их роста (через неделю, месяц, полгода). Эта видео-инструкция поможет вам правильно вырастить кристаллы дома из обычной соли:

Актуальность исследования. Зимой мы часто любовались покрытыми инеем деревьями, внимательно рассматривали снежинки во время снегопадов. И на одном из уроков окружающего мира мы узнали, что и иней, и снежинки это кристаллы, которые образовываются из паров воды.
Кристаллы встречаются повсюду. Они разнообразны, красивы, загадочны. Нам захотелось побольше узнать о том, какие бывают кристаллы, как они образуются, чем отличаются, и попытаться самой вырастить это маленькое чудо.
Объект исследования:кристаллы.
Предметом исследования — процесс кристаллизации.
Цель исследования:вырастить кристаллы из поваренной пищевой соли в домашних условиях.
Изучение научной литературы по теме исследования позволило выдвинуть следующую гипотезу: мы предполагаем, что в домашних условиях действительно можно вырастить кристаллы из поваренной соли.
В соответствии с целью и гипотезой исследования были определены следующие задачи:
Для решения поставленных задач и проверки гипотезы были использованы следующие методы исследования:
теоретический анализ литературы по исследуемой проблеме;
наблюдение за процессом роста кристалла;
Практическое значение исследования в том, что оно может быть использовано на уроках окружающего мира, во внеклассных мероприятиях.
Происхождение снежинки
Жизнь снежинки начинается высоко в небе, в холодном — прехолодном облаке.
Облака состоят из воздуха и воды. Но есть в них частицы и других веществ: соли, песка, пепла. Внутри облака могут оказаться даже живые бактерии, которые попали в небо на подхваченных ветром листьях деревьев. Такая частичка и нужна снежинке, чтобы начать расти (рис.1).

Как снежинка растет?
Водяные пары поднимаются высоко над землей, туда, где царит сильный холод. Там сразу же из водяных паров образуются крохотные льдинки-кристаллики. Это еще не те снежинки, какие падают на землю, они еще очень малы. Но шестиугольный кристаллик все время растет, развивается и наконец, становится удивительной красы звездочкой (рис.2)


Волшебное число 6.
Каждая снежинка имеет шесть лучей или шесть граней. Все из-за того, что при низкой температуре молекулы воды объединяются в группы по шесть, образуя правильные шестиугольники. Вот почему снежинки всегда имеют шестиугольную (плоскую) или шестигранную (объемную) форму. (рис.3).

Если представить снежинку в виде циферблата, ее лучи укажут на 2,4,6,8,10,12 часов.(рис.4)


Снежинки рождаются, когда маленькие капельки воды в облаках, попадая в холодную атмосферу, превращаются в кристаллы и замерзают. Ни одна снежинка не похожа на свою подружку-снежинку (рис. 5).


От чего зависит форма снежинки?
Японским ученым удалось выяснить, что форма снежинок зависит от температуры воздуха. Оказалось, что самые красивые кристаллы — звезды — появляются только при небольшом морозе (-14, -15, -16, -17 градусов). (рис.7).

Встречаются разные формы снежинок: игольчатые звезды; пластинчатые звезды; ежи, состоящие из нескольких столбиков; столбики с пластинками и звездами на концах. Встречаются также 12-лучевые звезды. Снежинки часто соединяются между собой и выпадают в виде хлопьев. Упадет снежинка на руку — не почувствуешь. Ведь весит она всего около миллиграмма! Чаще всего встречаются снежинки –звезды с шестью лучами (рис. 8).

Почему снежинки белые?
Снежинка — это снег, а снег — это просто замерзшая вода. Почему тогда снег белый, если это замерзшая вода? Он должен быть бесцветным. Снег белый оттого, что плоскость снежинки отражает свет, поэтому снег и кажется белым.
Почему снег скрипит под ногами?
Это происходит потому, что под тяжестью тела человека ломаются нежные лучики снежинок — звездочек. А так как их очень, очень много, слышится треск.
О чем поют снежинки?
При падении в воду снежинка создает крайне высокий звук, неслышимый для человека, но неприятный для рыб.
В лютый мороз самые маленькие снежинки прилетают погреться к нашим домам и остаются сказочными узорами на стеклах.
Побелело на ночь всюду.
А у нас в квартире чудо!
За окошком двор исчез –
Там волшебный вырос лес !
Снежинки растут, как растут кристаллы любого вещества, переходящего из жидкого состояния в твердое. Всего через несколько минут, упав на теплую поверхность, снежинка потеряет свой уникальный образ, который никогда снова не повторится.
Снежинки — это кристаллы, которые образуются из паров воды. Нам стало интересно, а из чего еще могут образовываться такие красивые кристаллы?
Основные сведения о кристаллах и их свойства
«Ярой альпийской зимой лед превращается в камень.
Кристаллы можно вырастить из растворов разных веществ. В природе кристаллы бывают разной формы, разного размера и цвета (рис.9).

Особое место среди кристаллов занимают драгоценные камни, которые с древнейших времен привлекают внимание человека. Люди научились получать искусственно очень многие драгоценные камни.
В природе найти нужный кристалл сложно, поэтому его можно вырастить искусственно. Нам стало интересно, можно ли выращивать кристаллы и как это сделать. Я решила вырастить снежинку из кристаллов соли.
Соль была известна человечеству с древнейших времен, ценилась на вес золота. К ней всегда относились очень бережно и уважительно.

В древнем Риме наёмным солдатам часто платили жалование не деньгами, а солью, отсюда и произошло слово солдат.Соль считали оберегом и наделяли защитными свойствами.
Михаил Васильевич Ломоносов писал, что в его время за 5 плиток соли можно было купить раба.
Получение кристаллов в домашних условиях
Этапы выращивания снежинки из кристаллов соли
белая пушистая (синельная) проволока (3 кусочка по 7 см)
пол-литровая стеклянная банка
поваренная соль (NaCl) ( около 18 чайных ложек),
белая нитка и деревянная палочка для подвешивания снежинки .

Ход эксперимента:
- Делаем снежинку, перемотав кусочки проволоки посередине обычной ниткой. Концы нитки должны остаться достаточно длинными, чтобы за них можно было подвешивать нашу снежинку.

- В литровую банку нальем кипяток. Можно и просто горячую воду, но чем горячее, тем быстрее будут образовываться кристаллы. Теперь туда же начнем добавлять соль, тщательно размешивая. Нам надо получить перенасыщенный солевой раствор — т. е. соль надо добавлять до тех пор, пока она не перестанет растворяться в воде. Если раствор получился мутным из-за того, что соль была с примесями, то его желательно отфильтровать и перелить в новую банку.

- Теперь в этот раствор опускаем нашу снежинку и ставим банку в тихое место.

- Процесс активного образования кристаллов будет идти быстро до тех пор, пока вода не остынет до комнатной температуры. Дальше процесс пойдет гораздо медленнее.


Поэтому примерно через несколько недель снежинка уже примет окончательный вид.
Заключение
При растворении поваренной соли в воде кажется, что соль полностью исчезает. Но это не так. Частички соли распадаются на мельчайшие кусочки, невидимые глазу. Но при определенных условиях они могут собраться вместе и снова стать видимыми. Да не просто видимыми, а создать причудливые структуры. Когда мы делаем перенасыщенный солевой раствор, растворяя в банке с водой соли больше, чем она может "принять", то излишки соли тут же начинают снова собираться в кристаллы. Очагом роста кристаллов может послужить любое тело в воде: пылинка, не растворившийся кристаллик той же соли или нитка. Поэтому когда мы опускаем в солевой раствор нашу снежинку, на ней тут же начинают расти кристаллы соли.
Гипотеза полностью подтвердилась. Нам удалось вырастить снежинку из кристаллов поваренной соли и научились проводить наблюдения за ростом кристалла.
Основные термины (генерируются автоматически): снежинка, кристалл, поваренная соль, соль, кристалл соли, снег, научная литература, перенасыщенный солевой раствор, пар воды, процесс роста кристалла.
Похожие статьи
Выращивание кристаллов в домашних условиях | Юный ученый
Процесс выращивания кристаллов поваренной соли не требует наличия каких-то особых химических препаратов. Кристаллы других солей выращиваются аналогично. Процесс выращивание кристаллов в домашних условиях можно разделить на основные этапы
Для выращивания кристалла мы поместили в концентрированный раствор соли на проволоке шишку так, чтобы она не касалась стенок емкости.
Изготовление теста из муки, соли и воды является старинным обычаем и применялось для выполнения фигурок из народных сказаний.
Кристаллы — это уникальные образования сложенных атомов. Многие кристаллы сделаны из минералов, но есть и другие типы материалов, которые также делают кристаллы. Что такое кристаллы? Что общего у снежинок, поваренной соли и карандаша? Это кристаллы.
Изучение некоторых физических свойств снега и процесса.
Снежинка — это замороженный кристалл воды (кристалл льда), имеющий форму шестилучевого многогранника. Кристаллы образуются в замороженных облаках при их переходе из парообразного состояния в замороженную, кристаллическую, твёрдую фазу.
Технология получения технического хлористого натрия из.
Упаренную суспензию, содержащую кристаллы поваренной соли и примесей, сгущают в отстойнике. При этом в осветленном растворе находятся кристаллы примесей, имеющие гораздо меньше, чем кристаллы поваренной соли размеры и потому уходящие с.
Влияние на рост и развитие растений макроэлементов.
Доказать отрицательное влияние раствора поваренной соли на рост и развитие растений. Минеральное питание является основным источником
В литературе встречается множество рекомендаций по применению поваренной соли как стимулятора роста растений и в борьбе с.
Снежинка — это кристалл льда, имеющий обычно форму 6-ти-угольных пластинок или
При замерзании молекулы воды выстраиваются в строго определённом порядке и образуют
Поскольку кристаллы льда шестиугольны, то лучи растут в шести направлениях под строго.
Исследовательская деятельность на уроках химии | Молодой ученый
Учебно-исследовательская деятельность учащихся на уроке химии.
Растворы веществ, которые готовят учащиеся на уроках (растворы солей с определенной массовой долей растворенного вещества.
Соавтор(ы): Meredith Juncker, PhD. Мередит Джанкер — аспирантка, работает над получением степени PhD по биохимии и молукулярной биологии в Медицинском центре Университета штата Луизиана. Ее исследования посвящены белкам и нейродегенеративным заболеваниям.
Количество источников, использованных в этой статье: 13. Вы найдете их список внизу страницы.
Кажется волшебством, когда в простом стакане воды как будто ниоткуда вырастают красивейшие кристаллы. На самом деле кристаллы образуются из растворенных в воде веществ. Проведите эксперимент по выращиванию кристаллов соли, и вы узнаете больше о том, как они образуются и растут.

- При обращении с горячей водой дети должны попросить помощи у взрослых.
- Лучше всего использовать дистиллированную воду, хотя подойдет и простая вода из-под крана. [1] X Надежный источник Science Buddies Перейти к источнику
- При нагревании воды ее молекулы начинают двигаться быстрее.

- Кристаллы поваренной соли вырастают в течение нескольких дней. Йодированная соль подходит хуже, хотя и она образует кристаллы. [2] X Источник информации
- Английская соль образует более мелкие кристаллы в виде иголок, причем они растут быстрее, чем из поваренной соли. Английскую соль можно приобрести в аптеке.
- Кристаллы квасцов вырастают быстро, иногда для этого требуется всего лишь несколько часов. [3] X Источник информации Квасцы можно приобрести в аптеке. [4] X Источник информации

- Итак, только что вы получили пересыщенный раствор. Это означает, что в растворе (жидкости) содержится больше соли, чем способна растворить вода! Когда вы разогрели воду, ее молекулы ускорились и расстояние между ними увеличилось, в результате чего в ней растворилось больше соли, чем в обычных условиях.

- Переливайте воду медленно и остановитесь, прежде чем в банку попадут крупинки соли. Если в банке окажутся нерастворившеся частицы соли, кристаллы могут вырасти на них, а не на бечевке.
- Пересыщенные растворы очень нестабильны, поэтому кристаллы могут выпасть в осадок, если вы встряхнете банку. Когда кристаллы растут, они поглощают тепло из раствора. [5] X Источник информации

Добавьте пищевой краситель (необязательно). С помощью пары капель пищевого красителя вы сможете изменить цвет кристаллов. Однако добавление пищевого красителя может привести к тому, что кристаллы будут немного более мелкими и комковатыми.

- Соль осядет на крохотных неровностях и краях бечевки, и они послужат местами зарождения и роста кристаллов. [6] X Источник информации Не используйте леску, так как она слишком гладкая.

Отрежьте подходящий кусок бечевки, чтобы она свободно висела в банке. Кристаллы вырастут лишь на той части бечевки, которая будет погружена в воду. При этом бечевка не должна касаться дна банки, иначе кристаллы получатся комковатыми и мелкими.

Всем мозгодрузьям большой привет! Хочу рассказать вам о моем интересном хобби, а именно о том, как самостоятельно выращивать красивые и большие кристаллы.

Выращивание кристаллов дело долгое, но увлекательное, для меня это даже не хобби, а страсть. И в этом мозгоруководстве я поделюсь своим опытом, своими советами и рекомендации о выращивании различных кристаллов, тем более что по этой теме очень мало полезной информации.
Шаг 1: Введение в мир кристаллов

Криста́ллы (от греч. κρύσταλλος, первоначально — лёд, в дальнейшем — горный хрусталь, кристалл) — твёрдые тела, в которых атомы расположены закономерно, образуя трёхмерно-периодическую пространственную укладку — кристаллическую решётку.
Кристаллы — это твёрдые вещества, имеющие естественную внешнюю форму правильных симметричных многогранников, основанную на их внутренней структуре, то есть на одном из нескольких определённых регулярных расположений составляющих вещество частиц (атомов, молекул, ионов). (Википедия)
В нашем большом мире существует огромное количество мозгокристаллов, которые имеют широкий спектр применения, к примеру, процессор компьютера сделан из кремния, который также является кристаллом. Итак, хватит разговоров, давайте займемся делом!
Шаг 2: Как сделать раствор (метод медленного испарения)

- кристаллический порошок — 100гр или больше (для получения больших кристаллов)
- дистиллированная или кипяченая вода – 100мл
- фильтровальная бумага
- чистые банки – 2 шт.
- терпение
- Смешайте кристаллический порошок и воду.
- Перемешивайте до полного растворения порошка.
- Отфильтруйте раствор, при этом не переживайте если часть порошка не растворилась.
- Оставьте раствор на некоторое время, кристаллы не растут быстро.
- После появления нескольких маленьких кристалликов выберите наиболее вам понравившийся и аккуратно выньте его.
- Снова профильтруйте раствор и поместите в него обратно выбранный вами кристалл. Поступайте так каждый раз при появлении новых кристалликов.
- Когда раствор не будет полностью покрывать ваш выращиваемый кристалл, сделайте новый раствор по тому же рецепту.
- Выращивание кристаллов занимает много времени, так что будьте терпеливы.
Советы (для выращивания всех кристаллов):
ВНИМАНИЕ. Не касайтесь руками, не пробуйте кристаллы и вещества для их приготовления на вкус, так как некоторые из них являются высокотоксичными (дихромат калия, нитрат калия или соединения йода)! Соблюдайте ТЕХНИКУ БЕЗОПАСНОСТИ и консультируйтесь со специалистом!
Шаг 3: Кристалл медного купороса










Для выращивания кристалла медного купороса нужно 100гр сульфата меди CuSO 4 , вода, фильтровальная бумага и 3 месяца времени.
. Медный купорос ядовит. Не пробуйте его!
Шаг 4: Кристалл из алюминиевых квасцов







Необходимы KAL (SO 4 ) 2, вода, фильтр.бумага и так же три месяца мозговремени.
Кристалл не ядовит, в прошлом его использовали для остановки кровотечений.
Шаг 5: Жеода дихромата калия



Для этой жеоды нужно 200гр дихромата калия K 2 Cr2 O 7 и другие материалы (вода, фильтровальная бумага и т.д.)
Чтобы создать эту жеоду сохраняйте все образующиеся кристаллы, не удаляйте их при фильтровании. Кристалл растет быстро и без особого ухода, через несколько дней ожидания уже появляется небольшая жеода.
. Дихромат калия очень токсичен!! Не касайтесь его без перчаток, не пробуйте его, тем более не давайте играть детям. Выращивайте жеоду в хорошо проветриваемом помещении.
Шаг 6: Кристалл сульфата никеля




Материалы те же: 100гр порошка сульфата никеля NiSO 4 , бумага, вода.
Из этого порошка можно вырастить кристаллы двух видов: при нагревании раствора до 30 ° С получаются кристаллы бирюзового цвета, а при нагревании раствора выше 30° C получаются полупрозрачные зеленые кристаллы.
. Сульфат никеля токсичен. Соблюдайте технику безопасности, не трогайте его.
Шаг 7: Кристалл сегнетовой соли




Для выращивания этого кристалла нужно взять 130гр сегнетовой соли KNAC 4 H 4 O 6, вода, фильтровальная мозгобумага.
При выращивании этого кристалла нужно соблюдать постоянную температуру окружающей среды. Еще интересный факт об этом кристалле – он имеет пьезоэлектрические свойства, то есть вырабатывает электричество, не много, но вырабатывает.
Шаг 8: Кристалл из хромовых квасцов










Для получения раствора нужно взять 14.7гр K 2 Cr 2 O 7(0.05 моль) и смешать его с 12.5мл 4 МН 2 SO 4 (0.05 моль) и 100 мл дистиллированной воды. Далее сам раствор нужно слегка нагреть. Согласно реакциям стехиометрии нам нужно 0.15 моль СО 2, который можно из 0.3 молей Na 2 S 2 O 3 (52 г) и 0.15 молей H 2 SO 4 (около 40 мл). Тиосульфат натрия помещаем в генератор двуокиси серы, то есть колбу Эрленмейера, которая закрыта пробкой с отверстием для порционной подачи серной кислоты и отвода получаемого газа. Чтобы получить постоянный поток необходимого газа, колбу слегка подогреваем, а газ отводим посредством резиновой трубки.
Во время реакции температура раствора в колбе Эрленмейера не должна превышать 40 ° C, чтобы избежать побочных реакций, а чтобы не получить сложных соединений в растворе с выращиваемыми кристаллами колбу с раствором охлаждаем на ледяной бане.
После получения раствора сине-зеленого цвета оставьте его на некоторое время, когда появятся кристаллы выберите несколько вам понравившихся, остальные удалите. Таким образов получатся мозгокристаллы темно-фиолетового цвета.
. Хромовые квасцы токсичны, не пробуйте их !!
Формула реакции: K 2 Cr 2 O 7 + H 2 SO 4 + 3SO 2 → K 2 SO 4 + Cr 2 (SO 4 ) 3 + H 2O 2Na 2 S 2 O 3 + H 2 SO 4 → SO 2 + 2S + 2Na 2 SO 4 (сера из генератора диоксида) K 2 SO 4 + Cr 2 (SO 4 ) 3 + 12H 2 O → 2KCr (SO 4 ) 2 · 12H 2 O
Шаг 9: Кристалл из алюминиевых и хромовых квасцов




Квасцы имеют похожую структуру, поэтому можно смешать их и вырастить красивый кристалл. Чтобы получить светло-фиолетовый кристалл смешайте алюминиевые и хромовые квасцы и проведите процесс выращивания, а для получения двухцветного кристалла в мозгораствор квасцов положите кристалл уже выращенный из алюминиевых квасцов.
Шаг 10: Золотистые кристаллы



Pb (NO 3 ) 2 + 2Ki → PbI 2 + 2KNO 3 .
. Не трогайте и не пробуйте вещества этого опыта !!


Чтобы получить монокристаллы гидроксида магния необходимо смешать 8гр желатина с 200мл дистиллированной воды, это будет средой для мозгореакции. Далее в полученный ранее гель добавляем 2 мл 10% раствора MgCl 2 и встряхиваем до гомогенизации среды. Затем мерный цилиндр с гелем добавляем 5мл аммиака с концентрацией 5М. Сам процесс кристаллизации идет очень медленно, через несколько дней образуются небольшие белые кольца, а через две недели получаются кристаллы гидроксида магния.
MgCl 2 + 2 NH 4 OH → Mg (OH) 2 + 2NH 4 Cl
Шаг 12: Что делать с выращенными кристаллами
Выращенные кристаллы покройте осторожно и аккуратно прозрачным лаком, так кристалл перестанет расти и будет менее токсичен. Сами токсичные кристаллы можно использовать как наглядное пособие занимательной химии, а нетоксичные кристаллы как украшения.
Еще раз – соблюдайте технику безопасности при работе с химреагентами, и удачных вам мозгоопытов!

Аргоннская национальная лаборатория в 1980 придумала технологию ледяной гидросмеси (ice slurry), которая не образует ледяные наросты, не слипается, течет по трубам и в 5-7 раз эффективнее простой воды для охлаждения.
Д. Пайк предложил добавить в лед опилки и из этого композита (пайкерита) сделать… авианосец.
Чуток копнув, я узнал, насколько глубока ледяная кроличья нора.

Первопроходец в исследовании различных типов льда — Перси Уильямс Бриджмен, нобелевский лауреат по физике в 1946, он работал с высокими давлениями (до 10 ГПа), открыл/описал в 1912 году 5-6 видов льда.
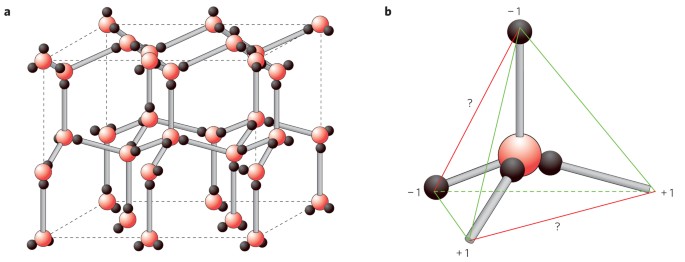

Шесть возможных молекулярных ориентаций центральной молекулы воды в пентамере Вальрафена.
Эксперименты с величиной и скоростью изменения температуры и давления, а так же хитрости с графеном позволяют играться со структурой и ориентацией протонов, что порождает 19 экспериментально полученных и несколько теоретических видов льда.
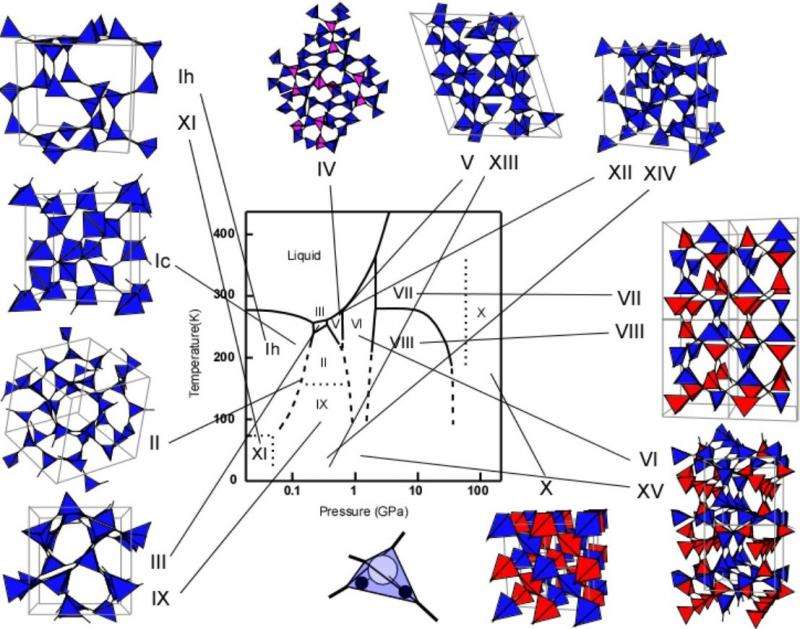
Фазовая диаграмма и структуры льда.

Сводная таблица 19 видов льда.
Лёд 0
Теоретическая структура. Лед-0 может получиться при кристаллизации льда Iси льда Ih из переохлажденной воды.
Аморфный лёд

Фазовая диаграмма аморфных льдов и жидкой воды.
Лёд-Iaили LDA (Low-density amorphous ice)
Лёд-Ia или HDA (High-density amorphous ice)
VHDA (Very-high density amorphous ice)
Аморфный лёд очень высокой плотности (2001) получают нагревом HDA до 160 К при давлении 1-2 ГПа.
Интересное видео, как лёд из одной фазы тает в другую:
Лёд Ih

Обычный гексагональный (hexagon, поэтому Ih) кристаллический лёд. Почти весь лёд на Земле относится ко льду Ih, и лишь малая часть — ко льду Iс (сubic).
Лёд Iс (1987)
Ромбовидное расположение воды во льду Iс
Лёд-Isd

Stacking disordered ice

Треугольная снежинка из Isd


Лёд 2 (1900)

Получают лёд-II, сжимая лёд Ih при температурах от −83 °C до −63 °C (190—210 K) и давлении 300 МПа, или путём декомпрессии льда V при температуре −35 °C (238 K). При нагреве лёд-II преобразуется в лёд-III.
Лёд 3

Можно получить при охлаждении воды до −23 °C (250 K) и давлении 300 МПа.
Лёд-III — наиболее просто получаемый и доступный для исследований лёд высокого давления. Впервые он был получен из обыкновенного льда при температуре −22 °C (температура тройной точки лёд Ih — лёд III — вода) путём повышения давления до 210 МПа
Лёд 4

Получают медленным нагревом (0,4 K/мин) аморфного льда высокой плотности от температуры 145 К при постоянном давлении 0,81 ГПа.
Лёд 5

Лёд-V производят охлаждением воды до 253 K (−20 °C) при давлении 500 МПа. Структура льда-V — самая сложная из всех фаз льда. Лёд V тает при 50 °С.
Лёд 6

Получают при охлаждении воды до −3 °C (270 K) и давлении 1,1 ГПа. В нём проявляется дебаевская релаксация. Лёд VI тает при температуре 81 ºС (355 K) при 2,216 ГПа и при температуре около 0 ºС при 0,6 ГПа.

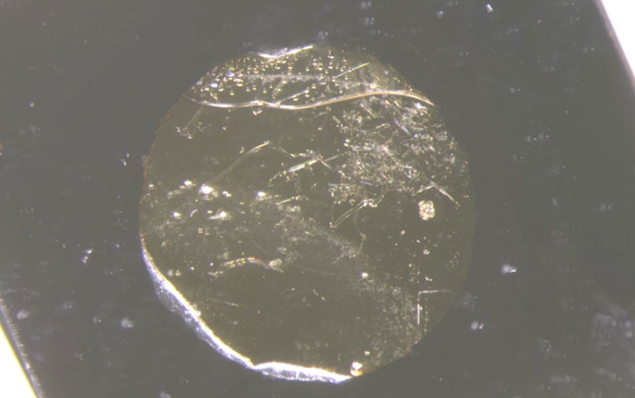
Монокристалл льда VI

Кристаллизация воды в тетрагональный лёд VI при комнатной температуре и давлении 0.9 ГПа.

Рост кристалла при трапецеидальном давлении.

Рост кристалла при синусоидальном давлении.
Лёд 7 (1969)
Самый неупорядоченный лёд, в нем не только атомы водорода, но и атомы кислорода не упорядочены.
Можно получить из воды под давлением 3 ГПа при охлаждении до комнатной температуры. Так же получается изо льда VI при увеличении давления при комнатной температуре.
Лёд 8

Упорядоченная версия льда-VII, в котором водород зафиксирован. Получается изо льда-VII при его охлаждении ниже 5 °C.
Лёд 9 (1973)
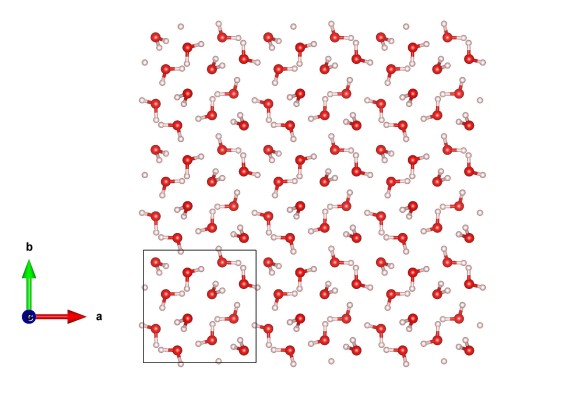
Лёд-IX — метастабильная форма твёрдой воды при температурах ниже 140 K и давлении 200-400 МПа. Получается изо льда III при охлаждении.
Лёд 10 (1984)
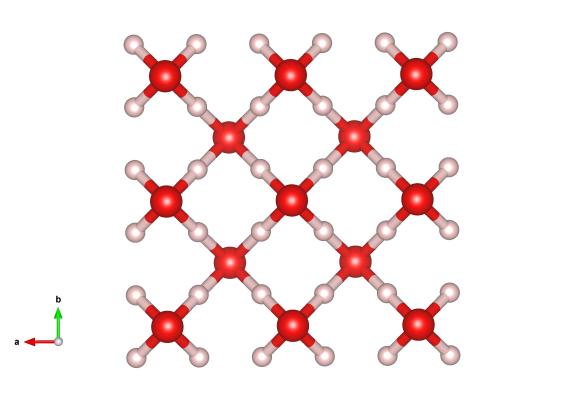
Симметричный лёд с упорядоченным расположением протонов. Образуется при давлениях около 70 ГПа.

Структура льда-X (слева верх) и предсказанные вариации Pbcm, Pbca, Cmcm.
Лёд 11 (1972)

Лёд-XI — это самая устойчивая конфигурация льда Ih с упорядоченной ориентацией протонов. Является сегнетоэлектриком (спонтанная поляризация, которую можно менять внешним электрическим полем).
Лёд 12 (2003)

Лед 13
Протонно-упорядоченная вариация льда-V. Получается при охлаждении воды до 130K при давлении 500 МПа.
Лёд 14 (2006)
Модификация льда-XII, где протоны расположены упорядоченно. Образуется при заморозке воды при температуре 118 K и давлении 1,2 ГПа.
Лед 15 (2009)

Лёд-XV — форма льда-VI с упорядоченными протонами, получается при охлаждении воды до 130 К при давлении 1 ГПа.

а) фазовая диаграмма льда с некоторыми маршрутами, используемыми для изучения упорядоченной формы льда и б) как молекула воды изменяется при переходе от неупорядоченной формы льда к упорядоченной.
Лёд 16 (2014)


Лёд-XVI имеет наименьшую плотность среди всех видов льда 0,81 г/см 3 , топологически эквивалентен КС-II (газовые гидраты). Получается путём удаления молекул газа из клатрата неона в вакууме при температуре ниже 147 К.

Фазовая диаграмма воды, расширенная до отрицательных давлений.
Лёд 17 (2015)
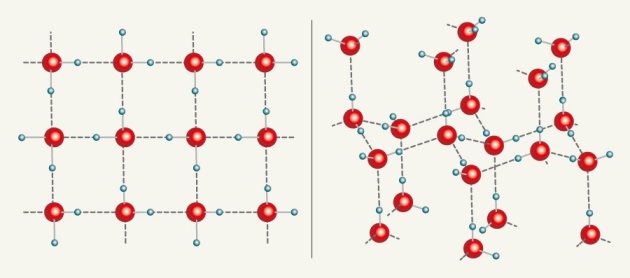
Квадратный лед получается если зажать воду между двумя слоями графена (1 нанометр) при комнатной температуре (Андрей Гейм подсчитал, что давление там примерно 10 000 атмосфер). Возможно, встречается в природе в трещинах камней и почвы.

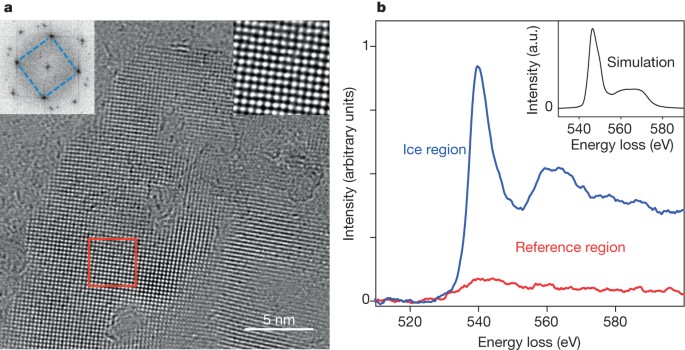
Лёд 18 (2019)

Супер-ионный лёд в четыре раза плотнее обычного льда и обладает электропроводимостью.
Лед-XVIII или суперионная вода может существовать при очень высоких давлениях 50-100 ГПа (удар лазерного импульса в ячейке с алмазными наковальнями) и температуре. Молекулы распадаются на ионы. Ионы кислорода формируют гранецентрированную кубическую решетку, а ионы водорода хаотично диффундируют внутри нее.
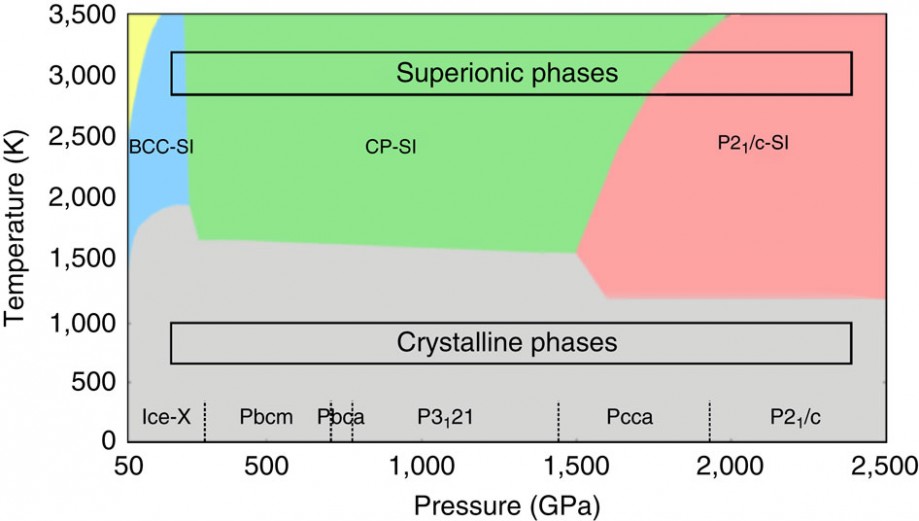
Фазовая диаграмма супер-ионного льда: объёмно-центрированный ионный лёд (синий), гранецентрированный/плотноупакованный (зелёный) и ионный лёд P21/c. Серый — кристаллический лед, жёлтый — область ионной жидкости.
Лед 19 (2021)
Различия в дифракционных картинах и строении кристаллической решетки льда-VI и льда-XIX
Если ко льду-VI применить давление от 0,88 до 2,20 гигапаскалей, то образуется лед-XV, и новый лед-XIX. Если проанализировать диэлектрическую проницаемость и нейтронную дифракцию, то придем к выводу о самостоятельности новой фазы.
Читайте также:

