Как сделать из этина этаналь
Обновлено: 02.07.2024
Сайт учителя химии и биологии МБОУ СОШ №2 с.Казаки Елецкого р-на Липецкой обл. Радиной М.В.
При окислении этанола образуется этаналь (уксусный альдегид) и далее этановая кислота (уксусная кислота). Сильные окислители сразу превращают этаналь в уксусную кислоту. К тому же результату приводит и окисление кислородом воздуха под влиянием бактерий. Мы легко сможем убедиться в этом, если немного разбавим спирт и оставим его на некоторое время в открытой чашке, а затем проверим реакцию на лакмус. Для получения столового уксуса до сих пор используют, в основном, уксуснокислое брожение спирта или низкосортных вин (винный уксус).
Для этого спиртовый раствор при интенсивной подаче воздуха медленно пропускают через опилки из буковой древесины. В продажу поступает 5 % или 30 %-ный столовый уксус или так называемая уксусная эссенция, содержащая 40% уксусной кислоты. Для большинства опытов она нам подойдет. Лишь в некоторых случаях понадобится безводная (ледяная) уксусная кислота, которая относится к числу ядов. Ее можно купить в аптеке или магазине химических реактивов. Она уже при 1,6 °С затвердевает в кристаллическую массу, похожую на лед. Синтетическим путем уксусную кислоту получают из этина через этаналь.
Неоднократно упоминавшийся этаналь, или уксусный альдегид,— важнейший промежуточный продукт в химической технологии, основанной на использовании карбида кальция. Его можно превратить в уксусную кислоту, спирт или же в бутадиен — исходное вещество для получения синтетического каучука. Сам этаналь производится в промышленности путем присоединения воды к этину. В Германии на комбинате синтетического бутадиенового каучука в Шкопау этот процесс осуществляется в мощных реакторах непрерывного действия.
Сущность процесса заключается в том, что этин вводится в нагретую разбавленную серную кислоту, в которой растворены катализаторы — соли ртути и другие вещества. Поскольку соли ртути очень ядовиты, мы не будем сами синтезировать этаналь из этина. Выберем более простой способ — осторожное окисление этанола.
Нальем в пробирку 2 мл спирта (денатурата) и добавим 5 мл 20 %-ной серной кислоты и 3 г тонкоизмельчениого бихромата калия. Затем быстро закроем пробирку резиновой пробкой, в которую вставлена изогнутая стеклянная трубка. Смесь нагреем малым пламенем до кипения и выделяющиеся при этом пары пропустим через ледяную воду. Образующийся этаналь растворяется в воде, и его можно обнаружить с помощью описанных выше реакций для определения алканалей. Кроме того, раствор проявляет кислую реакцию, потому что окисление легко идет дальше с образованием уксусной кислоты.
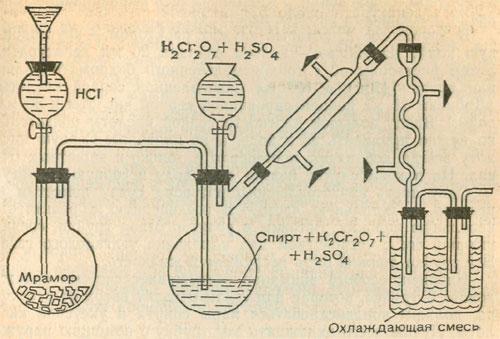
Чтобы получить этаналь в больших количествах и более чистым, соберем, руководствуясь рисунком, более сложную установку. Однако этот опыт можно выполнять только в кружке или при наличии у читателя большого опыта. Этаналь ядовит и очень летуч!
Левая часть установки предназначена для пропускания тока диоксида углерода (углекислого газа). Последний необходим для удаления выделяющегося этаналя из сферы реакции, прежде чем он окислится дальше до уксусной кислоты. Поместим в колбу кусочки мрамора и будем добавлять к ним малыми порциями разбавленную соляную кислоту. Для этого нужна капельная воронка с длинной отводной трубкой (не менее 25 см). Можно плотно присоединить такую трубку и к обычной капельной воронке с помощью резинового шланга. Эта трубка должна быть все время заполнена кислотой, чтобы углекислый газ мог преодолеть избыточное сопротивление последующей части установки и не выходил в обратном направлении.
В другой сосуд, который служит реактором,— круглодонную колбу на 250 мл — нальем сначала 20 мл денатурата. Затем растворим 40 г тонкоизмельченного бихромата калия или натрия (Яд!) в 100 мл разбавленной серной кислоты. Добавим 20 мл концентрированной серной кислоты к 80 мл воды. Ввиду большей плотности серной кислоты обязательно нужно приливать ее к воде, а не наоборот.
Серную кислоту всегда добавляют постепенно и только в защитных очках. Ни в коем случае нельзя лить воду в серную кислоту!
Одну треть приготовленного раствора сразу поместим в реактор, а остальную часть — в соединенную с реактором капельную воронку. Вставим в реактор отвод трубки, соединяющей его с устройством для выделения углекислого газа. Эта трубка должна быть погружена в жидкость.
Наконец, особого внимания заслуживает система охлаждения. В трубке, которая под углом отходит вверх от реактора, должны конденсироваться пары спирта и уксусной кислоты. Лучше всего охлаждать эту трубку с помощью наружного свинцового змеевика, пропуская через него проточную воду. В крайнем случае, можно обойтись без охлаждения, но тогда мы получим более грязный продукт.
Для конденсации этаналя, который кипит уже при 20,2 °С, используем прямой холодильник. Желательно, конечно, взять эффективный холодильник — змеевиковый, шариковый или с внутренним охлаждением. В крайнем случае подойдет и не слишком короткий холодильник Либиха. В любом случае охлаждающая должна быть очень холодной. Водопроводная вода годится для этого только зимой.
В другое же время года можно пропускать ледяную воду из большого бака, установленного на достаточной высоте. Приемники — две соединенные друг с другом пробирки — охладим, погрузив их в охлаждающую смесь из равных (по массе) количеств измельченного льда или снега и поваренной соли. Несмотря на все эти меры предосторожности, пары этаналя все же частично улетучиваются. Так как этаналь имеет неприятный резкий запах и ядовит, опыт нужно проводить в вытяжном шкафу или на открытом воздухе.
Только теперь, когда установка заряжена и собрана, начнем опыт. Вначале проверим работу прибора для выделения газа, приливая к мрамору малое количество соляной кислоты. При этом установка сразу же заполняется углекислым газом.
Можно использовать и капельную воронку без длинной отводной трубки. В этом случае в пробку, закрывающую колбу с мрамором, нужно вставить еще одну короткую стеклянную трубку. Такую же трубку вставим в пробку, закрывающую капельную воронку, и соединим обе трубки резиновым шлангом. Еще удобнее пользоваться аппаратом Киппа.
Если он наверняка проходит через реактор и никаких неплотностей не обнаруживается, приступим собственно к получению этаналя.
Приостановим выделение газа, включим всю систему охлаждения и нагреем содержимое реактора до кипения. Поскольку теперь при окислении спирта выделяется тепло, горелку можно убрать. После этого снова будем постепенно добавлять соляную кислоту, чтобы через реакционную смесь все время проходил умеренный ток углекислого газа. Одновременно оставшийся раствор бихромата должен медленно поступать из капельной воронки в реактор.
По окончании реакции в каждом из двух приемников содержится по несколько миллилитров почти чистого этаналя. Заткнем пробирку ватой и сохраним для следующих опытов на холоду. Длительное хранение этаналя нецелесообразно и опасно, так как он слишком легко испаряется и, находясь в склянке с притертой пробкой, может с силой выбивать пробку. В продажу этаналь поступает только в запаянных толстостенных стеклянных ампулах.
Вещество представляет собой бесцветную жидкость с резким запахом, хорошо растворяется в воде, спирте, эфире. Из-за очень низкой температуры кипения (20.2°С) хранят и перевозят ацетальдегид в виде тримера - паральдегида, из которого он может быть получен нагреванием с минеральными кислотами (обычно серной).
Химические свойства
Для уксусного альдегида характерны реакции альдегидов.
Получение
Получают уксусный альдегид гидратацией ацетилена в присутствии солей ртути (реакция Кучерова) или окислением этилового спирта.
Применение
Применяют уксусный альдегид для получения уксусной кислоты, бутадиена, некоторых органических веществ, альдегидных полимеров.
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое "Этаналь" в других словарях:
ЭТАНАЛЬ — (ацетальдегид, СН3СНО), бесцветная летучая и горючая жидкость, получаемая путем каталитического окисления этена или этанола либо каталитической гидратации этина (ацетилена). Используют в основном для получения других органических соединений.… … Научно-технический энциклопедический словарь
этаналь — сущ., кол во синонимов: 1 • ацетальдегид (2) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
этаналь — см. Уксусный альдегид … Большой медицинский словарь
уксусный альдегид — (син.: ацетальдегид, этаналь) простейший природный альдегид ациклического ряда, промежуточный продукт спиртового брожения; участвует в цикле трикарбоновых к т; производные У. а. применяются в качестве лекарственных средств … Большой медицинский словарь
АЛЬДЕГИД — АЛЬДЕГИД, вещество из класса органических соединений, для которого характерна группа СНО. Простейшим примером является МЕТАНАЛЬ (НСОН), который в виде водного раствора используется как консервант, а также применяется при производстве некоторых… … Научно-технический энциклопедический словарь
АЦЕТАЛЬДЕГИД — АЦЕТАЛЬДЕГИД, см. ЭТАНАЛЬ … Научно-технический энциклопедический словарь
ОКСИМЫ — ОКСИМЫ, в органической химии соединение, образующееся между гидроксиламином и АЛЬДЕГИДОМ или КЕТОНОМ. Оксимы являются продуктами конденсации (см. РЕАКЦИЯ КОНДЕНСАЦИИ), содержащими группу C=NOH. Используются в качественном анализе для определения… … Научно-технический энциклопедический словарь
ПАРАЛЬДЕГИД — (тример этаналя, С6Н12О3), бесцветная жидкость, образующаяся при ПОЛИМЕРИЗАЦИИ ЭТАНАЛЯ (ацетальдегида) под действием СЕРНОЙ КИСЛОТЫ. При нагревании в присутствии разбавленных кислот снова превращается в этаналь. Имеет приятный запах, но… … Научно-технический энциклопедический словарь
ЭТИН — (ацетилен, СНСН), бесцветный горючий газ, простейший из АЛКИНОВ, получаемый посредством КРЕКИНГА фракций нефти. В смеси с воздухом ацетилен взрывоопасен. При сжигании в присутствии кислорода ацетилен дает очень высокие температуры, до 3480 °С,… … Научно-технический энциклопедический словарь
У́ксусный альдеги́д — (син.: ацетальдегид, этаналь) простейший природный альдегид ациклического ряда, промежуточный продукт спиртового брожения; участвует в цикле трикарбоновых кислот; производные У. а. применяются в качестве лекарственных средств … Медицинская энциклопедия

*Цитирирование задания со ссылкой на учебник производится исключительно в учебных целях для лучшего понимания разбора решения задания.
Похожие решебники


Популярные решебники 10 класс Все решебники







Главная задача сайта: помогать школьникам и родителям в решении домашнего задания. Кроме того, весь материал совершенствуется, добавляются новые сборники решений.

C2H2 + H2O [H2SO4, Hg2 + ] = H3C - CHO (гидратация ацетилена).

Осуществить цепочку превращения метан - ацетилен - этаналь - этанол?
Осуществить цепочку превращения метан - ацетилен - этаналь - этанол.

Как получить глицерин, исходя из : ацетилена?
Как получить глицерин, исходя из : ацетилена.

Помогите пожаааааалуйста Из 61, 6л ацетилена(н?
Помогите пожаааааалуйста Из 61, 6л ацетилена(н.
У. ) получено реакцией гидратации 72, 6г этаналя.
Какова объемная доля примесей(φприм.

Какую массу этаналя можно получить гидратацией 11, 2л ацетилена, если доля выхода продукта составляет 80% от теоретически возможного?
Какую массу этаналя можно получить гидратацией 11, 2л ацетилена, если доля выхода продукта составляет 80% от теоретически возможного?

Срочно?
При брожении глюкозы получен этанол массой 55, 2 определить массу глюкозы подвергается брожению.
При взаимодействии 14г ацетилена с водой был получен этаналь.
Определите выход этаналя в граммах.

Помогите решить цепочку превращений : метан - - - - ацетилен - - - - этаналь - - - - уксусная кислота?
Помогите решить цепочку превращений : метан - - - - ацетилен - - - - этаналь - - - - уксусная кислота.

Как осуществить превращения : карбид кальция - ацетилен - этаналь - уксусная кислота - метилацетат?
Как осуществить превращения : карбид кальция - ацетилен - этаналь - уксусная кислота - метилацетат?

Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : метан - ацетилен - этаналь - этанол - этилен - этаналь?
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : метан - ацетилен - этаналь - этанол - этилен - этаналь.

Написать цепочку превращений : метан - ацетилен - этаналь - бромэтан - этен - этанол - этаналь - уксусная кислота - ацетат натрия?
Написать цепочку превращений : метан - ацетилен - этаналь - бромэтан - этен - этанол - этаналь - уксусная кислота - ацетат натрия.

К непридельным углеводородам относятся : 1)этаналь, пропен, ацетилен ; 2)ацетилен, этилен, пентадиен ; 3)бензол, циклогексан, фенол ; 4)этин, пропан, этаналь?
К непридельным углеводородам относятся : 1)этаналь, пропен, ацетилен ; 2)ацетилен, этилен, пентадиен ; 3)бензол, циклогексан, фенол ; 4)этин, пропан, этаналь.
Вопрос Как можно получить этаналь , исходя из ацетилена ?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 10 - 11 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.

Запишем уравнение реакции CuSO4 + 2 NaOH = Cu(OH)2 + Na2SO4 Белый осадок - этоNa2SO4. Посчитаем число моль сульфата натрия. Оно равно 11, 8 / (M(Na) * 2 + M(S) + M(O) * 4) = 11. 8 / 140. Значит, было 11. 8 / 140 * 2 моль шидроксида натрия ( * 2 ..

CаСО3 - карбонат кальция, нерастворимая средняя соль угольной кислоты. При температуре выше 900°С разлагается : СаСО3 = СаО + СО2↑ При взаимодействии с кислотами, вытесняется слабая угольная кислота, которая разлагается на воду и диоксид углерода : ..

Ba (0) + H ( + ) N ( + 5) O3 ( - 2) — Ba ( + 2) + N ( + 4) O3 ( - 2) + N ( + 4) O2 ( - 2) + H2 ( + ) O ( - 2) Ba (0) - 2ē — Ba ( + 2) восстановитель N ( + 5) - 1ē — N ( + 4) окислитель Расставляем коэффициенты : Ba + 4HNO3 — Ba(NO3)2 + 2NO2 + 2H2O.

1) 2NaOH + SO2 - > Na2SO3 + H2O NaOH + HCl - > NaCl + H2O Ответ : А, В 2) FeSO4 + 2KOH - > Fe(OH)2 + K2SO4 Ответ : Г.

1. А) 2NaOH + SO2 = Na2SO3 + H2O В) NaOH + HCl = NaCl + H2O 2. Г) FeSO4 + 2KOH = K2SO4 + Fe(OH)2↓.

5) 3 6) 2 7) 1)нет 2)нет 3)да 4)нет 5)да 6)да.

Фтор (F) заряд атома 9. Значит в атоме 9 электронов и 9 протонов.

Вот решение ответ : n = 0, 36 моль.

В пеоаом аопросе 1, 3.

P - 2 H2O - 5 P2O5 - 1 H2 - 5 2P + 5H2O = P2O5 + 5H2.
© 2000-2022. При полном или частичном использовании материалов ссылка обязательна. 16+
Сайт защищён технологией reCAPTCHA, к которой применяются Политика конфиденциальности и Условия использования от Google.
Читайте также:

