Катализатор фишера тропша своими руками
Добавил пользователь Skiper Обновлено: 08.09.2024
Процесс получения углеводородов на основе оксида углерода и водорода на железных и кобальтовых катализаторах разработан в 1923 году Фишером и Тропшем.
Химизм процесса
Получение углеводородных смесей из оксида углерода и водорода представляет собой комплекс сложных параллельных и последовательных реакций. Первой стадией процесса является совместная хемосорбция оксида углерода и водорода на поверхности катализатора, в результате чего образуется первичный поверхностный комплекс. В результате дальнейшего ступенчатого присоединения углеводородных фрагментов происходит рост углеводородной цепи. Основные направления процесса можно представить схемой:
Таким образом в результате синтеза образуется смесь парафиновых и олефиновых углеводородов, воды и СО2.
Синтез Фишера-Тропша протекает в присутствии катализаторов, содержащих металлы VIII группы Периодической системы – никель, кобальт, железо с добавками оксидов некоторых других металлов (тория, магния, циркония, титана). Выход и состав продуктов реакции определяется видом катализатора и условиями проведения процесса. Реакция является экзотермической. Помимо образования углеводородов в процессе синтеза в небольших количествах получаются органические кислородсодержащие соединения, главным образом спирты С1-С6. Промышленные катализаторы современного процесса Фишера-Тропша часто состоят из железа, нанесенного на оксид алюминия, диоксид кремния или кизельгур, и содержат в качестве промоторов соли щелочных металлов.
Применяют также Со-катализаторы, в качестве носителей осажденных кобальтовых катализаторов применяют природные и синтетические алюмосиликаты и цеолиты. На кобальтовых катализаторах образуются смеси, состоящие преимущественно из парафиновых углеводородов нормального строения (80%) с примесью нормальных алкенов (15%) с числом атомов углерода 1-100 и небольшого количества разветвленных алканов, алкенов и кислородсодержащих соединений (5%). Процесс протекает при температуре 170-200 о С и давлении 0,1-1,0 МПа. В присутствии железных катализаторов синтезы углеводородов из оксида углерода и водорода осуществляются в более жестких условиях: температуре в реакторе 200-235 о С, давлении 3-4 МПа. В результате образуются углеводородные смеси с большим содержанием олефинов (до 50%) и кислородсодержащих соединений.
Одной из нежелательных побочных реакций является диспропорционирование оксида углерода:
что приводит к отложению углерода на поверхности катализатора и часто является причиной дезактивации последнего.
Дизельное топливо можно получать как в ходе синтеза Фишера-Тропша непосредственно, так и в результате крекинга образующихся в процессе углеводородов выше С19 и олигомеризации алкенов С3-С8. Бензины, получаемые на железных катализаторах, имеют лучшие моторные характеристики, чем бензины, производимые на кобальтовых катализаторах. Однако при применении кобальтовых катализаторов образуется много дорогостоящих высокомолекулярных восков, что улучшает экономические показатели процесса.
Основным недостатком ФТ- синтеза является его низкая селективность. Смесь продуктов, полученная этим методом, включает 25-30% метана, 15-20% углеводородов С2-С4 и только 24-45% жидких углеводородов. Одной из важнейших проблем при совершенствовании процесса является организация переработки в топливные фракции или другие ценные продукты образующихся легких углеводородов. К недостаткам процесса следует также отнести дороговизну катализаторов, сложность их регенерации, низкую производительность.
Технологическое оформление процесса
В промышленности реализованы: технология в стационарном слое катализатора, в потоке взвешенного катализатора, в жидкой фазе с суспендированным катализатором.

Принципиальная технологическая схема высокопроизводительного синтеза Фишера-Тропша на железном катализаторе.
1 – реактор; 2 – мультициклон; 3 – теплообменник; 4 – конденсатор; 5 – сборник парафина; 6 – сборник высококипящих угледоводоров; 7 – сборник легких углеводородов; 8 – сборник реакционной воды.
Потоки: I – синтез-газ; II – питательная вода; III – пар; IV – циркулирующий газ; V – остаточный газ; VI – щелочь.
Исходный синтез-газ смешивают в соотношении 1:2,5 с циркулирующим газом, компримируют до 2,5 МПа и через теплообменник вводят в реактор в количестве 500-700 куб. м. на 1 куб м. катализатора в час. В реактор загружают 40 куб. м. железного катализатора. Катализатор работает непрерывно в течение 9-12 месяцев с постепенным повышением температуры с 220 до 250 о С, обеспечивая конверсию синтез-газа 65-73%. Производительность одного реактора – 250 т./сут. углеводородов С2 и выше.
В реакторах этого типа получают в основном насыщенные углеводороды, в том числе и высокомолекулярные твердые парафины типа церезина.
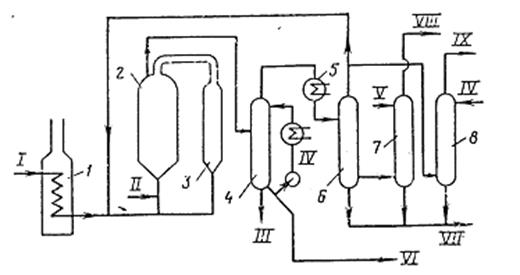
Принципиальная технологическая схема синтеза Фишера-Тропша в газовой фазе в потоке взвешенного катализатора.
1 – подогреватель; 2 – реактор; 3 – холодильник; 4 – колонна-сепаратор; 5 – конденсатор; 6 – разделительная колонна; 7 – колонна для промывки бензина; 8 – колонна для промывки газа.
Потоки: I – синтез-газ; II – ввод свежего катализатора; III – суспензия катализатора; IV – циркулирующее масло; V – вода; VI – вода и водорастворимые продукты; VII – тяжелое масло; VIII – бензин; IX – отходящий газ.
Синтез-газ вводят в реактор вместе с катализатором. Синтез проводят при температуре 310-350 о С и давлении 2-3 МПа. Продукты реакции и катализатор поступают в колонну-сепаратор, оборудованную циклонами для отделения катализатора. Отвод тепла осуществляют при помощи двух холодильников, через которые циркулирует масло. Срок службы катализатора 42-45 суток.
В смесях, получаемых в реакторах со взвешенным слоем катализатора, может содержаться значительное количество ценных побочных продуктов – кислородсодержащих соединений (спирты, карбоновые кислоты, альдегиды, кетоны).
ПРОИЗВОДСТВО МЕТАНОЛА
Метанол является ценным крупнотоннажным продуктом, находящим широкое применение в различных отраслях промышленности.
Объем потребления метанола в мире непрерывно возрастает. В настоящее время его мировое производство превышает 20 млн. т/год.
Традиционным потребителем метанола является производство формальдегида (в первую очередь, его водного раствора - формалина), который получают окислительной конверсией метанола. На долю формальдегида приходится половина производимого метанола.
Потребителями метанола являются производства различных мономеров (например, метилметакрилата и диметилтерефталата), метилтретбутилового эфира (МТБЭ), метилгалогенидов, метиламинов, ионообменных смол, уксусной кислоты. Метанол также широко используется как растворитель и экстрагент.
Одной из новых областей применения метанола является использование его в качестве моторного топлива взамен ставшего дефицитным и весьма дорогим бензина.

Метанол либо добавляют к бензину в количестве до 5%, либо используют целиком вместо бензина. Однако метанол обладает более низкой теплотворной способностью и является весьма токсичным, что, вероятно, будет сдерживать его применение.
Метанол – ядовитая бесцветная жидкость со сладковатым запахом.
Метанол в числе других кислородсодержащих соединений впервые был получен из оксида углерода и водорода в 1913 г. Для этой цели использовали железные катализаторы, которые однако быстро покрывались углеродом и дезактивировались. Применение цинк-хромовых катализаторов позволило устранить этот недостаток. Было установлено, что оксид цинка не чувствителен к сере, соединения которой обычно содержатся в синтез-газе и отравляют металлические катализаторы.
Реакция образования метанола идет с выделением тепла и уменьшением объема, поэтому ей благоприятствуют низкие температуры и высокие давления. При синтезе метанола протекают следующие реакции:
С повышением температуры степень превращения СО заметно снижается.
Условия проведения реакции определяются катализатором. Если катализатор обладает такой высокой активностью, что уже при низкой температуре достигается высокая степень превращения СО, то синтез метанола можно осуществлять уже при давлении 5 МПа. В противном случае, то есть при применении менее активного катализатора, работающего при более высокой температуре, необходимо давление ~30 МПа. Катализаторы, обычно применяемые в промышленности, проявляют активность только при высоких температурах (360-380 о С), т.е. в условиях термодинамически неблагоприятных. В промышленности наибольшее распространение получили цинк-хромовые катализаторы, а в последние годы – медьсодержащие катализаторы, достаточно активные при температуре 220-270 о С.
При управлении селективностью синтеза метанола необходимо учитывать, что протекание этой реакции гораздо менее термически благоприятно, чем протекание таких побочных реакций, как образование углеводородов, высших спиртов, диметилового эфира. Эти реакции можно подавить варьированием состава катализатора.
В зависимости от применяемых катализаторов (а, следовательно, условий синтеза) различают два варианта превращения синтез-газа в метанол: синтезы при высоком и низком давлении.
При высоком давлении применяют катализаторы на основе оксида цинка, характеризующиеся низкой чувствительностью к сере, промотированные оксидами хрома (межкристаллический промотор – располагающийся вне кристаллической решетки ZnO) или оксидами железа, кальция, магния (внутрикристаллические промоторы – располагающиеся внутри кристаллической решетки ZnO).
Реакторы высокого давления представляют собой цельнокованные аппараты колонного типа, для эффективного теплоотвода используют реакторы полочного типа с промежуточным вводом холодного газа и выносным или встроенным теплообменником. Обычное число полок 5-6, для пуска агрегата применяют встроенный электронагреватель или специальную трубчатую печь.
Наиболее эффективными каталитическими системами, работающими при низком давлении, являются медьсодержащие оксидные катализаторы. Однако медьсодержащие катализаторы отличаются высокой чувствительностью к примесям сернистых соединений, почти всегда содержащимся в синтез-газе. Если при синтезе на цинк-хромовых катализаторах допустимо содержание сероводорода в синтез-газе выше 100 ррm, то для медных катализаторов этот показатель не может превышать 1 ppm.
При низком давлении используют полочные реакторы, аналогичные тем, что применяются при высоком давлении, или реакторы трубчатого типа, в которых катализатор загружен в трубки, а тепло реакции отводится кипящей водой, циркулирующей в межтрубном пространстве реактора и связанной с паросборником, так как при съеме тепла генерируется водяной пар. При использовании трубчатого реактора не требуется пусковой нагреватель, реактор в пусковой период разогревается водяным паром из сети, что является преимуществом реактора этого типа. В то же время достоинством полочного реактора является простота конструкции и легкость загрузки и выгрузки катализатора.
Природный газ отделяют от тяжелых углеводородов и компримируют в турбокомпрессоре 1 до 2,5 МПа, после чего направляют на очистку и далее в блок конверсии метана 3. Туда же поступает водяной пар. К метану добавляют небольшое количество СО2. Конверсия метана осуществляется при температуре 850—860 °С. После печей конверсии синтез-газ поступает в котел-утилизатор 4, где генерируется пар высокого давления (12 МПа), который затем перегревается и поступает на турбины — привод компрессоров 1 и 11. Если конверсии подвергают тяжелое жидкое сырье, то блок очистки располагается после конверсии, а необходимость в компрессоре 1 отпадает. В последнем случае конверсию проводят при давлении 5,8 МПа, а синтез-газ после очистки не нуждается в дополнительной компрессии и поступает в циркуляционный компрессор 11.
Синтез-газ, полученный из природного газа, направляют на доохлаждение с целью конденсации воды. Далее синтез-газ дожимается в турбокомпрессоре 12 до 5—5,5 МПа, смешивается с циркуляционным газом и через теплообменник 6, обогреваемый горячим реакционным газом, поступает в два параллельно работающих реактора синтеза метанола 7.
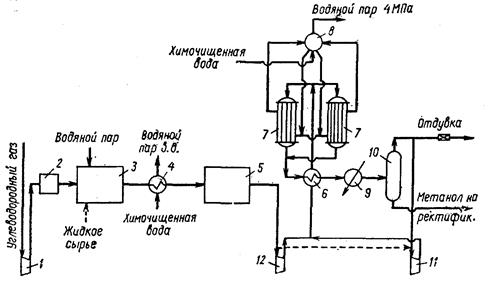
Технологическая схема синтеза метанола под низким давлением:
1,11,12— компрессоры; 2 — блок очистки; 3-блок конверсии метана; 4 - котел-утилизатор; 5 — блок очистки и доохлаждення синтез-газа; 6- теплообменник; 7 — реакторы синтеза метанола; 8—паросборник; 9 - холодильник; 10— газосепаратор в. д.
Реакторы трубчатого типа охлаждаются циркулирующей в межтрубном пространстве водой. Пар направляется в паросборник 8 , куда подается и химически очищенная вода. Конденсат из паросборника вновь поступает в реакторы 7, а водяной пар высокого давления направляется на перегрев и используется в турбинах. Продукты реакции направляются через теплообменник 6 , где отдают свое тепло синтез-газу, в конденсатор-холодильник 9 и в газосепаратор 10 для отделения метанола от циркуляционного газа. Последний поступает на прием циркуляционного компрессора 11 и вновь направляется в систему синтеза. Часть газа отдувают для удаления поступающих в систему инертных примесей (главным образом метана и азота). Метанол-сырец из газосепаратора 10 направляется на ректификацию.
Синтез углеводородов из СО и Н2 на гетерогенных катализаторах (синтез Фишера-Тропша) в настоящее время рассматривается как реальная альтернатива их получению из нефти.

Нефть является единственным глобальным сырьем для производства моторных топлив и важнейшим - для химического синтеза. Однако постепенно ситуация изменяется. Исчерпание мировых запасов нефти вынуждает обратиться к другим источникам углеводородного сырья, наиболее значительными из которых являются уголь и природный газ. Извлекаемые запасы газа в энергетическом эквиваленте превышают нефтяные в 1,5 раза, запасы угля - более чем в 20 раз [2, 3]. По экспертным оценкам, к 2015 г. доля нефти в мировом энергетическом балансе будет составлять 38 %, природного газа - 26 %, угля - 25 % [4].
Первой стадией превращения природного газа и угля в химические продуты и жидкие топлива является их конверсия в синтез-газ -смесь СО и Н2. Далее основные направления переработки синтез-газа выглядят следующим образом:
• синтез метанола;
• производство аммиака;
• оксо-синтез и формилирование ароматических соединений;
• карбонилирование метанола в уксусную кислоту;
• карбоксилирование олефинов;
• синтез Фишера-Тропша (ФТ).
Надо отметить, что получение синтез-газа (паровой конверсией или парциальным окислением метана, газификацией угля) является наиболее дорогой составляющей всего производства. Капитальные затраты на секцию синтез-газа в строительстве завода по получению метанола из природного газа или углеводородов по технологии ФТ из угля составляют 60-70 % 5.
Синтез Фишера-Тропша (ФТ) представляет собой сложную совокупность последовательных и параллельных превращений, протекающих на поверхности гетерогенного катализатора. Основными являются реакции гидрополимеризации СО с образованием парафинов и олефинов:
nCO + 2nH2 CnH2n + H2O, nCO + (2n + 1)H2 н> CnH 2 n + 2 + H2O. В присутствии железных катализаторов образуются также значимые количества оксигенатов - спиртов, альдегидов, кетонов и карбоновых кислот. При повышенных температурах в присутствии цеолитных сокатализаторов образуются ароматические соединения. Побочные реакции - прямое гидрирование СО в метан, диспропорционирование СО (реакция Белла-Будуара) и реакция водяного газа, интенсивно протекающая на железных катализаторах:
Максимальный теоретически возможный выход углеводородов из 1 нм3 синтез-газа состава СО:Н2 = 1:2 составляет 208 г.
В условиях синтеза ФТ термодинамические вероятности образования продуктов выглядят следующим образом [8]:
• метан > алканы > алкены > О-содержащие;
• низкомолекулярные н-алканы > высокомолекулярные н-алканы;
- высокомолекулярные н-олефины > низкомолекулярные н-олефины.
В действительности выход метана на хороших катализаторах синтеза ФТ не превышает 8 %. Молекулярно-массовое распределение диктуется кинетикой полимеризации (см. ниже). Таким образом, синтез ФТ является кинетически контролируемым процессом, состав конечных продуктов далек от равновесного.
Синтез ФТ - сильно экзотермический процесс. Тепловой эффект реакции гидрополимеризации СО составляет 165 кДж/моль СО, тепловой эффект прямого гидрирования еще выше - 215 кДж/моль. Отвод большого количества тепла в ходе синтеза представляет собой важнейшую проблему при проектировании промышленных установок синтеза ФТ. Катализаторами реакции являются металлы VIII группы. Наибольшую каталитическую активность проявляют Ru, Fe, Co, Ni. Рутений активен уже при 100 °С, в его присутствии при повышенном давлении образуются парафины очень высокой молекулярной массы (полиметилен). Однако этот металл слишком редок и дорог, чтобы рассматриваться в качестве промышленного катализатора. Никелевые контакты при атмосферном давлении обеспечивают в основном прямое гидрирование СО в метан. При повышенном же давлении легко образуется летучий Ni(CO)4, так что катализатор вымывается из реактора. В силу этих причин коммерчески использовались только железные и кобальтовые каталитические системы.
Кобальтовые катализаторы были первыми катализаторами, используемыми в промышленности (в Германии, а затем во Франции и Японии в 1930-1940-е годы) [8]. Типичными для их работы являются давление 1-50 атм и температура 180-250 °С. В этих условиях образуются, главным образом, линейные парафины. Кобальт обладает значительной гидрирующей активностью, поэтому часть СО неизбежно превращается в метан. Эта реакция резко ускоряется с повышением температуры, поэтому кобальтовые катализаторы не могут использоваться в высокотемпературном процессе ФТ. По последним данным, удельная активность кобальтовых катализаторов выше, чем железных [9].
Железные катализаторы с середины 1950-х годов используются на заводах синтеза ФТ в ЮАР [8, 10]. По сравнению с кобальтовыми они гораздо более дешевы, работают в более широком интервале температур (200-360 °С), и позволяют получать более широкий спектр продуктов: парафины, низшие α-олефины, спирты. В условиях синтеза ФТ железо катализирует реакцию водяного газа, что позволяет эффективно использовать получаемый из угля синтез-газ, в котором соотношение СО:Н2 ниже стехиометрического 1:2. Железные катализаторы имеют более низкое сродство к водороду по сравнению с кобальтовыми, поэтому метанирование не является для них большой проблемой. Однако в силу той же низкой гидрирующей активности поверхность железных контактов быстро зауглероживается, и срок их службы составляет несколько недель. Кобальтовые контакты, напротив, способны работать без регенерации год и более. Еще одним недостатком железных контактов является их ингибирование водой. Поскольку вода является продуктом синтеза, кинетика процесса для железных катализаторов неблагоприятна, конверсия СО за один проход невысока. Для достижения высокой степени превращения необходимо организовывать рецикл газа [3].
И железные, и кобальтовые катализаторы крайне чувствительны к отравлению серой. Поэтому синтез-газ должен быть предварительно очищен от серы, по крайней мере, до уровня 2 мг/м 3 [11]. Остаточная сера адсорбируется поверхностью катализатора, так что в итоге продукты синтеза ФТ практически ее не содержат. Это обстоятельство делает синтетическое дизтопливо, полученное по технологии ФТ, весьма привлекательным ввиду современных жестких экологических требований к транспорту.
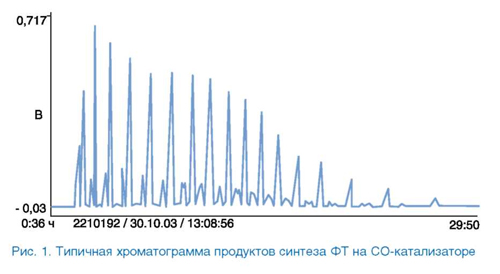
В синтезе ФТ образуется широкая углеводородная фракция (рис. 1).
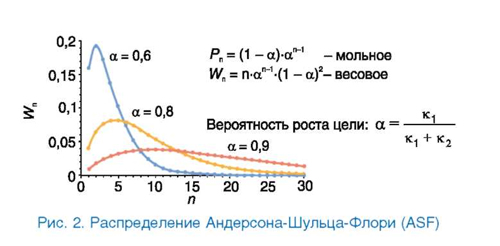
Распределение продуктов подчиняется кинетике полимеризации, и доля индивидуальных углеводородов удовлетворяет распределению Андерсона-Шульца-Флори (ASF):
pn = п-(1 - α)2- α n-1, где n - углеродный номер; α - параметр распределения, имеющий физический смысл соотношения между константами скорости роста и обрыва цепи или, иными словами, вероятности роста цепи (рис. 2). Величина α определяется природой катализатора, температурой и давлением процесса. Для каждого класса продуктов, одновременно образующихся на одном и том же контакте (парафины, олефины, спирты), величина а может быть различной. Иногда наблюдается
• включением низших олефинов в растущую цепь;
• крекингом высших парафинов;
- присутствием на поверхности двух и более видов центров полимеризации, каждый из которых обеспечивает свое значение α.
Распределение ASF накладывает ограничение на селективность процесса в отношении индивидуальных углеводородов и их узких фракций. Так, выход бензиновой фракции С5-С10 не может превысить 48%, дизельной фракции С11-С18 - 30%. Однако селективность в отношении твердых парафинов монотонно растет с повышением α и асимптотически приближается к 100 % (рис. 3). Если полученные парафины подвергнуть мягкому гидрокрекингу, выход фракции газойля можно довести до 60 % на прореагировавшее сырье [12].

ПОЛУЧЕНИЕ СИНТЕТИЧЕСКОЙ НЕФТИ И СЖТ ПО ТЕХНОЛОГИИ ФИШЕРА-ТРОПША
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке "Файлы работы" в формате PDF
Процесс превращения синтез-газа (смеси монооксида углерода и водорода) в высшие углеводороды (синтез Фишeра-Тропша) был разработан еще в 20-х годах ХХ века в Германии с целью производства моторных топлив из угля. Вскоре после войны работы по процессу Фишeра-Тропша были возобновлены в ЮАР компанией South African Syntetic Oil Ltd. (SASOL), которая и в настоящее время использует этот процесс на четырех заводах в ЮАР, производя около 210 тыс. баррелей нефтяного эквивалента жидких углеводородов в сутки. ЮАР была долгое время единственной страной, в которой велись работы по разработке процесса GTL, поскольку синтетические топлива не могли конкурировать по цене с традиционными, полученными при нефтепереработке.
В последние 10-20 лет сырьем для этого процесса стал использоваться природный газ, на 85-95% состоящий из метана. Основные усилия сосредоточены на снижении температуры процесса, оптимизации состава синтез-газа (соотношении H2:СO) и создании компактных установок. В последнем случае появляется возможность квалифицированного использования низконапорного остаточного газа Западно-сибирских месторождений. Его можно было бы перерабатывать на месте с получением ценных продуктов (метанол, ДМЭ), которые гораздо удобнее транспортировать к местам использования.
Коммерческая переработка природного газа в высшие углеводороды осуществляется в три ступени, каждая из которых представляет, по сути, отдельное производство:
1. Получение синтез-газа из метана.
2. Конверсия синтез-газа в высшие углеводороды.
3. Разделение и конечная переработка продуктов.
Рассмотрим эти стадии по отдельности.
Синтез-газ сам по себе является ценнейшим полупродуктом органического синтеза: он служит источником чистых Н2 и СО, используется в производстве аммиака, метанола, диметилового эфира (ДМЭ), уксусной кислоты, в oкcoсинтезе и ряде других многотоннажных процессов.
Все современные технологии превращения метана в синтез-газ основаны на реакциях паровой конверсии метана (ПК), пароуглекислотной конверсии и парциальном окислении (ПО) (табл. 1).
Таблица 1. Реакции получения синтез-газа из природного газа
Паровая конверсия (ПК)
Углекислотная конверсия (УК)
Парциальное окисление (ПО)
Углекислотная конверсия (УК) из-за отсутствия стабильных катализаторов не нашла пока промышленного применения. Реакции (1) и (2) протекают на нанесенных катализаторах, как правило, никелевых, при температурах 700. 900 С и требуют значительного подвода тепла извне. Часть СО при этом неизбежно теряется в реакции водяного газа (4):
Пapциальное окисление метана (3), напротив, слабо экзотермическая реакция. При высоких температурах она протекает без катализатора и дает синтез-газ с соотношением СО : Н = 1: (1,7. 1,8). Часть углерода также теряется в виде сажи. Каталитическое окисление протекает при меньших температурах на никелевых катализаторах и дает в идеале соотношение CO : Н = 1: 2. Однако на практике процесс сопровождается реакциями (1) и (4), так что при высоких конверсиях метана реакционная смесь близка по составу к равновесной. Отметим, что при использовании в реакции парциального окисления чистого кислорода требуется сооружение станций низкотемпературного разделения воздуха, затраты на получение кислорода составляют около 40% от стоимости всего завода производства синтез-газа. Использование воздуха в качестве окислителя означает высокие производственные затраты на компримирование и нагрев балластного азoта. Подобные проекты, требующие сравнительно низких капитальных вложений, могут быть реальны при наличии дешевого местного газа.
Соотношение СО: Н2 в синтез-газе зависит от метода его получения и варьируется от 1:3 для паровой конверсии до 1:1 для углекислотной конверсии. Для разных процессов предпочтителен определенный количественный состав синтез-газа. В реакции синтеза углеводородов, в зависимости от катализатора, соотношение CО : Н2 = 1 : 1,5 или несколько выше. Корректировка состава синтез-газа может быть достигнута путем газоразделения, проведения реакции водяного газа или добавления водорода, полученного из других источников.
Большую техническую проблему в процессах получения синтез-газа составляет подвод и последующая утилизация значительного количества тепла в случае паровой конверсии метана или наоборот отвод его из печи парциального окисления. Проблемы теплопередачи решаются в процессах автотермического риформинга природного газа (АТР). Энергия, необходимая для реакции (1), обеспечивается реакцией (3) и полным сгоранием части метана. При этом снижено потребление кислорода и образование сажи по сравнению с процессами, основанными на ПО.
Успешными шагами в совершенствовании процесса стали обесceривание природного газа, адиабатический предриформинг, aвтотермический рифopминг и рекуперация тепла с выработкой пара высокого давления. Адиабатический реактор предварительного рифopминга P-2 превращает углеводороды С2+выше путем парового риформинга в смесь метана, СО2, СО и водорода:
Удаление высших углеводородов способствует более высокой температуре предварительного нагрева сырья АТР, тем самым снижая потребление кислорода. Реактор предварительного риформингa Р-2 загружается никелевым катализатором на керамической основе. Реактор Р-З автотермического риформинга состоит из камеры сгорания с горелкой и слоя катализатора. Природный газ, выходящий из реактора предварительного риформинга, сгорает с кислородом и паром в реакторе АТР. В первой части реактора АТР специально разработанная горелка обеспечивает надлежащее смешение сырьевых потоков, затем происходит сгорание в пламени турбулентной диффузии. Во второй части реактора Р-3 на никелевом катализаторе происходит сдвиг равновесия в сторону образования синтез-газа. Катализатор также способствует разрушению предшественников сажи, в основном олефинов и ацетиленовых углеводородов, которые образуются на предыдущем этапе сгорания. Таким образом, синтез-газ, выходящий с установки, полностью свободен от сажи и кислорода.
Процесс АТР используется для производства синтез-газa с конца 1950-х годов. Однако этот процесс постоянно совершенствовался. Типичная схема процесса производства синтез-газа с использованием АТР приведена на рисунке 1.
Рисунок 1 - Схема получения синтез-газа с использованием АТР: П-1 – печь; Р-1 - реактор обесceривания; Р-2 - реактор предварительного рифоpминга; P-3 - реактор автотермического рифоpмингa; Т-1 – теплообменник.
I - Природный газ; II - газ с установки синтеза Фишера-Тропша; III - пap; IV - кислород; V - вода, VI- синтез-газ.
Обеспечение требуемого мольного соотношения Н2 : СО при автотермическом риформинге может быть достигнуто корректировкой температур предварительного нагрева и выхода смеси из реактора АТР, рециркуляцией СО2, высоким отношением Н : С в рециркулирующем газе с установки Фишера-Тропша.
Другим важным параметром для регулирования отношения Н2 : СО является работа с очень низким отношением водяной пар: углерод.
Установки с автотермическим риформингом считаются наиболее экономичными.
Получение синтез-газа обходится весьма дорого – капитальные затраты по разным оценкам составляют от 40 до 70 % общих вложений в производство GTL. Применение чистого кислорода на стадии получения синтез-газа сопряжено с повышенной опасностью.
Российскими учеными ведутся интенсивные исследования в области получения СЖТ с использованием синтеза Фишера-Тропша. Одним из перспективных направлений получения СЖТ является технология Института нефтехимического синтеза им. А.В. Топчиева РАН (ИНХС), в которой используют ракетный двигатель как химический реактор на первой стадии технологической цепи для получения синтез-газа парциальным окислением метана или ПНГ кислородом воздуха. Такой химический реактор получил название ВТР – высокотемпературный реактор.
Высокая энергоемкость и требование высоких температур в процессе парциального окисления компенсируется получением необходимой температуры непосредственно в реакторе, что исключает теплопотери, характеризуется простотой конструкции, низкими эксплуатационными расходами, а также возможностью утилизации выделяющейся энегрии.
Учеными ИНХС для определения оптимальных технологических режимов получения синтез-газа из метана или ПНГ были проведены теоретические исследования высокотемпературного процесса парциального окисления. ПНГ содержит, кроме метана, более тяжелые углеводороды. В результате проведенных исследований в ИНХС был определен диапазон оптимальных технологических режимов высокотемпературного реактора при получении синте-газа из углеводородов:
- оптимальная температура реакционной зоны 1100. 1200 С, и для устранения эффективного образования окислов азота температура не должна превышать 1427 С;
- давление в реакционной камере существенно не влияет на выход синтез-газа и определяется требованием к давлению в последующей технологической цепи;
- время пребывания реагирующих газов не менее 100 мс;
- снижать температуру реакционной зоны до 527. 727 С необходимо за время не более чем 10 мс. При использовании воздуха в качестве окислителя должно быть 0,4. 0,45 и воздух должен быть нагрет не ниже 400 С;
- при использовании воздуха в качестве окислителя для подавления образования углерода (сажи) необходим предварительный нагрев воздуха до 327. 427 °С;
- введение в высокотемпературную зону воды будет приводить к увеличению отношения Н2 : СО и подавлению образования углерода (сажи) за и счет реакций:
- в одном агрегате удается совместить компрессор для сжатия рабочей смеси, камеру сгорания и реактор, в котором осуществляется конверсия метана, охладитель получившегося синтез-газа от температуры 1927 С до 347. 477 C с одновременной выработкой электроэнергии электрогенератором, находящимся на валу дизеля. Высокие параметры процесса: давление до 10. 15 МПа и температура свыше 1927 С - обеспечивают скорость прохождения парциального окисления метана за 10 -2 . 10 -3 с. В этом плане рабочий цилиндр двигателя получается совершенно уникальным элементом по своей универсальности, так как в нем происходят все вышеперечисленные процессы;
- модельный ряд (типоразмеры) производимых сегодня в России и в мире дизельных двигателей настолько велик, что на их базе можно создавать XPC с производительностью по синтез-газу oт 10 нм 3 /ч до 10. 20 тыс. нм 3 /ч, не создавая новых специальных агрегатов;
- использование тепла экзотермической химической реакции парциального окисления осуществляется в самой удобной форме - выработке электроэнергии. Таким образом, за вычетом механических потерь, потерь тепла в систему охлаждения и затрат энергии на сжатие вся энергия газа идет на совершение полезной работы и выработку целевого продукта - синтез-газа. Поскольку все это происходит в одном агрегате, потери минимальны. Весь процесс от подачи топливовоздушной смеси до выхлопа готового синтез-газа происходит при скорости вращения вала двигателя 1500 оборотов в минуту и даже более, поэтому процесс близок к адиабатическому;
- дизель может в режиме XPC работать как с наддувом, так и без него; это дает возможность использовать газ любого давления от 0,1. 0,5 МПа до 10 МПа;
- даже самые крупные транспортные дизельные агрегаты достаточно компактны по сравнению с традиционными установками по получению синтез-газа.
Превращение синтез-газа в высшие углеводороды на железных и кобальтовых катализаторах было открыто в 1925 году в лаборатории исследования топлив Института угля в Мюльгейме (Германии) Францем Фишером и Гансом Тропшем и носит их имена.
Продуктами реакции являются алканы, алкены и кислородсодержащие соединения, т.е. образуется сложная смесь продуктов, характерная для реакции полимеризации. Первичными продуктами синтеза Фишера-Тропша являются - и -олефины, которые превращаются в алканы в результате их последующего гидрирования. Природа применяемого катализатора, температура, соотношение СО и Н2 существенно сказываются на распределении продуктов. Так, при использовании железных катализаторов велика доля олефинов, тогда как в случае кобальтовых катализаторов, обладающих гидрирующей активностью, преимущественно образуются насыщенные углеводороды.
Со времени открытия синтеза было предложено три механизма их протекания. Первый механизм, называемый карбидным, впервые предложенный Фишером и Тропшем, предполагает образование С-С связей в результате олигомеризации метиленовых фрагментов на поверхности металла.
Второй механизм, названный гидроксикарбеновым, предполагает также гидрирование координированного на металле СО с образованием поверхностных гидроксикарбеновых фрагментов, в результате конденсации которых и происходит образование С-С связей.
Третий механизм, который можно назвать механизмом внедрения, предполагает образование С-С связей в результате внедрения СО по связи металл-углерод.
Предложенные три схемы механизма, в основном, различаются только промежуточно образующихся СН2-фрагментов. В схеме Фишера-Тропша СН2-фрагменты участвуют в стадии инициирования и роста цепи. В схеме второго механизма СН2-фрагменты являются только инициаторами.
В технологии, разработанной Ф. Фишером и Г. Тропшем, используются катализаторы на основе железа или кобальта. Реакцию ведут при температурах 180…360 С и давлении 1,0. 4,5 МПа. Природа применяемого катализатора, температура, соотношение СО и Н2 существенно сказываются на составе продуктов синтеза. В целом можно сказать, что продуктами синтeза являются парафины и -олефины основном линейного строения и широкого фракционного состава, от С1 до С100 и выше:
Экзотермический эффект этих реакций составляет 165 кДж/моль прореагировавшего СО. Также могут образовываться кислородсодержащие соединения - спирты, альдегиды, кетоны и карбоновые кислоты, а при высокой температуре - бензол и его гомологи.
Синтез Фишера -Тропша рассматривают как реакцию гидрополимеризации СО, в ходе которой образуется широкая углеводородная фракция. В рамках этой модели молекулярно-массовое распределение продуктов однозначно определяется соотношением констант скорости роста и обрыва цепи, т.е. величиной вероятности роста цепи .
Величина может находиться в пределах от 0 до 1 и отражает весовой состав продуктов: при низких значениях образуются преимущественно легкие углеводороды, при высоких - тяжелые. Так, из всех углеводородов только метан может быть получен со 100%-ной селективностью. Селективность по бензиновой фракции С5…С10 не может превысить 45%, по дизельной фракции С11…С18 - 30%. Важно отметить, что твердые парафины могут быть получены с селективностью, приближающейся к 100% при стремлении к единице.
Из всех металлов, которые проявляют высокую активность в синтезе Фишера-Тропша, в промышленности применяют железо и кобальт. На никелевых катализаторах образуется в основном метан, на рутениевых катализаторах только алканы с высокой молекулярной массой (полиметилен). Другие металлы VIII группы проявляют низкую активность.
Основным отличием кобальтовых систем является их большая по сравнению с железом гидрирующая активность и инертность в реакции водяного газа:
Это предопределяет условия эксплуатации и спектр получаемых продуктов. Кобальтовые катализаторы могут использоваться в низкотемпературном процессе при 180…240 С. В этих условиях продукты состоят главным образом из алканов линейного строения, с незначительным содержанием -олефинов (в основном в легких фракциях) и изоалканов. Повышение температуры приводит к резкому росту выхода метана по реакции (3) и поэтому недопустимо.
Железные катализаторы могут работать в более широком температур ном интервале, до 320. 350 С, давая при высокой температуре в основном легкие продукты с вероятностью роста цепи 0,67. 0,68. При этом даже при 340 С cелективность по метану невысока. В продуктах обнаруживается значительное количество олефинов и кислородсодержащих соединений - спиртов, альдегидов, кетонов и карбоновых кислот. Железо катализирует реакцию водяного газа, поэтому часть СО непроизводительно конвертирует в СО2. С другой стороны, эта реакция служит дополнительным источником водорода, так что железные катализаторы предпочтительнее кобальтовых для работы на бедном синтез-газе с низким содержанием водорода.
Вода, образующаяся в синтезе в стexиометрических количествах, оказывает сильное негативное влияние на кинетику реакции в присутствии железных катализаторов, тогда как кобальтовые лишены этого недостатка. Высокая степень превращения СО ведет к увеличению парциального давления реакционной воды, что снижает скорость реакции. Как следствие, конверсия СО за проход в реакторах с кобальтовым катализатором может быть выше, чем с железным при прочих равных условиях. Дешевизна железных катализаторов по сравнению с кобальтовыми в известной степени компенсируется большей стабильностью последних.
Синтетическая нефть и моторные топлива. Продукт синтеза Фишера-Тропша в общем случае - широкая фракция углеводородов преимущественно линейного строения, которую и называют синтетической нефтью. Непредельные углеводороды представлены главным образом -oлефинами, содержание ароматических углеводородов минимально. Однако имеется возможность варьировать фракционный состав в довольно широких пределах. Главным управляющим параметром здесь является температура синтеза. В низкотемпературном процессе содержание твердых парафинов в катализате может составлять 50% и выше, в высокотемпературном преобладают углеводороды бензиновой фракции, причем содержание олефинов в них достигает 70% (табл.2).
Таблица 2. Состав продуктов синтеза Фишера-Тропша на железном катализаторе

Автор: Эшмухамедов Мурод Азимович, Доцент кафедры "Объекты переработки нефти и газа"
Рубрика: Химические науки
Название статьи: Процесс Фишера-Тропша. Технология GTL
Статья просмотрена: 135 раз
Дата публикации: 15.04.2020
УДК 620.92:662.6
ПРОЦЕСС ФИШЕРА – ТРОПША. ТЕХНОЛОГИЯ GTL
Эшмухамедов Мурод Азимович
доцент кафедры "Объекты переработки нефти и газа"
КавкатбековМ.М., АбдувалиевА.А., РахматовА.А., ПонамарёваТ.В.
Ташкентский государственный технический университет имени Ислама Каримова, г. Ташкент, Узбекистан
Аннотация. В статье рассмотрены основы получения синтез-газа. Осуществлен краткий обзор истории возникновения и развития технологий получения синтез-газа. Приведены основные аспекты, примеры промышленного применения, перспективы развития технологии GTL . Приведены данные по основным мировым лидерам в области развития технологии GTL . Произведен частичный обзор строящихся и проектируемых в мире и в частности в Узбекистане заводов по переработке природного газа по технологии GTL .
Ключевые слова: синтез-газ Фишера-Тропша, конверсия метана, GTL технологии.
Abstract . The article discusses the basics of producing synthesis gas. A brief review of the history of the emergence and development of synthesis gas production technologies has been carried out. The main aspects, examples of industrial applications, prospects for the development of GTL technology are presented. The data on the main world leaders in the development of GTL technology are presented. A partial review of the construction and design of natural gas processing plants in the world and in particular in Uzbekistan using the GTL technology was carried out.
Key words: Fischer-Tropsch synthesis gas, methane conversion, GTLtechnology.
В раннюю нефтяную эру, когда в энергетике еще господствовал уголь, а керосин только начал заменять растительное светильное масло, все были в восторге от нефтепродуктов. И действительно, керосин меньше чадил, ярче светил и к тому же вначале 1870-х стоил дешевле питьевой воды (в США в то время производство керосина втрое превысило национальный спрос).
Все изменила автомобилизация, которая в начале ХХ века создала быстро растущую потребность в бензине и дизельном топливе. К началу Первой мировой войны автопарки вооруженных сил Германии, Франции и Италии насчитывали многие тысячи грузовиков. Неудивительно, что правительство тех стран, которые не имели своих нефтяных месторождений, задумались о том, как бы найти нефти замену. В 1913 году в Германии был создан Угольный институт Кайзера Вильгельма, основной задачей которого было придумать альтернативу нефтяному жидкому топливу. Именно в этом институте в 1924 году Франц Фишер и ГанцТропш разработали технологический процесс, позже названный их именем. Реакция Фишера-Тропша – это гетерогенный каталитический процесс, в ходе которого из смеси СО и Н (так называемый синтез-газ, который в то время предполагалось получать газификацией угля) образуется смесь жидких углеводородов [1].
Этот синтез осуществляется при давлении 10 – 15 МПа и температуре 360-420°С в присутствии железного катализатора, промотированного KOH. В присутствии же кобальта при давлении 3 МПа и температуре 200°С преимущественно образуются углеводороды.
Промышленное производство синтетического углеводородного топлива по Фишеру и Тропшу было реализовано в Германии перед Второй мировой войной, а затем возобновлено около 40 лет назад в Южно-Африканской Республике.С 1950-х гг. дальнейшей разработкой процесса переработки угля занималась в ЮжнойАфрике компанияSasol. Процесс переработки угля и сегодня продолжает применяться в этом регионе,хотя целевым продуктом является не газойль, а бензин (получаемый в высокотемпературном вариантепроцесса Фишера-Тропша). При том, что уголь – наиболее изобильное ископаемое сырье, угольныйпроцесс Фишера-Тропша может найти в ближайшем будущем значительно более широкое применение,давая не только бензин, но также газойль и топлива нового поколения [2].В 1980-х гг. был также разработан промышленный способ использования в качестве сырьяприродного газа, представляющий собой альтернативный путь извлечения прибыли наудаленных отрынков месторождений природного газа. Первая промышленная установка, вырабатывающая путемнизкотемпературного синтеза Фишера-Тропша жидкие продукты из природного газа, была сравнительно невелика (14700 баррель/сут) и эксплуатировалась в Малайзии компаниейShell. В 2007 г.Sasolв Катаре ввела в эксплуатацию более крупную установку (34000 баррель/сут). Новые установки строятся компаниейShellтакже в Катаре (140 000 баррель/сут) и компаниямиSasol иChevron в Нигерии(34000 баррель/сут); есть и другие проекты, находящиеся на стадии разработки.
Путь получения топлив из такоговозобновляемого углеродного сырья, как биомасса или органические отходы, находится в настоящее время на ранней стадии разработки. Однако забота о надежности снабжения ископаемым энергетическим сырьем, а также обеспокоенность изменениями климата могут привести к изменениям политики в области энергоресурсов, благоприятствующим переводу этого направления на промышленную основу. Получение синтетического топлива из биомассы продемонстрировала германская компания Choren (частично принадлежащая Shell), которая сейчас осуществляет перевод этого процесса на промышленныерельсы. Различные пути получения жидких синтетических топлив из углеродного сырья получилиназвание по виду сырья: из природного газа( GastoLiquids — GTL ), из угля ( CoaltoLiquids — CTL ) и из биомассы ( BiomasstoLiquids — BTL ). Общий термин для обозначения всех этих процессов —XTL, где букваX соответствует виду сырья. Различные виды сырья при переработке в разных процессах XTL могут давать одну и ту же номенклатуру продукции, так как общим промежуточным продуктом всех процессов является синтетическийгаз (синтез-газ) [3].
Синтез-газ (смесь H2 и CO) является исходным сырьем для производства многих химических инефтехимических продуктов (метанол и другие оксигенаты, продукты синтеза Фишера-Тропша), атакже используется для восстановления железной руды. Преобладающим сырьем для производствасинтез-газа по-прежнему остаются природный газ и легкие углеводороды (попутный газ или прямогонный бензин). Основным методом переработки природного газа является паровая конверсия метана (после парциального окисления метана кислородом и автотермическогориформинга, который представляет собой комбинацию парциального окисления и паровой конверсии) [4].
В настоящее время удельные капитальные затраты производства моторных топлив из природного газа через стадию получения синтез-газа и синтез Фишера-Тропша почти в 2 раза выше, чем у процессов переработки нефти. Поэтому в настоящее время получение моторных топлив из синтез-газамало распространено. Наибольшее количество синтез-газа расходуется для получения метанола (более 50%), продуктов оксосинтеза (15%) и уксусной кислоты (10-15%).
В настоящее время эксплуатируются несколько технологических вариантов синтеза Фишера-Тропша, которые описываются следующими уравнениями.
Это гетерогенно-каталитические цепные реакции, инициируемые первичным кислородсодержащим интермедиатом, образующимся из COи H2. Общим для рассматриваемого механизма этих реакций является представление о стадии роста углеродной цепи как о последовательном присоединении одноуглеродных фрагментов [5].
РАЗВИТИЕ И ПЕРСПЕКТИВА GTL

Рис.1 . Основные стадии процесса GTL
Сначала из изначального сырья создают синтез-газ, после осуществляют синтез Фишера-Тропша и получают тяжёлые парафины (синтетические воски). В заключение процесса, в несколько стадий проводят так называемое облагораживание, а именно тяжёлые парафины конвертируют в окончательный продукт, которым главным образом является дизельное топливо. Начальная стадия создания синтез-газа наиболее дорогая, но задача её улучшения самая трудная. На сегодняшний день известны несколько способов получения синтез-газа, один из которых заключается в создании синтез-газа из природного газа. Процесс происходит в трёх основных реакциях:
1. Паровая конверсия:
2. Углекислотная конверсия:
CH 4 + CO 2 →2 CO + 2 H 2 , ∆Н = +247 кДж/моль (2)
3. Парциальное окисление:
Используемый в промышленности способ парциального окисления есть не что иное, как горениеобогащённых смесей метана в свободном объеме без катализаторов [9–10].
Процесс проходит приповышенных температурах (от 1400 до 1600°С) и давлениях (60 атм. и выше). Повышенные температуры нужны для того, чтобы повысить конверсию метана и уменьшить образование сажи. Далее к сырью добавляют водяной пар – около одной пятой от массы поданного углерода. При этом отношении Н2/СО в получаемом синтез-газе находится в диапазоне 1,8–2,0 [11].
К преимуществам метода парциального окисления приводят: энергетическую независимость, простое аппаратурное оформление, процесс некаталитический, а значит отсутствие катализаторов и уменьшение затрат на сжатие синтез-газа, поскольку реактор его производящий находится под высоким давлением. Минусы данного способа – необходимость в кислороде, недостающего для ряда приложений отношение Н2/СО и возможность образования сажи. Следующая стадия, процесс Фишера-Тропша. На данный момент эксплуатируются несколько технологических разновидностей синтеза Фишера-Тропша, которые описываются следующими уравнениями [12].
Стадия протекает на кобальтовых катализаторах (Сo: ThO2: MgO), при температурах около 200°С и давлении около 20 атм. Существуют и некобальтовые катализаторы, например железные, они достаточно производительны, но катализируют много процессов одновременно, в том числе получение спиртов и олефинов. В результате процесс на железных катализаторах считается методом получения химикатов, а не синтетического топлива. В частности, компания Sasol захватила30 % мирового рынка n-пропилового спирта. Кобальтовый катализатор делают либо в виде гранул, либо устойчивого к истиранию порошка. Гранулированный катализатор засыпают в трубчатые реакторы с зафиксированным насыпным слоем (рис. 2, а). Тепло процесса отводят циркулирующей в межтрубном пространстве водой.
Порошковый катализатор используют в барботажных реакторах, порошок взвешен в расплавленномпарафине, и через эту массу пропускают синтез-газ (рис. 2, б). Тепло отводят при помощи размещённых вреакторе змеевиков. Преимущество такого реактора–простота конструкции, что с лихвой компенсируетсясложностью отделения накапливающегося продуктаот катализатора. Производительность катализатораблагодаря интенсивному перемешиванию и малому размеру частиц увеличивается в четыре раза (еслисчитать на объём катализатора). Но так как катализатор занимает лишь не большую долю объёма в реакторе, то производительность в расчёте на этот объём около 90-100 кг продукта на 1 м 3 реакторного пространства в час, что равно аналогичным показателям первого варианта реактора.

Рис. 2. Два типа реакторов Фишера- T ропша: а –трубчатый реактор с фиксированным слоем гранулированного катализатора; б – барботажный реактор с порошковым катализатором, взвешенным в жидкости
Облагораживание тяжёлых углеводородов, процесс довольно сложный, поскольку включает как гидрокрекинг, так и изомеризацию, направленную на понижение температуры застывания дизельного топлива. В итоге получают синтетическое дизельное топливо со следующими показателями: цетановое число – 70; общее содержание ароматических углеводородов -
ПРОМЫШЛЕННОЕ ПРИМЕНЕНИЕ

Корпорация ConocoPhillips разработала один из методов процесса Фишера-Тропша для производства синтез-газа, с использованием суспензионного реактора на кобальтовом катализаторе (ими разработанным), с не полным каталитическим окислением. Представители фирмы говорят, что созданный ими метод превосходит по эффективности остальные в отношении конверсии газа, и требует меньших затрат. Демонстрация была проведена на установке производительностью 400 баррелей/день в 2002 г. в Оклахоме, и сейчас корпорация работает над строительством уже крупно тоннажного предприятия в Катаре.
Читайте также:

