Как сделать характеристику атома
Добавил пользователь Алексей Ф. Обновлено: 18.09.2024
Основной структурной единицей веществ атомного строения является атом.
Атом – мельчайшая, электронейтральная, химически неделимая частица вещества, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
Электрон – одна из элементарных частиц материи, обладающая массой покоя и элементарным отрицательным зарядом.
Когда говорят о массе покоя, то подразумевают, что частица может находиться в состоянии покоя и иметь массу. Существуют частицы, которые не могут находиться в состоянии покоя, например частицы света - фотоны. В этом случае говорят, что фотон не имеет массы покоя.
Заряд электрона называется элементарным, так как это наименьший отрицательный заряд в природе. По этой причине заряд электрона условно принимают равным -1.
Атомное ядро – центральная, положительно заряженная, сложно организованная часть атома, состоящая из нуклонов, связанных между собой ядерными силами.
С точки зрения атомной физики протон и нейтрон являются двумя состояниями одной и той же частицы – нуклона.
Нуклон – структурная единица ядра атома, которая может находиться в двух состояниях, протона и нейтрона.
Ключевые слова конспекта: строение атома, элементарные частицы, протоны и электроны в атомах, атомный номер, массовой число, число нейтронов, нуклид, изотопы, ионы, катионы, заряд иона.
Согласно модели Резерфорда каждый атом состоит из находящегося в его центре ядра и электронной оболочки. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре. Электроны движутся вокруг ядра. Число электронов атома равно положительному заряду ядра.
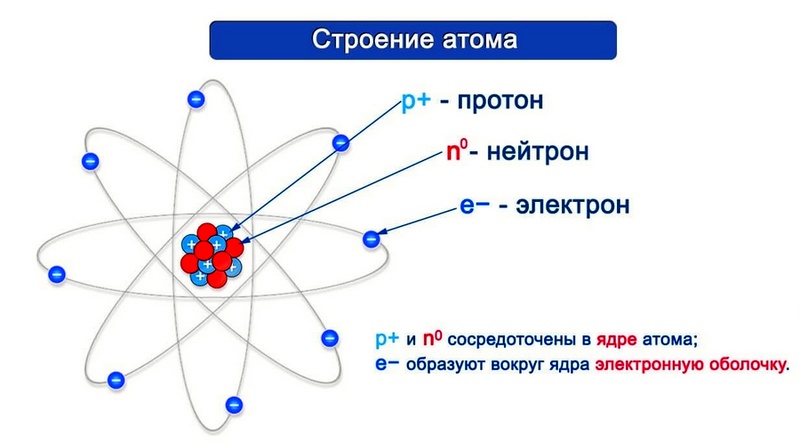
Диаметр атома 10 -10 м, диаметр ядра 10 -14 – 10 -15 м. Масса атома водорода равна 1,67 • 10 -24 г, атома углерода — 1,99 • 10 -23 г, атома железа — 9,29 • 10 -23 г.
Элементарные частицы — это протоны, электроны и нейтроны, из них состоят все атомы.
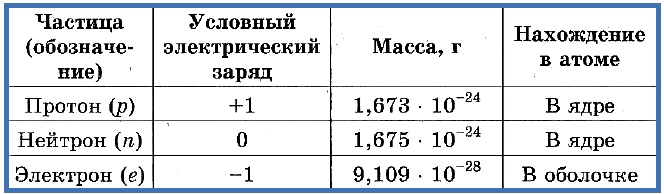
Число протонов разное у атомов различных видов, оно определяет заряд ядра атома и равно атомному номеру элемента в таблице Менделеева. Поскольку атом — электро-нейтральная частица, число электронов в нем равно числу протонов.
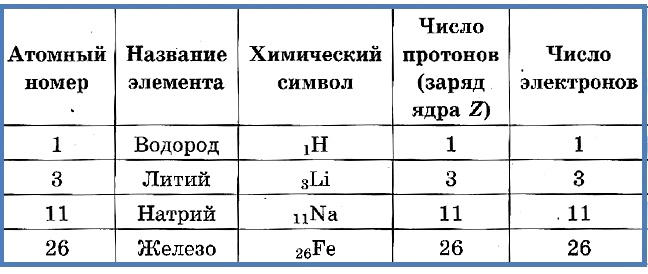
Атомный номер указывают слева внизу от символа элемента, например: 1Н, 26Fe. Обозначение атомного номера — прописная латинская буква Z.
Массовое число атома А — это сумма чисел его протонов и нейтронов в ядре. Массовое число указывают слева вверху от символа элемента или добавляют к названию элемента через дефис, например: 23 Na или натрий-23.
Массовое число кислорода, А( 16 О) = 16 = (8р + 8n).
Число нейтронов N в ядре атома определяют по формуле: N = A — Z. Например, для атома натрия с массовым числом 23, 23 Na: А = 23, Z = 11, N = А – Z = 23 — 11 = 12.
Нуклид — это вид атомов с определенным числом протонов и нейтронов в ядре. Например, в природе встречается три вида нуклидов кислорода: 16 О, 17 О и 18 О.
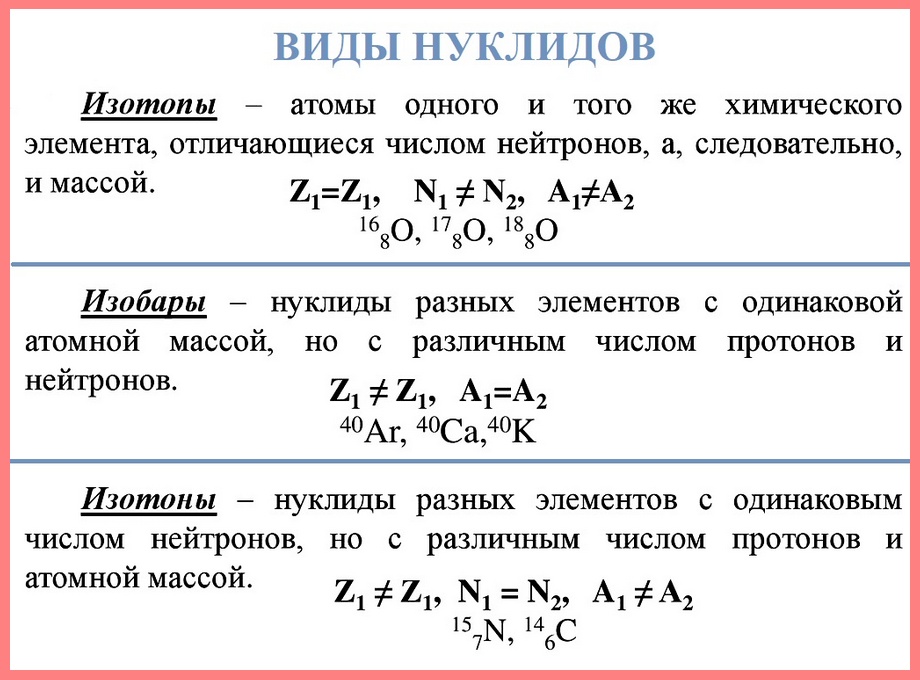
Изотопы — это атомы одного вида с одинаковым числом протонов, но разным числом нейтронов. Так, атомы 16 О, 17 О и 18 О — это изотопы. Природные изотопы урана — 234 U, 235 U и 238 U.
Ионы — заряженные частицы, образующиеся при отщеплении от нейтральных атомов или присоединении к ним электронов. Ионы образуются также из молекул в результате присоединения протона Н + (NH3 → NH4 + ) или отщепления Н + (HNO3 -> NO3 – ).

Катионы — это положительно заряженные ионы (Na + , Аl 3+ ), анионы — отрицательно заряженные ионы (Cl – , NO3 – ).
Заряд иона указывают в виде индекса справа вверху от символа химического элемента: Li + , Са 2+ . На первом месте пишут цифру, на втором — знак заряда. Цифру 1 не пишут.
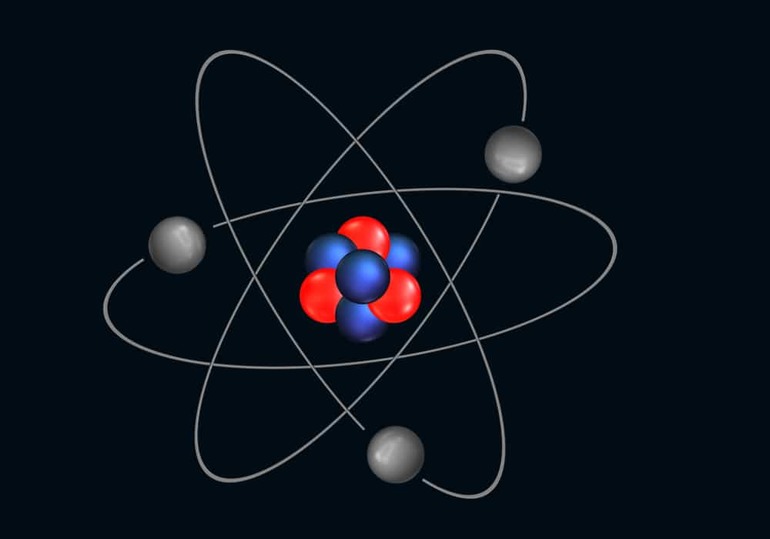
Как устроен атом
Со временем учёные выяснили, что они крупно заблуждались: структура атома оказалась вовсе не монолитной. С постепенным увеличением точности приборов стало ясно, что она включает в себя 3 типа микрочастиц: положительно, отрицательно и нейтрально заряженные. Называются они следующим образом:
Частицы, несущие положительный заряд, назвали протонами, нейтральный — нейтронами, отрицательный — электронами.
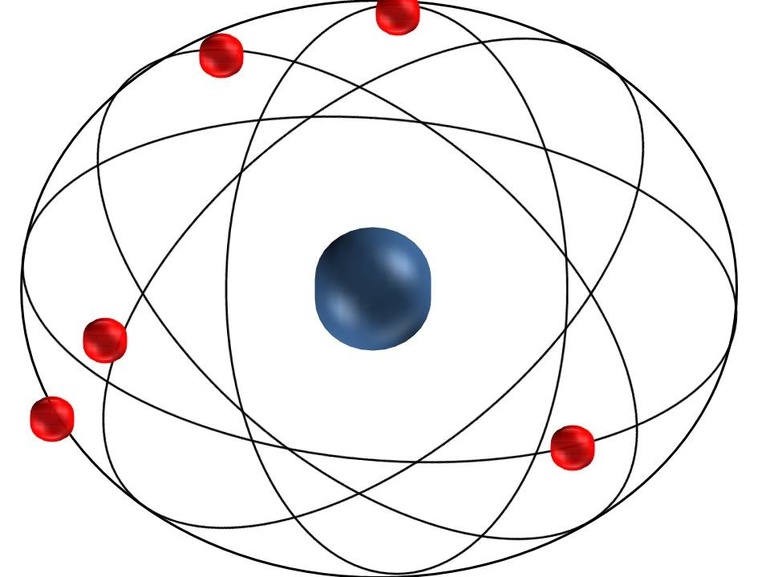
Основа любого атома — это его ядро. Оно состоит из положительных и нейтральных микрочастиц, то есть из протонов и нейтронов. Их количество может быть одинаковым, а может и разниться. В результате получается, что ядро — это всегда положительно заряженная часть атома. Однако сам он заряжен нейтрально, и причина тому — электроны, летающие вокруг ядра по орбитальным спиралям. Такова общая схема строения атома.
Ядро: протоны и нейтроны
Общее название для составных частиц ядра, коими являются протоны и нейроны — нуклоны. Вместе они и составляют почти всю массу атома, а значит, и почти всю материю во Вселенной. Теория гласит, что каждый протон или нейтрон включает в себя ровно 3 составные частицы, именуемые кварками, между которыми имеется связующее глюонов облако. Кварки, согласно модели, являются такими же неделимыми частицами, как электроны. Глюоны же обеспечивают их взаимную связь друг с другом.
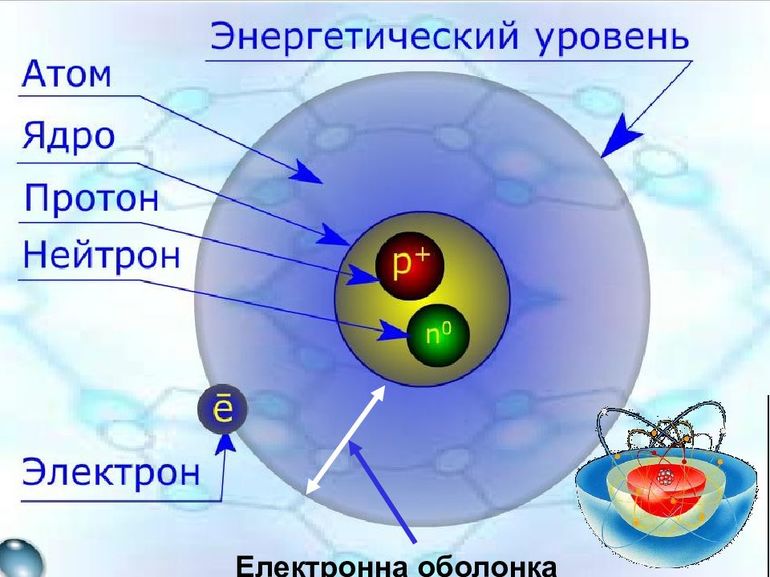
В то же время сами атомные ядра чрезвычайно малы. Размеры каждого ядра в десятки тысяч раз меньше размеров всего атома. Но несмотря на это, почти вся атомная масса заключается в его положительно заряженном ядре, тогда как электрон представляет собой чисто энергетическую, нематериальную частицу. Получается, что материального вокруг нас вовсе не так много, как кажется на первый взгляд. Куда больше места занимают энергетические потоки, связывающие физическое вещество.
Число протонов, содержащихся в том или ином атоме, указывает на его порядковый номер в Периодической системе химических элементов. Например, у кислорода порядковый номер 8, а значит, и число протонов у него точно такое же. Формула, по которой вычисляется количество нейтронов: округлённая атомная масса минус число протонов. Атомная масса элемента указана под его порядковым номером в графической таблице Менделеева. Например, для атома хлора (Cl) это будет 35 — 17 = 18, для брома (Br) 80 — 35 = 45, а для серы (S) 32 — 16 = 16. С числом нейтронов связано понятие изотопа.
Процесс ионизации
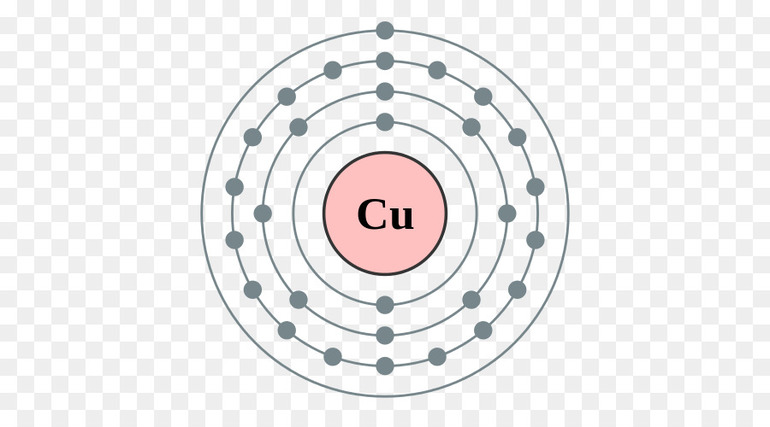
Возьмём для примера медь (Cu), относящуюся к классу простых веществ. В обычном состоянии у неё имеется 29 электронов. Но если она отдаст 2 электрона, у неё их останется всего 27. А сам атом меди превратится в положительный ион меди или, иначе, в катион меди. В их роли часто выступают всевозможные металлы (магний, алюминий, литий, натрий, хром), которые могут легко терять до трёх электронов.
Отрицательно заряженные ионы, в свою очередь, называются анионами. Как правило, они являются неметаллами, так как обладают высокой электроотрицательностью — способностью притягивать к себе электроны. Например, им может стать атом кремния, присоединив к себе хотя бы один электрон.
Что такое электрон
Электроны, двигающиеся вокруг ядра по сферической траектории, образуют так называемое электронное облако. А оно уже создаёт вокруг каждого атома его личное электромагнитное поле, оказывающее влияние на другие атомы.
Немного истории

В 1891 году в результате проведённых экспериментов ирландский физик Стони сумел вывести, что электричество переносится мельчайшими частицами, которые имеются в составе любого атома. Тогда же он и предложил назвать их электронами.
Спустя несколько лет, физики Перрен и Томсон нашли доказательства, что электрон имеет сугубо отрицательный заряд. Кроме того, они смогли рассчитать массу и скорость электрона.
Природа частицы
Отрицательная частица электрон имеет крайне маленькие размеры. Отдельные электроны не поможет разглядеть даже самый мощный микроскоп. Визуально их можно наблюдать только в виде размытого электронного облака вокруг ядра. Электрон — это устойчивая частица энергии, которая постоянно находится в движении. Вне движения он просто не существует. И не похоже, чтобы у этой энергетической единицы была какая-то структура. Но масса у него всё-таки есть, хотя, как и его габариты, она очень маленькая.
В теории электрон включает в себя 3 нематериальные квазичастицы, несущие о нём различную информацию. Всего их 3:

- Холон, отвечающий за заряд.
- Спинон, заведующий его вращением.
- Орбитон, говорящий о его положении на орбите.
Но это всего лишь условности, и они никак не указывают, что электрон и правда можно поделить на отдельные частицы. На текущем уровне развития науки эта частица пока считается неделимой. И нет оснований полагать, что в будущем это может измениться.
Электроны обладают способностью поглощать энергию. В случаях, когда это происходит, атом, который в себе их содержит, переходит с одного энергетического уровня на другой. Если поглощенной энергии слишком много, электрон может выйти из атомной структуры и стать независимой частицей. При этом он будет проявлять волновые свойства.
Электронная конфигурация
Электронная конфигурация атома — схематическое отображение отрицательных частиц, расположенных на атомных орбиталях. Умея делать такую запись, можно очень быстро определять количество орбиталей у того или иного атома. Перед тем как приступать к определению самой конфигурации, необходимо найти порядковый номер и заряд нужного элемента.
Любой атом состоит из нескольких электронных оболочек. Их максимальное количество достигает семи. Каждая из них имеет подуровни, заполняемые электронами последовательно, в строго установленном порядке. Число подуровней, содержащееся в той или иной оболочке, равняется её номеру. Внешние слои с большим количеством подуровней, находящиеся дальше от ядра, имеют большую энергию по сравнению с внутренними, чьё расположение близко к ядру.

Всего есть 6 типов подуровней, каждый из которых может содержать определённое число орбиталей. Электроны на каждом из них, когда они заполнены полностью, располагаются в чётном количестве. Эти подуровни обозначаются следующими буквами:
- s. Имеет всего одну орбиталь. Может содержать только 2 электрона.
- p. 3 орбитали, максимальные 6 электронов.
- d. 5 орбиталей, 10 частиц.
- f. 7 орбиталей, 14 частиц.
- g. 9 орбиталей, 18 частиц.
- h. 11 и 22 частицы.
- i. 13 и 26 частиц.
Орбитали заполняются в следующем порядке:
1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
Цифра справа обозначает номер оболочки, буква слева — подуровень этой оболочки.
Наглядная запись
Теперь возьмём для примера какой-нибудь химический элемент. Например, калий. В таблице Менделеева он имеет запись K и его можно найти под номером 19. Значит, у него имеется 19 электронов, которые нужно расфасовать по орбиталям в указанном порядке. Делаем это.

Сначала идёт уровень 1s. Подуровень s может содержать только 2 электрона. Число электронов записывается в виде маленького индекса над буквой. В данном случае это будет 1s 2 .
Следом по порядку идёт 2s. Тоже s и тоже только 2 электрона. 2s 2 .
Дальше 2p. Смотрим, сколько электронов может содержать уровень p. 2p 6 .
Теперь снова возвращаемся на подуровень s, который опять-таки включает в себя всего лишь 2 электрона. 3s 2 .
12 уже упорядочено. Осталось 7. И следующий уровень — 3p 6 .
Остался всего один электрон, который нужно разместить на следующем s-подуровне. В результате на нём остаётся одно свободное место — всего частиц может быть 2, но мы располагаем только одну оставшуюся. А записывается это как 4s 1 .
В одну строчку это всё записывается следующим образом: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 .
Различные атомные модели

Ещё философы Древней Греции — колыбели науки, пытались постичь природу этой необыкновенной частицы. Особенно среди прочих выделился Демокрит. И пусть с вершины нынешней науки его идеи кажутся немного наивными и примитивными, на тот момент это всё же был большой прорыв.
По мнению философа, из атомов состоит даже такая неосязаемая субстанция, как человеческая душа. Ещё он считал, что каждый отдельный атом имеет примерно те же физические свойства, что и вещество, которое он образует. Например, огонь, как он думал, должен иметь острые атомы, а вода — наоборот, гладкие.
Английский физик Дж. Томсон тоже внёс значительный вклад в развитие представлений об атомном устройстве. Но несмотря на это, и его идеи были несколько ошибочными. В 1904 году он выдвинул модель, рассматривающую атом в качестве физического тела, имеющего положительный заряд, внутри которого располагались отрицательно заряженные частицы.
В том же году, что и Томсон, Х. Нагаока предложил планетарную модель атома, которая была уже ближе к истине, но все равно не дотягивала до неё. В его модели строения атома электроны подобны кольцам Сатурна, и по тому же принципу крутятся вокруг ядра с положительным зарядом.
Последняя предложенная модель была разработана совместно Бором и Резерфордом. Она же и является устоявшейся в современном учёном мире. Практически все последующие научные наработки берут за основу именно их теорию строения атома, лишь с некоторыми незначительными изменениями. Её так и назвали — модель Резерфорда-Бора.
Атомы каждого химического элемента имеют строго индивидуальный линейчатый спектр, присущий только данному элементу и не меняющийся от опыта к опыту. Как это можно объяснить? Как вывести формулу, дающую весь набор частот атомного спектра? Чтобы сделать это, нужно узнать, как устроен атом.
Модель Томсона
Согласно Томсону атом представляет собой шар размером порядка см. По этому шару некоторым образом распределён положительный заряд, а внутри шара, подобно изюминкам, находятся электроны (рис. 1 ).

Рис. 1. Модель атома Томсона
Суммарный заряд электронов в точности равен положительному заряду шара, поэтому атом в целом электрически нейтрален.
Излучение атомов объясняется колебаниями электронов около положений равновесия (как вы помните, любой ускоренно движущийся заряд излучает электромагнитные волны). Однако вся совокупность экспериментальных данных по атомным спектрам не укладывалась в модель Томсона. Например, для некоторых химических элементов были подобраны формулы, хорошо описывающие их спектры, но эти формулы из модели Томсона никак не следовали.
Опыты Резерфорда
Резерфорд говорил об -частицах как об ионах гелия; сейчас мы знаем, что это ядра гелия.
Но в те времена об атомных ядрах ещё ничего не знали — о них Резерфорду лишь предстояло догадаться, глядя на результаты своих знаменитых опытов!
Каково же было всеобщее удивление, когда такие частицы обнаружились! Да, как и следовало ожидать, подавляющая доля -частиц отклонялась несущественно. Но совсем небольшая их часть (примерно одна частица из нескольких тысяч) отклонялась на угол, больший (рис. 2 ).

Рис. 2. Рассеяние -частиц на атомах
Эти отклонения казались совершенно невероятными. По словам Резерфорда, дело выглядело так, словно артиллерийский снаряд налетел на кусок бумаги и от удара повернул назад.
Расчёты, однако, показывают, что такое поле оказывается слишком слабым — его тормозящего действия никак не хватит для того, чтобы остановить -частицу и отбросить её назад!
Таким образом, наличие -частиц, отброшенных фольгой, опровергло модель Томсона. Что же было предложено взамен?
Планетарная модель атома
Чтобы отбросить -частицу, положительный заряд атома должен создавать куда более сильное электрическое поле, чем то, которое получается в модели Томсона. А чтобы создать такое поле, положительный заряд должен быть сосредоточен в области, гораздо меньшей размера атома.
Размер этой области можно вычислить. Если положительный заряд занимает область размером , то вблизи заряда создаётся электрическое поле с потенциалом
Зная кинетическую энергию -частицы, можно найти величину тормозящего потенциала , а затем и размер положительно заряженной области. Вычисления, проведённые Резерфордом, дали следующий результат:
Эта величина на пять порядков (в сто тысяч раз!) меньше размера атома. Так на смену модели Томсона пришла планетарная модель атома (рис. 3 ).

Рис. 3. Планетарная модель атома
В центре атома находится крошечное положительно заряженное ядро, вокруг которого, словно планеты вокруг Солнца, движутся электроны. Между ядром и электронами действуют силы кулоновского притяжения, но упасть на ядро электроны не могут за счёт своего движения — точно так же, как и планеты не падают на Солнце, хоть и притягиваются к нему.
Заряд ядра по модулю равен суммарному заряду электронов, так что атом в целом электрически нейтрален. Однако электроны могут быть выбиты из своих орбит и покинуть атом — тогда атом превращается в положительно заряженный ион.
Масса электронов составляет очень малую часть общей массы атома. Например, в атоме водорода всего один электрон, и его масса в раз меньше массы ядра. Следовательно, почти вся масса атома сосредоточена в ядре — и это при том, что ядро в сто тысяч раз меньше самого атома.
Чтобы лучше почувствовать соотношение масштабов атома и ядра, представьте себе, что атом стал размером с Останкинскую телебашню ( м). Тогда ядро окажется горошиной размером мм, лежащей у вас на ладони. И тем не менее, почти вся масса атома заключена в этой горошине!
Вот таким удивительным объектом оказался атом. Однако планетарная модель атома, объяснив результаты опытов Резерфорда по рассеянию -частиц, оказалась лишь первым шагом на пути к пониманию внутриатомных процессов. А именно, планетарная модель приводила к одному серьёзному противоречию, и преодоление этого противоречия Нильсом Бором положило начало физике атома. Читаем следующий листок!

Сегодня даже дети дошкольного возраста знают, что все вокруг состоит из молекул и атомов. А вот что это такое и из чего они, в свою очередь, состоят — знает далеко не каждый взрослый. В этой статье просто и доступно, поделимся современными знаниями о мельчайших частицах.
Что такое атом — история открытия
Итак, все окружающие нас объекты и мы сами состоим из крошечных частиц, которые называются атомами. В их состав входят еще меньшие частицы: протоны, нейтроны и электроны. Современное строение атома наука открыла сравнительно недавно, до этого его долго считали неделимой частицей.
Мысль о том, что все вокруг состоит из мельчайших, невидимых глазу частиц возникла в Древней Греции и Древней Индии еще до нашей эры. Древнегреческий философ Демокрит был материалистом. Именно он первым ввел в обиход понятие атома (с греческого — atomos — неделимый). Демокрит считал, что невидимые частицы вечны, их бесчисленное множество, они постоянно двигаются, обладают весом, размером и формой.
Последующее развитие теория атомизма получила в Средние века и Новое время в работах французского физика Пьера Гассенди (1592—1655 гг.) и английского ученого Роберта Бойля (1627-1691 гг.).
Развитием атомистической теории и превращением ее в атомно-молекулярное учение занимались также Ломоносов, Лавуазье, Дальтон.
Но теорию Томсона опроверг Эрнест Резерфорд. В 1917 году британским физиком было совершено открытие протона — положительно заряженной элементарной частицы. Открыв протон, Резерфорд предположил и наличие нейтронов — нейтрально заряженных частиц в атоме. Позже их существование экспериментально подтвердил Джеймс Чэдвик. Основываясь на своем открытии, Резерфорд предложил свое описание атомной модели: положительно заряженное ядро и окружающие его электроны.
В начале XX века планетарную модель заменила волновая модель, принятая научным сообществом во всем мире.
Современные представления о строении атома были бы невозможны без открытия элементарных частиц и явления радиоактивности. Огромный вклад в науку, помимо вышеназванных ученых, внесли Эрвин Шредингер, Макс Планк, Вольфганг Паули.
Атомная структура — современные знания

На чем базируется, из скольки главных частиц состоит
Основу современных представлений теории атомизма составляют следующие положения:
- Атом состоит из ядра и окружающей его электронной оболочки.
- Электронная оболочка представляет собой движущиеся вокруг ядра электроны.
- Ядро всегда положительно заряжено — оно состоит из протонов, обозначающихся символом — p и нейтронов — n. Заряд ядра всегда равен сумме протонов в нем.
- Атом электронейтрален, так как число отрицательных частиц — электронов (е–) равняется числу положительных частиц — протонов (p+).
- Его электронейтральность может нарушаться, при условии, что он отдает или присоединяет электроны, при этом он становится положительно или отрицательно заряженным ионом соответственно.
- Электроны располагаются вокруг ядра в трехмерном пространстве. Они находятся в специальных областях, которые называют орбиталями. Каждая из этих областей характеризуется формой, размером и ориентацией внутри атома, каждой из орбиталей присваивается буквенно-цифровое обозначение.
Свойства, масса и размер
Массовое число — это сумма нейтронов и протонов в ядре атома.
Размеры атомов крайне малы. Самым маленьким по размеру считается атом Гелия, его радиус составляет 32 пикометра. Атом цезия является самым большим, его радиус равен 225 пикометров. Пико = \(10^\) . А радиус ядра в 10 000 раз меньше радиуса атома.
Электронно-графическая формула
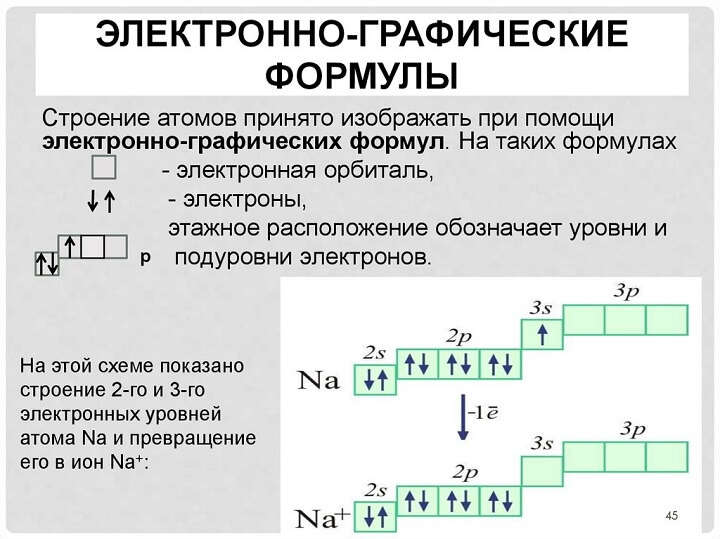
Периодическая система и строение атома, какая взаимосвязь
В таблице Менделеева указывается относительная атомная масса химических элементов.
Количество протонов в ядре соответствует порядковому номеру химического элемента в известной таблице Менделеева. Заряд ядра — это главная характеристика атома, которая влияет на распределение вещества в таблице Менделеева.
Количество нейтронов в таблице не указывается, их можно рассчитать, вычтя из массы атома порядковый номер химического вещества (число его протонов).
Почему ядро не распадается
Науке известно 4 основных вида взаимодействия между телами и частицами:
- слабое;
- сильное;
- электромагнитное;
- гравитационное.
Внутри атома, в его ядре, между протонами и нейтронами существует сильное взаимодействие, которое не позволяет ядру с легкостью распадаться. В середине XX века человечество обнаружило, что при расщеплении ядер происходит высвобождение огромной энергии, что послужило толчком для развития атомной промышленности и ядерного оружия.
Атомистическая теория — не самая сложная тема, которая есть в физике и химии. Если столкнулись с заданиями посложнее и не понимаете, с чего начать, ищите помощи у специалистов Феникс.Хелп!
Читайте также:

