Формула как сделать водород
Добавил пользователь Skiper Обновлено: 05.10.2024
Одноатомная форма водорода — самое распространённое химическое вещество во Вселенной, составляющее примерно 75 % всей барионной массы. Звёзды, кроме компактных, в основном состоят из водородной плазмы. Самый лёгкий из элементов периодической таблицы.
Три изотопа водорода имеют собственные названия: 1 H — протий, 2 H — дейтерий и 3 H — тритий (радиоактивен). Ядро самого распространённого изотопа — протия — состоит из одного только протона и не содержит нейтронов.
При стандартных температуре и давлении водород — бесцветный, не имеющий запаха и вкуса, нетоксичный двухатомный газ (химическая формула — H2), который в смеси с воздухом или кислородом горюч и крайне пожаро- и взрывоопасен [4] . В присутствии других окисляющих газов, например фтора или хлора, водород также взрывоопасен. Поскольку водород охотно формирует ковалентные связи с большинством неметаллов, большая часть водорода на Земле существует в молекулярных соединениях, таких как вода или органические вещества. Водород играет особенно важную роль в кислотно-основных реакциях.

Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
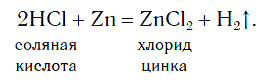
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:
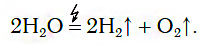
Из уравнения процесса разложения следует, что из 2 моль воды образуются 2 моль водорода и 1 моль кислорода. Следовательно, и соотношение объемов этих газов также равно:
![]()
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
![]()
Существуют и другие промышленные способы получения водорода.
Применение водорода
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 о С. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.

В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
- В лаборатории водород получают действием кислот на металлы.
- В промышленности для получения водорода используют доступное и дешевое сырье — природный газ, воду.
- Водород — это перспективный источник энергии XXI в.

Удорожание энергоносителей стимулирует поиск более эффективных и дешевых видов топлива, в том числе на бытовом уровне. Более всего умельцев–энтузиастов привлекает водород, чья теплотворная способность втрое превышает показатели метана (38.8 кВт против 13.8 с 1 кг вещества). Способ добычи в домашних условиях, казалось бы, известен – расщепление воды путем электролиза. В действительности проблема гораздо сложнее. Наша статья преследует 2 цели:
- разобрать вопрос, как сделать водородный генератор с минимальными затратами;
- рассмотреть возможность применения генератора водорода для отопления частного дома, заправки авто и в качестве сварочного аппарата.
Краткая теоретическая часть
Водород, он же hydrogen, – первый элемент таблицы Менделеева – представляет собой легчайшее газообразное вещество, обладающее высокой химической активностью. При окислении (то бишь, горении) выделяет огромное количество теплоты, образуя обычную воду. Охарактеризуем свойства элемента, оформив их в виде тезисов:

- Горение водорода – процесс экологически чистый, никаких вредных веществ не выделяется.
- Благодаря химической активности газ в свободном виде на Земле не встречается. Зато в составе воды его запасы неиссякаемы.
- Элемент добывается в промышленном производстве химическим способом, например, в процессе газификации (пиролиза) каменного угля. Зачастую является побочным продуктом.
- Другой способ получения газообразного водорода – электролиз воды в присутствии катализаторов – платины и прочих дорогих сплавов.
- Простая смесь газов hydrogen + oxygen (кислород) взрывается от малейшей искры, моментально высвобождая большое количество энергии.
Для справки. Ученые, впервые разделившие молекулу воды на hydrogen и oxygen, назвали смесь гремучим газом из-за склонности к взрыву. Впоследствии она получила название газа Брауна (по фамилии изобретателя) и стала обозначаться гипотетической формулой ННО.

Раньше водородом наполняли баллоны дирижаблей, которые нередко взрывались
Из вышесказанного напрашивается следующий вывод: 2 атома водорода легко соединяются с 1 атомом кислорода, а вот расстаются весьма неохотно. Химическая реакция окисления протекает с прямым выделением тепловой энергии в соответствии с формулой:
Здесь кроется важный момент, который пригодится нам в дальнейшем разборе полетов: hydrogen вступает в реакцию самопроизвольно от возгорания, а теплота выделяется напрямую. Чтобы разделить молекулу воды, энергию придется затратить:
Это формула электролитической реакции, характеризующая процесс расщепления воды путем подведения электричества. Как это реализовать на практике и сделать генератор водорода своими руками, рассмотрим далее.
Создание опытного образца
Чтобы вы поняли, с чем имеете дело, для начала предлагаем собрать простейший генератор по производству водорода с минимальными затратами. Конструкция самодельной установки изображена на схеме.
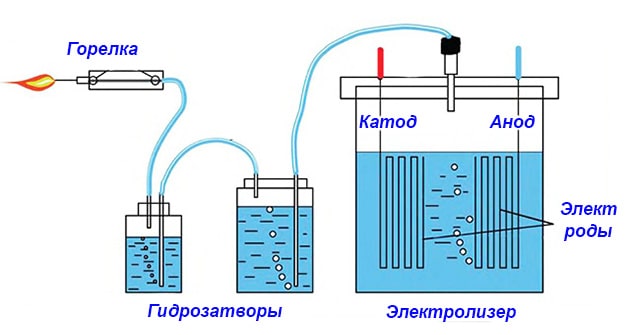
Из чего состоит примитивный электролизер:
- реактор – стеклянная либо пластиковая емкость с толстыми стенками;
- металлические электроды, погружаемые в реактор с водой и подключенные к источнику электропитания;
- второй резервуар играет роль водяного затвора;
- трубки для отвода газа HHO.
Важный момент. Электролитическая водородная установка работает только от постоянного тока. Поэтому в качестве источника питания применяйте сетевой адаптер, автомобильное зарядное устройство или аккумулятор. Электрогенератор переменного тока не подойдет.
Принцип работы электролизера следующий:
Чтобы своими руками сделать показанную на схеме конструкцию генератора, потребуется 2 стеклянных бутылки с широкими горлышками и крышками, медицинская капельница и 2 десятка саморезов. Полный набор материалов продемонстрирован на фото.

Из специальных инструментов потребуется клеевой пистолет для герметизации пластиковых крышек. Порядок изготовления простой:
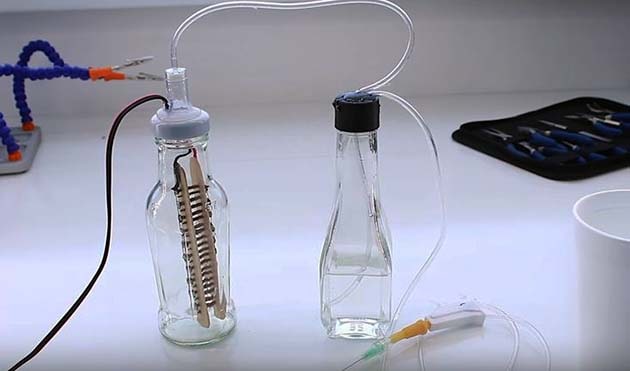
- Плоские деревянные палочки скрутите саморезами, располагая их концами в разные стороны. Спаяйте головки шурупов между собой и подсоедините провода – получите будущие электроды.
- Проделайте отверстие в крышке, просуньте туда разрезанный корпус капельницы и провода, затем герметизируйте с 2 сторон клеевым пистолетом.
- Поместите электроды в бутылку и завинтите крышку.
- Во второй крышке просверлите 2 отверстия, вставьте трубки капельниц и накрутите на бутылку, заполненную обычной водой.
Для запуска генератора водорода налейте в реактор подсоленную воду и включите источник питания. Начало реакции ознаменуется появлением пузырьков газа в обеих емкостях. Отрегулируйте напряжение до оптимального значения и подожгите газ Брауна, выходящий из иглы капельницы.
Второй важный момент. Слишком высокое напряжение подавать нельзя — электролит, нагревшийся до 65 °С и более, начнет интенсивно испаряться. Из-за большого количества водяного пара разжечь горелку не удастся. Подробности сборки и запуска импровизированного водородного генератора смотрите на видео:
О водородной ячейке Мейера
Если вы сделали и испытали вышеописанную конструкцию, то по горению пламени на конце иглы наверняка заметили, что производительность установки чрезвычайно низкая. Чтобы получить больше гремучего газа, нужно изготовить более серьезное устройство, называемое ячейкой Стэнли Мейера в честь изобретателя.
Принцип действия ячейки тоже основан на электролизе, только анод и катод выполнены в виде трубок, вставляющихся одна в другую. Напряжение подается от генератора импульсов через две резонансные катушки, что позволяет снизить потребляемый ток и увеличить производительность водородного генератора. Электронная схема устройства представлена на рисунке:
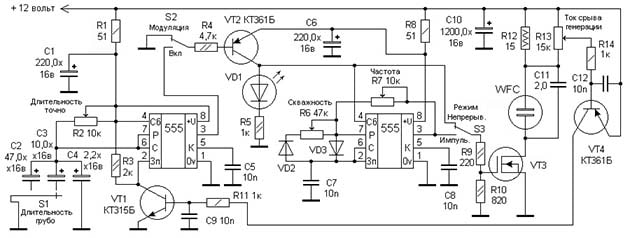
Для изготовления ячейки Мейера потребуется:
- цилиндрический корпус из пластмассы или оргстекла, умельцы нередко используют водопроводный фильтр с крышкой и патрубками;
- трубки из нержавеющей стали диаметром 15 и 20 мм длиной 97 мм;
- провода, изоляторы.

Нержавеющие трубки крепятся к основанию из диэлектрика, к ним припаиваются провода, подключаемые к генератору. Ячейка состоит из 9 или 11 трубок, помещенных в пластиковый либо плексигласовый корпус, как показано на фото.

Под ячейку Мейера можно приспособить готовый пластиковый корпус от обычного водопроводного фильтра
Соединение элементов производится по всем известной в интернете схеме, куда входит электронный блок, ячейка Мейера и гидрозатвор (техническое название – бабблер). В целях безопасности система снабжена датчиками критического давления и уровня воды. По отзывам домашних умельцев, подобная водородная установка потребляет ток порядка 1 ампера при напряжении 12 В и обладает достаточной производительностью, хотя точные цифры отсутствуют.
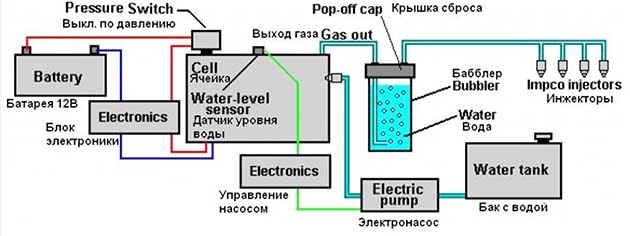
Принципиальная схема включения электролизера
Реактор из пластин
Высокопроизводительный генератор водорода, способный обеспечить работу газовой горелки, выполняется из нержавеющих пластин размером 15 х 10 см, количество – от 30 до 70 шт. В них просверливаются отверстия под стягивающие шпильки, а в углу выпиливается клемма для присоединения провода.

Кроме листовой нержавейки марки 316 понадобится купить:
- резина толщиной 4 мм, стойкая к воздействию щелочи;
- концевые пластины из оргстекла либо текстолита;
- шпильки стяжные М10—14;
- обратный клапан для газосварочного аппарата;
- фильтр водяной под гидрозатвор;
- трубы соединительные из гофрированной нержавейки;
- гидроокись калия в виде порошка.
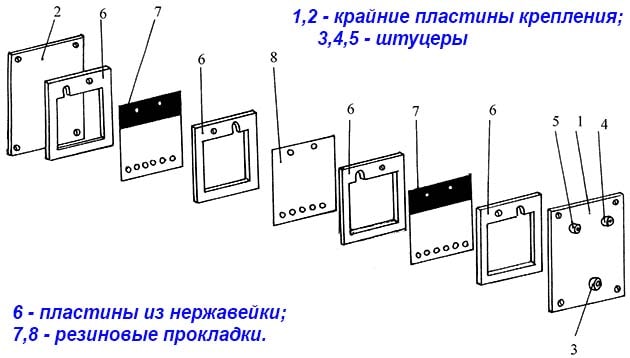
Пластины нужно собрать в единый блок, изолировав друг от друга резиновыми прокладками с вырезанной серединой, как показано на чертеже. Получившийся реактор плотно стянуть шпильками и подключить к патрубкам с электролитом. Последний поступает из отдельной емкости, снабженной крышкой и запорной арматурой.
Примечание. Мы рассказываем, как сделать электролизер проточного (сухого) типа. Реактор с погружными пластинами изготовить проще – резиновые прокладки ставить не нужно, а собранный блок опускается в герметичную емкость с электролитом.
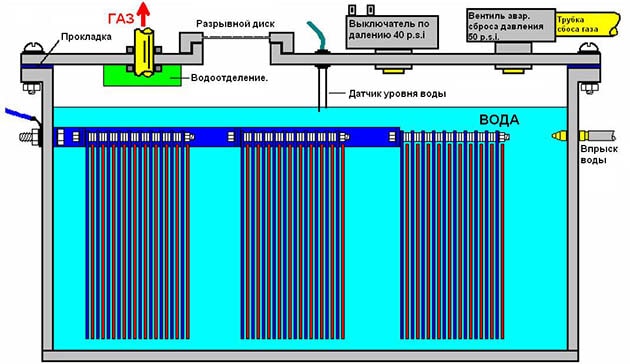
Схема водородной установки мокрого типа
Последующая сборка генератора, производящего водород, выполняется по той же схеме, но с отличиями:
Для питания реактора проще всего задействовать сварочный инвертор, электронные схемы собирать не нужно. Как устроен самодельный генератор газа Брауна, расскажет домашний мастер в своем видео:
Выгодно ли получать водород в домашних условиях
Ответ на данный вопрос зависит от сферы применения кислородно-водородной смеси. Все чертежи и схемы, публикуемые различными интернет-ресурсами, рассчитаны на выделение газа HHO для следующих целей:
- использовать hydrogen в качестве топлива для автомобилей;
- бездымно сжигать водород в отопительных котлах и печах;
- применять для газосварочных работ.
Главная проблема, перечеркивающая все преимущества водородного топлива: затраты электричества на выделение чистого вещества превышают количество энергии, получаемое от его сжигания. Что бы ни утверждали приверженцы утопичных теорий, максимальный КПД электролизера достигает 50%. Это значит, что на 1 кВт полученной теплоты затрачивается 2 кВт электроэнергии. Выгода – нулевая, даже отрицательная.

Вспомним, что мы писали в первом разделе. Hydrogen – весьма активный элемент и реагирует с кислородом самостоятельно, выделяя уйму тепла. Пытаясь разделить устойчивую молекулу воды, мы не можем подвести энергию непосредственно к атомам. Расщепление производится за счет электричества, половина которого рассеивается на подогрев электродов, воды, обмоток трансформаторов и так далее.
Важная справочная информация. Удельная теплота сгорания водорода втрое выше, чем у метана, но – по массе. Если сравнивать их по объему, то при сжигании 1 м³ гидрогена выделится всего 3.6 кВт тепловой энергии против 11 кВт у метана. Ведь водород – легчайший химический элемент.
Теперь рассмотрим гремучий газ, полученный электролизом в самодельном водородном генераторе, как топливо для вышеперечисленных нужд:
Для справки. Чтобы сжигать гидроген в отопительном котле, придется основательно переработать конструкцию, поскольку водородная горелка способна расплавить любую сталь.
Заключение
Гидроген в составе газа ННО, полученный из самодельного водородного генератора, пригодится для двух целей: экспериментов и газосварки. Даже если отбросить низкий КПД электролизера и затраты на его сборку вместе с потребляемым электричеством, на обогрев здания попросту не хватит производительности. Это касается и бензинового двигателя легковой машины.
53 Replies to “Как сделать генератор водорода в домашних условиях”
Спасибо за Ваше замечание по количеству трубок.
В статье не стоит задача что-то доказывать. Излагается ситуация на данный момент и общее руководство по изготовлению генератора — ежели кто захочет.
Получать горючий газ HHO можно по методу (реакция) Марсоля, разлагая воду на цинке и сурьме, всё.
Боюсь, этот метод ничем не лучше других. Если изучить скудную информацию по данной теме, то в глаза сходу бросается 3 нестыковки:
1. Вода в молекулярном двигателе Марсоля разлагается на кислород и водород, минуя паровую фазу. Нонсенс.
2. Насос и сопротивление затрачивает электричество, поршень совершает механическую работу. Каково соотношение затраченной и полученной энергии, неизвестно.
3. Потери теплоты в насосе и молекулярном двигателе неизбежны.
Сдается мне, разложение электролизом куда перспективнее.
Все очень даже работает, я езжу на 3-литровом моторе с расходом в 7-8 литров самого дешманского бензина. И что радует помимо экономии, что в конях прибавка около 15%,так что жизнь налаживается, да и ресурс мотора до 40% увеличивается, вот как-то так!
Да статья интересная,а еще интереснее как работают автомобильные газогенераторы. Ведь как уже слышно налаживается серийный выпуск автомобилей на водородном топливе заправляемые обычной водой,то есть там стоит газогенератор и как слышал и КПД намного выше.
Есть ещё один важный момент, который не рассмотрен в статье: это увеличение эффективности природных источников энергии с помощью электролиза. Как известно, для получения солнечной энергии можно использовать солнечные панели, либо коллекторы. Но эти решения трудно использовать для отопления, так как солнце наиболее интенсивно светит днём и летом, а топить нужно зимой и ночью. Потому напрямую греть ТЭН от солнечной панели не получится.
Чтобы запасать энергию, используются аккумуляторы, но у них низкий КПД и короткий срок службы в циклическом режиме.
И тут интересно рассмотреть возможность использования электролиза для запасания солнечной (или ветровой) энергии. Например летом на солнце использовать электричество солнечной панели, чтобы получить запас водорода, а ночью зимой этот водород сжигать в водородном котле. То что у системы низкий КПД — в этом случае не важно, солнца ведь и так много. Гораздо важнее насколько безопасно получится запасать водород в больших объёмах, чтобы потом использовать по мере необходимости.
Ваша идея запасать водород на ночь, используя солнечную энергию днем, действительно интересна. В статье мы не рассматривали эту возможность, потому что никто не применял подобную схему на практике. Во всяком случае, нам неизвестны такие факты. Ну и конечно, надо считать выгоду – во сколько обойдется производство водорода днем (плюс стоимость оборудования) и обычное отопление по ночному тарифу.
Мной давно рассмотрена идея синтеза водорода при помощи гибрида ветряка и солнечными элементами, последующим электролизом и связыванием водорода в гидрид алюминия.
То что водородная установка работает это 100% правда , я сам ими занимался 25 лет назад. Вопрос только в том кто вам даст этим заниматься ? Нефтеные магнаты тоже хотят кушать и они вас съедят за эти установки. 2 вопрос , куда вы денете миллионы безработных которых уволят с нефтеперерабатывающих заводов?
Установка РАБОТАЕТ.
То, что установка работает известно давно. Ещё в СССР хотели запустить автобусы на водороде. Не дали, по причине причинения вреда экономике.
Для повышения КПД, наверно, надо генератор с частотой резонансной колебательной частоте молекулы воды.
И мне если можно . Разрабатываю газообразный водород в сухой для овощных зерновых культур
Поделитесь чертежами пожалуйста,мне для отопления дома.Можете?
А если водород собирать из системы водяного отопления, которая работает на электричестве. У которой в котле вместо электроТЭНов будет стоять реактор из пластин?
Не думаю, что это хорошая идея. Львиная доля энергии будет расходоваться на нагрев теплоносителя, который постоянно идет из системы отопления. Водорода выделится мизер, и как его улавливать? На выходе воздухоотводчика?? Да и смысл этим заниматься, если все равно греем воду электрокотлом.
Для чего надо лезть в мировую экономику, просто создать для себя комфортные условия проживания, а на остальных плевать нет народа в стране у всех хата скраю, Сибирь горит и лес миллионами кубометров вывозят, а народишку наплевать, так и тут, сделал для себя и плюй в потолок:)
Представьте себе, человек включает в сеть прибор, опускает его в колбу с водой и по всему дому загораются лампочки, работают электроплита и стиральная машина. И в результате работы прибора отходами является вода, которую завтра вновь можно использовать. Фантастика? Не совсем. В мировых лабораториях ученые работают над получением альтернативного топлива. И водородное топливо — одно из наиболее перспективных в этом плане.
Сейчас, когда вещества окружающего мира разложены на атомы, а человек стремится заглянуть внутрь ядра, водород и другие газы хорошо изучены. Древние алхимики, из-за невидимости газов, не учитывали участие воздуха в проводимых реакциях. И только со временем к ученым пришло понимание, что воздушные газы — полноценные участники химических реакций, и без их исследования картина мира будет неполной.
У истоков завтрашних изобретений стоят исследования ученых XVI-XVII вв и теория о флогистоне — некой горючей субстанции, что улетучивается из веществ при горении, смешивается с воздухом и не может быть выделена из него.
В 1703 году теория флогистона описана немецким ученым Георгом Шталем для объяснения процессов горения, восстановления и обжига.
Лавуазье во второй половине восемнадцатого века осуществили водный синтез водорода с помощью горячего железа, что доказало присутствие водорода в составе воды.
Водород (Hydrogenium) — рождающий воду. Обозначается латинской литерой Н. Вселенная на 75% состоит из водорода, и на остальные 93 природных элемента, присутствующих в таблице Менделеева приходятся остальные 25%. На Земле — его позиция скромнее, девятый по распространенности. Водород входит в состав воды, благодаря круговороту которой поддерживается жизнь на земле.
Физические свойства водорода
не обладает цветом,
не ощутим вкусовыми и обонятельными рецепторами человека ( NB! Помним, что пробовать в лаборатории ничего нельзя!)
кипит и плавится при отрицательных температурах. (-252,6 0С и -259,2 0С соответственно);
в сравнении с воздухом, водород легче практически в 14 раз;
из-за неполярности молекулы Н2, водород плохо растворим в воде,
некоторые металлы (палладий) могут абсорбировать атомарный водород с образованием гидридов металлов..
Формулы получения водорода
1. Реакция металлов с разбавленными кислотами:
Zn +2HCl → ZnCl2 +H2↑
Для получения водорода используется аппарат Киппа. Представлен на странице 73 учебника “Химия 8 класс” под редакцией Н.Е.Кузнецовой
2. Реакция щелочных и щелочноземельных металлов с водой:
2Na +2H2O → 2NaOH +H2↑
3. Реакции гидролиза гидридов:
NaH +H2O → NaOH +H2↑
СаH2 + 2Н2О = Са(ОН)2 + 2Н2↑
4.Реакции цинка, кремния или алюминия со щелочами:
2Al +2NaOH +6H2O → 2Na[Al(OH)4] +3H2↑
Si + 2NaOH + H2O → Na2SiO3 + 2H2
Zn +2KOH +2H2O → K2[Zn(OH)4] +H2↑
5. Электролиз воды.
2H2O → 2H2+О2
Не смотря на то, что в результате электролиза получается чистый водород, экономически этот способ самый дорогой.

1. Взаимодействие с галогенами.
При обычной температуре водород реагирует со фтором:
H2 + F2 = 2HF.
Яркий свет обеспечивает реакцию водорода с хлором с выделением хлороводорода, взаимодействие с бромом протекает не так активно, водород с йодом не реагирует до конца даже при высокой температуре.
2. Взаимодействие с кислородом.
Горение водорода в кислороде - экзотермическая реакция. Температура водородно-кислородного пламени достигает почти 3000 °С.
Читайте также:

