Как сделать модель атома гелия
Обновлено: 07.07.2024
Практически все знания об элементарных частицах материи получены наукой с помощью различного рода ускорителей (синхрофазатроны, теватроны,бетатроны,коллаидеры…). В этих ускорителях, элементарные частицы разгоняются до высоких скоростей и ударяются в другие частицы. В результате, получаются “новые” “элементарные частицы”, с другими характеристиками.
Отсюда делается вывод: элементарных частиц материи много во вселенной.
Но, почему-то никто не задумывается, что в результате такого жесткого столкновения элементарная частица материи может разрываться. Точнее: наука даже не допускает этой мысли. Элементарная частица, в господствующей модели, цельна и неделима.
Наука потому и является “наукой”, что она должна изучать все варианты. Иначе получаем типичное средневековье: “Так думать запрещено!”
Представим, ч то всё многообразие “элементарных частиц материи”, полученных в результате опытов на различных ускорителях, есть результат разрыва элементарных частиц только одного типа – протона.
Протон – единственная настоящая элементарная частица материи,существующая во вселенной. Все остальные “элементарные частицы” – есть результат жесткого воздействия на протон и его разрыва. Полностью о строении протона и как он разрывается можно прочесть в статье “Фундаментальные взаимодействия материи и энергии“
В данной статье мы в сжатой форме рассмотрим: по каким правилам и закономерностям природа формирует атомы химических элементов. Этих правил и закономерностей четырнадцать. (Подробно и более научно материал раскрыт в статьях,- в указанных, ниже, ссылках).
Итак, эти правила и закономерности:

- В виде стрелки изображена элементарная частица материи.
- Оконечность стрелки указывает направление её движения.
2. Элементарная частица представляет собой диполь . Она обладает как силой притяжения, так и силой отталкивания. На рисунке показано разграничение зон действия этих сил:
- Зона действия сил притяжения: передняя (по ходу движения) полусфера пространства.
- Зона действия сил отталкивания: задняя (по ходу движения) полусфера пространства.
Такое распределение зон действия сил объясняет абсолютно все материальные взаимодействия во вселенной:
- и гравитационные,
- и ядерные,
- и сильные,
- и слабые,
- и химические, электрические, механические… – абсолютно все.
В первую очередь: позволяет элементарным частицам объединяться в атомы.
3. Элементарные частицы материи, сближаясь, образуют парную структуру из элементарных частиц – атом дейтерия. Эта парная структура – атом дейтерия – есть тот самый “строительный блок”, их которого построены атомы всех химических элементов таблицы Менделеева.
схематичное изображение атома дейтерия

Именно из парной структуры из двух элементарных частиц, а не из структуры “протон + нейтрон” состоят все химические элементы во вселенной. (Подробно, как парная структура “превращается” в протон, нейтрон и электрон, можно прочитать в статье “Атомное строение веществ“)
На рисунке мы видим схематическое изображение такой парной структуры – атом дейтерия.
Что сразу бросается в глаза:
- Изменяются зоны действия сил притяжения и отталкивания. Зона действия сил отталкивания увеличилась, а зона действия сил притяжения сузилась. Подчеркиваю: изменились зоны действия сил, но никак – не их соотношение.
4. Правило стандартной скорости: фрмированию атомов каждого химического элемента соответствует своя, строго определенная скорость поступательного движения галактики в пространстве вселенной.
- Сразу после Большого взрыва галактики, галактика состояла только из одиночных элементарных частиц материи – или атомов протия.
- Затем, по мере разгона галактики, элементарные частицы материи объединяются в парные структуры – атомы дейтерия. Это значит, что галактика достигла стандартной скорости образования атомов дейтерия.
- Далее, в какой-то момент галактика достигает стандартной скорости образования атома гелия. Атом гелия образуется в результате объединения двух парных структур в счетверенную структуру из элементарных частиц.
- Затем галактика достигает скорости образования атомов лития, затем – бериллия, бора, углерода… К атому гелия, поочередно, присоединяется по одной парной структуре.
Такая закономерность – есть следствие непрерывного ускорения галактики в пространстве вселенной. На это указывают последние научные данные.
5. В первую очередь, две парные структуры объединяются в атом гелия. Счетверенная структура из элементарных частиц – атом гелия – входит в состав всех атомов всех химических элементов как первый период. И находится в центре структуры всех атомов.
схема атома гелия
Здесь мы видим такое же разграничение зон действия сил притяжения и отталкивания. Силы притяжения атома действуют в передней (по ходу движения) полусфере, а отталкивания – в задней полусфере движения.
6. Здесь мы подходим к важнейшему правилу формирования атомов химических элементов:
Все элементарные частицы (парные структуры) одного периода в составе атома располагаются строго в одной плоскости . И имеют общий вектор поступательного движения.
Это четко видно уже на рисунке атома гелия. Все оконечности стрелок – передних оконечностей элементарных частиц материи – располагаются строго в одной плоскости. Эта плоскость – есть линия разграничения сил притяжения и отталкивания атома гелия.
7. Каждый период в составе атома представляет собой кольцо из парных структур.И располагается вокруг оси, центром которого является счетверенная структура атома гелия.
Понятно, что силы притяжения и отталкивания падают, по мере удаления от элементарной частицы. Понятно, что это падение распространяется от центра – к периферии. То есть – имеет форму шара или окружности. Вот и получаем форму расположения парных структур вокруг центра атома – в виде окружности – кольца.
При этом, выполняется закономерность:
8. Все парные структуры одного периода располагаются строго симметрично относительно друг друга и вокруг центра атома.
Например, атом углерода имеет такую структуру:

Здесь первый период представляет собой счетверенную структуру – атом гелия. Во втором периоде мы видим четыре парные структуры. Которые симметрично расположены относительно центра атома.
9. Следующая закономерность построения структуры атома: Атом всегда выступает по отношению к последнему периоду как единое целое.
В приведенной схеме атома углерода, счетверенная структура атома гелия выступает как единое целое по отношению ко второму периоду.
Можем рассмотреть элементы третьего периода. В них единым целым, по отношению к третьему периоду, будет выступать первый плюс второй периоды. К четвертому строящемуся периоду единым целым выступают первый плюс второй, плюс третий периоды. И так далее…
10. Следующая закономерность построения структуры атомов: На определенном расстоянии от центра атома может располагаться только определенное количество парных структур.
То есть: во втором – третьем периодах – по восемь парных структур. В четвертом – пятом – по весемнадцать. В шестом – седьмом – по тридцать две.
Каждая парная структура, присоединяясь к атому, увеличивает и силу отталкивания атома. Благодаря чему последний строящийся период отодвигается на большее расстояние от центра атома.
11. Расстояния между периодами в атоме намного превышают расстояния между парными структурами внутри периода. Отсюда и следует закономерность: каждый период относится к атому, как единая цельная структура.
При реакции ядерного распада, например, атом радиоактивного химического элемента отторгает целиком последний период. В результате остаются: атом инертного газа и химический элемент второго периода – по числу оставшихся парных структур.
12. Очень важная закономерность: Сила притяжения атома действует только в передней, по ходу движения атома, полусфере пространства. Сила отталкивания атома действует только в задней, по ходу движения атома, полусфере пространства.
Атом всегда ориентирован в пространстве вперед своими последники периодами. То есть – своей широкой частью.
Он, как воронка, своим “раструбом” притягивает (как бы “всасывает”) к себе материальные частицы. В то же время, силы отталкивания “расположены” снаружи “воронки”
Вспомним распределение зон действия сил притяжения и отталкивания протия и дейтерия. И перенесем их на структуру более сложного атома. Например: аргона.
строение атома аргона

- Первое, что мы видим: все три периода атома кольцами расположены вокруг общей оси атома. Эта ось изображена на схеме в виде пунктирной стрелки.
- Периоды в атоме расположены каскадом: в основании – первый период (счетверенная структура атома гелия). Вокруг него, в одной плоскости – кольцо второго периода. И выше – каскадным кольцом – плоскость кольца третьего периода.
- Причем, парные структуры внутри периодов строго ориентированы.
- диаметр кольца третьего периода больше диаметра кольца второго периода.
- Точно таким же каскадом располагаются и четвертый – пятый, и шестой – седьмой периоды.
На нижеприведенной рисунке мы видим, как бы “разрез” колец второго и третьего периодов атома. Главное: здесь мы видим разную пространственную ориентацию элементарных частиц.
- Пространственная ориентация парных структур второго периода почти совпадает с направлением движения атома (пунктирная стрелка).
- Пространственная ориентация парных структур третьего периода почти перпендикулярна направлению движения атома.
Благодаря такой ориентации мы видим одинаковое количество парных структур в четвертом – пятом и шестом – седьмом периоде.
Точно также ориентированы друг к другу и к центру атома парные структуры четвертого – пятого и шестого – седьмого периодов.
Таков результат распределения зон сил отталкивания и притяжения.

13. В результате и получаем: Атом имеет плоско – каскадную структуру, напоминающую по форме люстру.
- Своим широким концом, как раструбом, “люстра” – атом – притягивает к себе другие материальные частицы. Здесь расположена зона действия сил притяжения.
- С обратной стороны: позади “люстры” – атома располагается зона действия сил отталкивания.
Таким образом, зона действия сил притяжения атома напоминает конус. Своим “острием” этот “конус” направлен внутрь атома.
А зона действия сил отталкивания напоминает полушарие, “обхватившее” снаружи “люстру” – атом.
14. Плоско – каскадная структура атома способна изменяться. Изменяться, в зависимости от температуры и давления. Это четко проявляется в явлении “сверхпроводимость“.
Сверхпроводимость в проводниках возникает, когда их охлаждают до сверхнизких температур – близких к абсолютному нулю. Что в это время происходит с атомами?
- Плоско – каскадная структура атома сначала “выпрямляется” до плоской, а, затем – “выгибается” в обратную сторону. То есть: зона действия сил притяжения стремительно растет. Из конусовидной она стремится к шаровидной форме. А зона действия сил отталкивания наоборот: стремительно уменьшается. От шаровидной формы – к конусообразной.
- Расстояния между периодами начинают уменьшаться.
Атом сжимается и “выворачивается наизнанку”. Это и ведет к сверхпроводимости.
Итак, мы рассмотрели правила и закономерности построения структуры атомов. Их четырнадцать:
- Элементарная частица материи имеет форму вытянутой, в пространстве, нити.
- Элементарная частица материи обладает и силой притяжения, и силой отталкивания.
- Парная структура из элементарных частиц – есть тот самый “кирпичик”, из которых построены все атомы всех химических элементов таблицы Менделеева.
- Правило стандартной скорости: образованию каждого химического элемента соответствует своя, строго определенная скорость поступательного движения галактики в пространстве вселенной.
- Счетверенная структура из элементарных частиц входит в состав всех атомов всех химических элементов во вселенной как первый период.
- Все элементарные частицы (парные структуры) одного периода в составе атома располагаются строго в одной плоскости.
- Каждый период в составе атома представляет собой кольцо из парных структур.И располагается вокруг оси, центром которого является счетверенная структура атома гелия.
- Все парные структуры одного периода располагаются строго симметрично относительно друг друга вокруг центра атома.
- Атом всегда выступает по отношению к последнему строящемуся периоду как единое целое.
- На определенном расстоянии от центра атома может располагаться только определенное количество парных структур.
- Расстояния между периодами в атоме намного превышают расстояния между парными структурами внутри периода.
- Сила притяжения атома действует только в передней, по ходу движения атома, полусфере пространства. Сила отталкивания атома действует только в задней, по ходу движения атома, полусфере пространства.
- Атом имеет плоско – каскадную структуру, напоминающую по форме люстру.
- Плоско – каскадная структура атома способна изменяться.
Подробно обо всех указанных закономерностях построения атома можно прочитать в статьях:
Порядок заполнения оболочек атома гелия (He) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ - до 6, на ‘d’ - до 10 и на ‘f’ до 14
Гелий имеет 2 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
Степень окисления гелия
Атомы гелия в соединениях имеют степени окисления 0.
Степень окисления - это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Ионы гелия
Валентность He
Атомы гелия в соединениях проявляют валентность .
Валентность гелия характеризует способность атома He к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Валентность не имеет знака.
Квантовые числа He
Квантовые числа определяются последним электроном в конфигурации, для атома He эти числа имеют значение N = 1, L = 0, Ml = 1, Ms = -½
Видео заполнения электронной конфигурации (gif):

Результат:
Энергия ионизации
Чем ближе электрон к центру атома - тем больше энергии необходимо, что бы его оторвать. Энергия, затрачиваемая на отрыв электрона от атома называется энергией ионизации и обозначается Eo. Если не указано иное, то энергия ионизации - это энергия отрыва первого электрона, также существуют энергии ионизации для каждого последующего электрона.
Тем, кто интересуется химией, будет интересно узнать, что гелий — химический элемент восемнадцатой группы знаменитой таблицы Менделеева, возглавляющий группу инертных газов и идущий под вторым порядковым номером. В настоящее время это вещество получило широкую сферу применения, искусственно синтезируясь из природного газа, содержащегося в земных недрах.

Основная информация об элементе
Уникальное в своем роде вещество считается одним из самых распространенных во всей Вселенной, уступая пальму первенства в своем объеме только водороду, ведь его доля составляет около 23 процентов от общей массы этого безграничного пространства. Близкие к рекордным показатели демонстрируют и другие физические свойства гелия, которые стоит рассмотреть более подробно.
Физические особенности
Химический элемент относят к практически полностью инертным газам, он не является токсичным и не имеет вкуса и запаха. Одиночное строение атома гелия остается таковым при любых условиях, чего не скажешь о других его характеристиках, зависящих от атмосферного давления, температурного режима и многих других параметров. Самый легкий идеальный газ после водорода, гелий обладает следующими физическими свойствами:
- Молярная масса атома газа составляет 4,002601 грамма на моль. Что касается молярного объема, то этот показатель равен 31,81 сантиметра кубических на моль, тогда как молярная теплоемкость составляет 20,79 Дж/Кмоль.
- Плотность вещества напрямую зависит от температурного режима, соответствуя 0,147 грамма на сантиметр кубический при падении столбика термометра ниже отметки в минус 270 градусов Цельсия и 0,000117846 градуса при нагревании до плюс 20 градусов и выше.
- Температура кипения у гелия является наиболее низкой, если сравнивать его с любым другим химическим элементом. Так, вещество имеет свойство закипать при температуре, равной 4,2152 Кельвина, что эквивалентно минус 268,94 градуса Цельсия.
- Температурный режим плавления соответствует 0,95 Кельвина или минус 272,2 градуса Цельсия при давлении, равном 2,5 МПа. При этом удельная теплота плавления составляет 0,0138 килоДжоуля на моль при удельной теплоте испарения 0, 0829 кДж/моль.
- Получение вещества в твердом виде становится возможным только при атмосферном давлении выше 25 атмосфер, тогда как при любых других показателях (даже нулевых) он не переходит в эту фазу.
- Гелий, найденный в природных условиях, всегда состоит из двух изотопов стабильного типа, один из которых имеет высокий процент распространения, близком к сотне, тогда как другой встречается гораздо реже, причем в совершенно разных естественных источниках (до 0,00014%). Помимо прочего, науке известны еще как минимум 6 радиоактивных гелиевых изотопов искусственного происхождения.
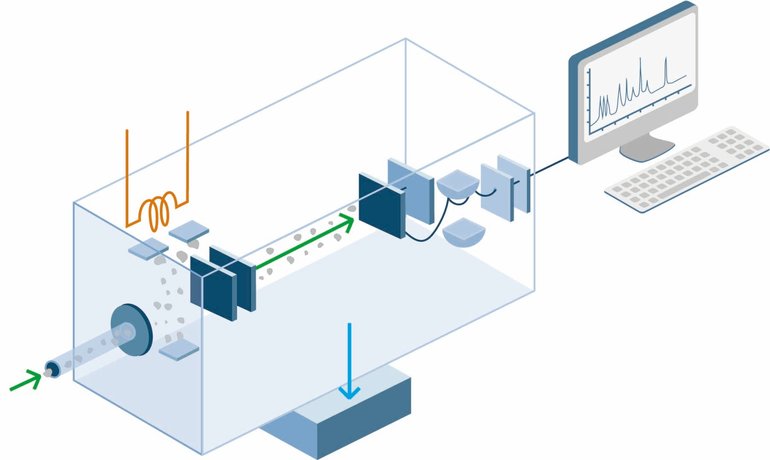
Стоит отметить, что для качественного определения вещества сегодня используется анализ эмиссионного спектра излучения, тогда как для количества применимым остается хроматографическое и масс-спектрометрическое тестирование. Кроме того, актуальными являются простейшие методы идентификации, подразумевающие измерение таких основных параметров, как плотность, молярная масса и теплопроводность.
Гелий в своем газообразном состоянии очень тяжело растворяется в воде (гораздо сложнее, чем любой другой газ). Так, в литре воды, температура которой составляет 20 градусов Цельсия, объем растворимого газа составляет не более 8,8 миллилитра из 100. Еще худшую растворимость можно наблюдать в этиловом спирте, так как ее показатель не превышает 2,8 мл/л при 15-градусной температуре и 3,2 мл при нагревании этанола до 25 градусов Цельсия.
А вот скорость диффузии гелия превышает актуальный для воздуха показатель в три раза, опережая даже водород, у которого коэффициент проникаемости ниже на 65%. Абсолютным рекордсменом гелий является и по коэффициенту преломления, максимально приближаясь к единице. Эффект Джоуля — Томсона у гелия имеет отрицательное значение в нормальной среде из-за его слишком быстрого охлаждения.
Что касается остывания в процессе дросселирования, то оно становится возможным только при 40 К и нормальном атмосферном давлении. Если же температура продолжит опускаться, то становится возможным переход гелия из газообразного в жидкое состояние, но только при условии применения охлаждения расширительного типа, обеспечить которое реально только с помощью специального преобразователя относительной потенциальной энергии в механическую.
Химические свойства

- Величина ковалентного радиуса равна 28 пм при радиусе иона, соответствующем 93 пм.
- Уровень электроотрицательности по шкале Полинга соответствует 4,5 баллам.
- Электродный потенциал, как степени окисления, а следовательно, и валентность элемента имеют нулевые значения.
- Энергия ионизации первого электрона равна 2361,3 кДж/моль.
- Показатель теплопроводности элемента соответствует 300 К.
- Молекулярная ионная энергия равна 58 ккал/моль.
- Равновесное расстояние между ядрами химически связанных элементов соответствует 1,09 А.
Что касается соединений вещества, то сегодня известной является его связь LiHe. Сам элемент имеет свойство образовывать двухатомные молекулы фторида и хлорида, обозначение первого из которых HeF, а второго HeCl, притом что их получение становится возможным только при воздействии электрического разряда или УФ-излучения на смесь описываемого элемента с фтором или хлором, соответственно.
Совершенно другими свойствами обладает гелий в газообразном состоянии. Не последнюю роль в этом вопросе играет воздействие на газ различного рода физических и химических процессов. К примеру, если пропустить ток через трубочку с гелием, то можно наблюдать его радужное свечение, сила которого будет зависеть от создаваемого давления в закрытом пространстве. Если же не прибегать к подобным приемам, то останется один только желтый спектр, считающийся привычным для гелия в его нормальном состоянии.
Ввиду содержания в веществе нескольких линий спектра по мере уменьшения атмосферного давления происходит изменение его цветового излучения, которое начинает меняться от желтого к оранжевому, розовому и зеленому. Всего же учеными принято выделять два основных спектра — единичный и триплетный, первый из которых свойственен атомам в их нормальном состоянии. Что касается перехода в триплетное состояние, то он становится возможным только при использовании разряда в 19,77 эВ.

Вывести атом из его привычного состояния можно и другими методами воздействия, один из которых заключается в искусственно созданном столкновении с другими атомами вещества с последовательной передачей энергии между ними. А вот обратный переход из триплетного состояния в синглетное естественным путем практически невозможен. Такое состояние называется метастабильным и для того, чтобы перевести газ в стандартное положение вновь, приходится прибегать к различным методам внешнего воздействия.
Интересные факты о гелии
Немного истории
Сегодня уже мало кто вспомнит, что открытие элемента произошло еще 18 августа 1868 года, когда известный французский ученый решил исследовать солнечную хромосферу в момент полного затмения звезды в одном из индийских городов. Примечательно, что всего лишь через 3 месяца такое же открытие было сделано в Англии, правда, тогда о его неактуальности еще никто не знал, ввиду более сложной корреспонденции научных данных.
В 1881 году итальянский вулканолог Луиджи Пальмери, исследовавший Везувий, также идентифицировал это вещество, поспешив сообщить о своей находке общественности. Но самое важное событие в области открытия гелия произошло 27 годами позже, когда он был впервые выявлен в недрах планеты. Тогда газ удалось добыть из такого распространенного минерала, как клевеит, и со временем именно он использовался учеными для того, чтобы установить величину его удельного веса и других физических параметров.

Со временем исследователи научились получать гелий в жидком виде, для чего впервые довелось применить процедуру дросселирования. В отличие от этого попытки добывать твердый гелий долгое время не увенчивались успехом. Ситуация изменилась только в 1926 году, когда вдобавок к охлаждению было применено и критическое понижение атмосферного давления до 35 атм, в результате чего удалось выделить кристаллическую решетку вещества.
Получение и применение
Удивительно, но, несмотря на свое внушительное распространение во всей Вселенной, гелий довольно редко встречается на Земле. Разной является и природа образования этого элемента на Земле и в космосе, так как в первом случае его выделение происходит за счет распада альфа-частиц тяжелых элементов. В итоге часть вещества проходит через земные породы, сливаясь с природным газом и демонстрируя концентрацию от 7 процентов от общего объема и выше.
В настоящее время месторождения, в которых наблюдаются большие залежи гелия, имеются на территории таких стран, как Индия, Бразилия, Россия и Танзания. Естественно, речь идет о гелийсодержащих газах, которые используются в промышленности для выведения чистого элемента или его производных. Для этого применяется процедура охлаждения посредством дросселирования, и в этом случае сложность разжижения элемента в значительной мере облегчает процесс.
На выходе удается получить смесь, состоящую не только из гелия, но и из водорода и неона, после чего производится очистка. В итоге доля сырого гелия будет составлять около 70−90 процентов от общего объема. После финишной фильтрации продукт, который, как известно, не может гореть, а следовательно, и не представляет никакой угрозы, транспортируясь в металлических баллонах, изготовленных в соответствии с ГОСТ 949–73 . Если же стоит вопрос о перевозке сжиженного газа, то в ход идут специальные сосуды марки СТГ-10 и СТГ-25.

Что касается применения, то гелий используется в следующих сферах:
- Металлургия.
- Пищевая промышленность.
- Для изготовления хладагентов для различных агрегатов и рабочих установок.
- Для наполнения различных судов воздухоплавания и шариков.
- В дайвинге для приготовления дыхательных смесей, необходимых для погружения.
- В ракетных установках в качестве одной из составляющих теплоносителя.
- Для наполнения трубок газорезного типа.
- В сфере газовой хроматографии.
- Для поиска утечек в трубопроводах и всевозможных инфраструктурных установках.
Естественно, на этом применение элемента не заканчивается, ввиду чего производство гелия является очень развитым и востребованным в настоящее время.

Среди прочих преимуществ газа — его высокие перспективы в сфере термоядерной энергетики, благо, мировые запасы гелийсодержащих веществ не позволяют отнести его в разряд дефицитного.
Так, современные эксперты называют цифру в 45,6 миллиарда метров кубических, притом что объемы производства перевалили за 110 миллионов еще в 2003 году.
Курс элементарной физики принято заканчивать атомом водорода, хотя во Вселенной существуют гелий, литий и другие атомы. Рассмотрим коротко устройство атома гелия, который по-своему интересен. Известно, что ядро гелия содержит два протона и два нейтрона. Физики называют его ?-частицей. Атом гелия должен содержать два электрона, чтобы компенсировать двойной положительный заряд ядра. Гелий образуется примерно так. Сначала в результате каких-то ядерных реакций возникает свободная ?-частица. Попав в облако электронов, ?-частица захватывает электрон, который начинает вращаться вокруг неё по сферали, разрешённой для атома гелия. При этом образуется ион гелия, состоящий из ядра и одного электрона. Это напоминает атом водорода, но с другими уровнями энергии для электрона. Такое водородоподобное состояние длится недолго. Вскоре ион гелия захватывает второй электрон, чтобы стать нейтральным атомом. Возникает вопрос, на какой сферали будет находиться второй электрон, ведь первая уже как бы занята?
Из квантовой теории следует вывод, что линии водорода тоже должны быть дублетными, поскольку протону при захвате электрона безразлично направление вращения последнего. Поэтому в любой порции водорода присутствуют атомы, где ядро и электрон вращаются в одну сторону, и атомы, где они вращаются в разные стороны. При наложении спектров этих атомов их линии попадают на близкие, но разные участки. Для выявления такого расщепления требуются чувствительные спектрометры.
Из курса химии известно, что за гелием следует атом лития, который в нейтральном состоянии содержит три электрона. Два из них, имеющие противоположные магнитные моменты, образуют внутреннюю двойную оболочку, как у гелия. Для третьего электрона здесь места уже нет. Поэтому третий электрон занимает место на внешней сферали, образуя наружную сферическую оболочку. Эта структура, похожая на атом водорода, должна иметь водородоподобный спектр. Так как связь внешнего электрона с ядром ослаблена, линии спектра лития должны быть смещены в инфракрасную область.
С увеличением порядкового номера атомов вещества возрастает его плотность. В плотном (сконденсированном) состоянии внешние оболочки атомов начинают влиять друг на друга так, что меняется их форма. Так в атоме углерода (порядковый номер 6) четыре внешних электрона образуют не сферические, а веретенообразные оболочки. Это как если взять слабо надутый воздушный шар и растянуть его вдоль диаметра. Характеристикой такой оболочки является длинная ось. Атом углерода интересен тем, что длинные оси четырех оболочек внешних электронов располагаются в пространстве симметрично вдоль воображаемых диагоналей куба. Этим объясняется твердость алмаза, так как куб раздавить нелегко.
Читайте также:

