Как сделать из воздуха кислород
Добавил пользователь Дмитрий К. Обновлено: 05.10.2024
Получение кислорода из селитры Получение кислорода из марганцовки Перекись водорода в таблетках
Для получения кислорода, потребуются вещества, которые им богаты. Это пероксиды, селитры, хлораты. Мы будем использовать те, что можно достать без особого труда.
Для получения кислорода в домашних условиях есть несколько способов, разберём их по-порядку.
Самый простой и доступный способ получения кислорода – использовать марганцовку (или более правильное название – перманганат калия). Всем известно, что марганцовка – прекрасный антисептик, используется в качестве обеззараживающего вещества. Если её нет, то можно приобрести в аптеке.
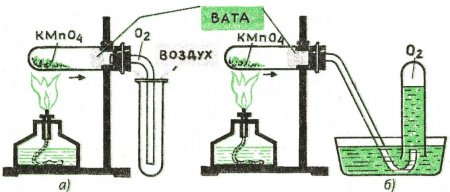
Поступим так. В пробирку насыпаем немного марганцовки, закроем пробиркой с отверстием, в отверстие установим газоотводную трубку (по ней будет идти кислород). Другой конец трубки поместим в другую пробирку (она должна располагаться вверх дном, так как выделяющийся кислород легче воздуха и будет подниматься вверх. Такой же пробкой закром вторую пробирку.
В итоге у нас должно получиться две пробирки, соединённые между собой газоотводной трубкой через пробки. В одной (неперевёрнутой) пробирке - марганцовка. Будем нагревать пробирку с марганцовкой. Тёмно-фиолетово-вишнёвый цвет кристалликов марганцовки исчезнет и превратится в тёмно-зелёные кристаллы манганата калия.
Реакция протекает так:
Так из 10 грамм марганцовки можно получить почти 1 литр кислорода. Через пару минут можно извлечь колбу с марганцовкой из пламени. Мы получили кислород в перевёрнутой пробирке. Можем его проверить. Для этого аккуратно отсоединим вторую трубку (с кислородом) от газоотводной трубки, прикрыв отверстие пальцем. Теперь, если внести слабо горящую спичку в колбу с кислородом, то она ярко вспыхнет!
Получение кислорода возможно также с помощью натриевой или калиевой селитры (соответствующие соли натрия и калия азотной кислоты).
(Нитраты калия и натрия – они же – селитры, продаются на магазинах для удобрений).
Итак, для получения кислорода из селитры возьмём пробирку из тугоплавкого стекла на штативе, поместим туда селитровый порошок (5 грамм будет достаточно).Потребуется под пробирку поставить керамическую чашечку с песком, та как стекло может расплавиться от температуры и потечь. Следовательно, горелку надо будет держать немного сбоку, а пробирку с селитрой – под наклоном.
При сильном нагреве селитры она начинает плавиться, при этом выделяется кислород. Реакция проходит так:
Образующееся вещество – нитрит калия (или натрия, смотря, какая селитра использована) – соль азотистой кислоты.
Ещё один способ получения кислорода – использовать перекись водорода. Пероксид, гидроперит – всё одно и то же вещество. Перекись водорода продаётся в таблетках и в виде растворов (3%, 5%, 10%), которое можно приобрести в аптеке.
В отличии от предыдущих веществ, селитр или марганцовки, перекись водорода – неустойчивое вещество. Уже при наличии света она начинает распадаться на кислород и воду. Поэтому в аптеках перекись продаётся в пузырьках из тёмного стекла.
Кроме того, быстрому разложению перекиси водорода на воду и кислород способствуют катализаторы, например, оксид марганца, активированный уголь, стальной порошок (мелкая стружка) и даже слюна. Поэтому, перекись водорода нагревать не нужно, достаточно катализатора!














ну, слава Богу, стихами заговорил. А то я уж подумал, всё, ускакал Пегас






учебник химии попал


учебник химии попал


учебник химии попал
на буккроссинге у гоголевки подобрал




Все эти способы получения кислорода,которые накопипастил здесь Сова,давно известны и очень энергозатратны.Применяются только в лабораторных условиях для демонстрации свойств кислорода.Цеолиты же как молекулярные сита начали широко использоваться в 21 веке.По затратам энергии на получение литра кислорода непосредственно из воздуха,отделяя азот,этот способ выгоднее чем традиционный(сжижение воздуха и разделение его на кислородных станциях).И самое главное преимущество-непосредственное получение в местах использования-медицина,техника,технологии.


. в далёкие 60-е некоторые продвинутые студенты дома ЛСД получали.
Теперь вишь ли кислород. А водород куда бкдете отводить ? А ведь в смеси с воздухом взрывоопасен.
Не пытайтесь повторить. Довольствуйтесь собственным метаном.


конформист: . в далёкие 60-е некоторые продвинутые студенты дома ЛСД получали.
Теперь вишь ли кислород. А водород куда бкдете отводить ? А ведь в смеси с воздухом взрывоопасен.
Не пытайтесь повторить. Довольствуйтесь собственным метаном.
Ты имеешь в виду разложение воды электролизом,которое предлагает Сова?Конечно образуется.Но он об этом и не задумывался.




Эти цеолиты раньше продавали за копейки как наполнитель фильтров для очистки воды, кажется ручеек назывался.
Где то в гараже валяется, если не потерян при переезде.


Папа: Эти цеолиты раньше продавали за копейки как наполнитель фильтров для очистки воды, кажется ручеек назывался.
Где то в гараже валяется, если не потерян при переезде.


Участвовать в голосованиях и оставлять комментарии могут только авторизованные пользователи.
Если Вы еще не проходили процедуру регистрации - зарегистрируйтесь
Надежная подача промышленного кислорода важна во многих отраслях промышленности. Чистый кислород необходим для поддержания дыхания под водой, в шахтах, для работы аппаратов ИВЛ, пожарным. Его используют в машиностроении, металлургии, для резки и плавки металлов, косметологии, стекольном производстве, сжигания топлива и во многих других сферах.
В промышленных целях чистый кислород вырабатывают тремя разными способами, каждый из которых имеет свои особенности.
Таблица 1. Промышленные способы получения газообразного кислорода:
- Маслые расходы электроэнергии
- Отсутствие постоянного контроля над выработкой кислорода
- Получение кислорода высокой степени очистки (до 95%) с количеством примесей не более 10%
- Высокая производительность
- Большой ресурс оборудования
- Не требуется контроль со стороны оператора
- Большой ресурс оборудования
- Компактные габариты и небольшой вес агрегата
- Экономия электроэнергии
- Незначительные расходы на эксплуатацию
- Чистота кислорода в пределах 45%
- Чистота кислорода – до 99,9%
- Подходит для предприятий с большим расходом кислорода (более 1000 м³/ч)
- Возможность получения кислорода в жидком и газообразном состоянии
Чем генератор кислорода отличается от кислородного концентратора?
Генератор кислорода – аппарат для получения кислорода в газообразном состоянии из атмосферного воздуха. Данные устройства производят кислород чистотой до 95% для технологических процессов, требующих газ в больших объемах и на постоянной основе.
Концентратор кислорода – устройство для выделения молекул кислорода из атмосферного воздуха, концентрации их и подаче в виде потока. Принцип работы аппарата основан на пропускании воздушной струи через молекулярное сито, разделении молекул азота и кислорода в разные баллоны. Концентрация кислорода в таком оборудовании достигает 95%. Концентраторы кислорода используют для выработки кислорода в небольших объемах, и применения его в бытовых/медицинских целях или для технологических процессов, где кислород необходим в малых объемах. Рабочее давление таких аппаратов в среднем составляет 0,5 бар, производительность – до 5 л/мин.
Что представляет собой короткоцикловая безнагревная адсорбция?
- Экономия средств на покупку, заправку и доставку баллонов газа от сторонних организаций,
- Исключение риска остановки технологического процесса из-за нехватки или отсутствия кислорода,
- Исключение простоев в работе из-за прерывания технологических процессов,
- Производство кислорода требуемой степени чистоты и в требуемых объемах,
- Снижение расходов на эксплуатацию генераторов.
Технология напорной короткоцикловой адсорбции (Pressure Swing Adsorbrion (PSA)) базируется на разделении молекул газов из поступающего атмосферного воздуха путем чередования двух процессов – адсорбции и десорбции. В Адсорбер №1 подается воздушная смесь, где под высоким давлением адсорбенты удерживают молекулы азота в молекулярном сите с развитой микропористой структурой, в то время как молекулы кислорода и неадсорбируемые/малоадсорбируемые молекулы других газов отводятся через клапан в специальный резервуар. В Адсорбере №2 происходит фаза регенерации, при которой путем сброса давления с поверхности адсорбентов удаляются поглощенные компоненты.

Рисунок 1. Схема работы установки короткоцикловой безнагревной адсорбции:
Производительность адсорбционных генераторов кислорода варьируется от нескольких литров в минуту до сотен кубических метров в час.
Другие отличия безнагревной PSA:
- Фазы адсорбции и регенерации адсорбента происходят в одном и том же температурном режиме, при этом парциальное давление при десорбции ниже, чем при адсорбции.
- Отсутствие стадий нагрева и охлаждения адсорбирующих компонентов приводит к экономии времени и энергии,
- Быстрый запуск циклов, быстрая остановка процесса по сравнению с криогенным оборудованием,
- Автоматическое регулирование процесса генерации кислорода,
- Невысокие энергетические затраты,
- Длительный срок эксплуатации адсорбентов, за счет регенерации менять адсорбирующие компоненты нужно не чаще 1 раза в 5 лет,
- Невысокая стоимость установок по сравнению с криогенными технологиями.
Пример типовой компоновки адсорбционной кислородной установки:
где: 1 - Компрессор воздушный, 2 - Осушитель, 3 - Ресивер воздушный, 4 - Фильтр, 5 - Генератор кислорода, 6 - Ресивер азотный
Преимущества собственного производства кислорода на оборудовании короткоцикловой адсорбции
Собственное производство кислорода на месте обладает множеством преимуществ по сравнению с заказом баллонов у сторонних организаций: от снижения затрат до постоянной готовности генераторов к работе.
При газовой сварке и резке нагрев металла осуществляется высокотемпературным газовым пламенем, получаемым при сжигании горючего газа или паров жидкости в смеси с технически чистым кислородом.
Кислород является самым распространенным элементом на земле, встречающимся в виде химических соединений с различными веществами: в земле - до 50% по массе, в соединении с водородом в воде - около 86% по массе и в воздухе - до 21% по объему и 23% по массе.
Кислород при нормальных условиях (температура 20°С, давление 0,1 МПа) - это бесцветный, негорючий газ, немного тяжелее воздуха, не имеющий запаха, но активно поддерживающий горение. При нормальном атмосферном давлении и температуре 0°С масса 1 м 3 кислорода равна 1,43 кг, а при температуре 20°С и нормальном атмосферном давлении - 1,33 кг.
Кислород имеет высокую химическую активность, образуя соединения со всеми химическими элементами, кроме инертных газов (аргона, гелия, ксенона, криптона и неона). Реакции соединения с кислородом протекают с выделением большого количества теплоты, т. е. носят экзотермический характер.
При соприкосновении сжатого газообразного кислорода с органическими веществами, маслами, жирами, угольной пылью, горючими пластмассами может произойти их самовоспламенение в результате выделения теплоты при быстром сжатии кислорода, трении и ударе твердых частиц о металл, а также электростатического искрового разряда. Поэтому при использовании кислорода необходимо тщательно следить за тем, чтобы он не находился в контакте с легковоспламеняющимися и горючими веществами.
Всю кислородную аппаратуру, кислородопроводы и баллоны необходимо тщательно обезжиривать. Кислород способен образовывать в широких пределах взрывчатые смеси с горючими газами или парами жидких горючих, что также может привести к взрывам при наличии открытого огня или даже искры.
Отмеченные особенности кислорода следует всегда иметь в виду при использовании его в процессах газопламенной обработки.
Атмосферный воздух в основном представляет собой механическую смесь трех газов при следующем их объемном содержании: азота - 78,08%, кислорода - 20,95%, аргона-0,94%, остальное - углекислый газ, водород, закись азота и др. Кислород получают разделением воздуха на кислород и азот методом глубокого охлаждения (сжижения), попутно идет отделение аргона, применение которого при аргонодуговой сварке непрерывно возрастает. Азот применяют как защитный газ при сварке меди.
Кислород можно получать химическим способом или электролизом воды. Химические способы малопроизводительны и неэкономичны. При электролизе воды постоянным током кислород получают как побочный продукт при производстве чистого водорода.
В промышленности кислород получают из атмосферного воздуха методом глубокого охлаждения и ректификации. В установках для получения кислорода и азота из воздуха последний очищают от вредных примесей, сжимают в компрессоре до соответствующего давления холодильного цикла 0,6-20 МПа и охлаждают в теплообменниках до температуры сжижения, разница в температурах сжижения кислорода и азота составляет 13°С, что достаточно для их полного разделения в жидкой фазе.
Жидкий чистый кислород накапливается в воздухоразделительном аппарате, испаряется и собирается в газгольдере, откуда компрессором его накачивают в баллоны под давлением до 20 МПа.
Технический кислород транспортируют также по трубопроводу. Давление кислорода, транспортируемого по трубопроводу, должно быть согласовано между изготовителем и потребителем. К месту сварки кислород доставляется в кислородных баллонах, и в жидком виде - в специальных сосудах с хорошей теплоизоляцией.
Для превращения жидкого кислорода в газ используют газификаторы или насосы с испарителями для жидкого кислорода. При нормальном атмосферном давлении и температуре 20°С 1 дм 3 жидкого кислорода при испарении дает 860 дм 3 газообразного. Поэтому доставлять кислород к месту сварки целесообразно в жидком состоянии, так как при этом в 10 раз уменьшается масса тары, что позволяет экономить металл на изготовление баллонов, уменьшать расходы на транспортировку и хранение баллонов.
Для сварки и резки по ГОСТ 5583-78 технический кислород выпускается трех сортов:
- 1-й - чистотой не менее 99,7%
- 2-й - не менее 99,5%
- 3-й - не менее 99,2% по объему
Чистота кислорода имеет большое значение для кислородной резки. Чем меньше содержится в нем газовых примесей, тем выше скорость реза, чище кромки и меньше расход кислорода.
Читайте также:

