Оригами молекула воды
Добавил пользователь Евгений Кузнецов Обновлено: 19.09.2024
Такая же как и покупная, 1 в 1.
Касательно остальных двух - не знаю, никогда их не тестила. Но, думаю, раз получилась 1я, то и остальные 2 так же должны быть не хуже оригинала)
Цена вопроса вообще смешная и бросовая.
За почти 150 мл 3х Молекул на все про все я потратила 330 грн.
На Мейкапе это вышло бы около 2400 грн, про Брокард вообще молчу.
Экспериментом довольна. Завтра буду тестить Молекулу 2, а через 3-4 недели Молекулу 3 (ей надо постоять).
Делаются элементарно.
- Комментариев: 97
- Благодарочка 10
Мнения, высказанные в этой теме, передают взгляды авторов и не обязательно отражают позицию администрации

Химия, изложенная скучным научным языком, вряд ли заинтересует школьника. А вот если подключить наглядные пособия, обучение пойдет веселее. Еще интереснее изготовить макет своими руками. В статье расскажем, как с помощью пластилина можно сделать модель молекулы. Для познавательного урока подойдет структура любой молекулы: железа, спирта, углекислого газа. Подробнее остановимся на нескольких вариантах. Модели остальных веществ будут выполняться по тем же правилам: атомы лепим из пластилина, а для структурных связей используем зубочистки или спички.


Что необходимо?
Прежде чем приступать к уроку лепки, а заодно и химии, необходимо подготовить следующие материалы:
- пластилин нескольких оттенков;
- зубочистки или спички;
- доску или клеенку для работы с пластилином;
- формулы молекул, взятые из интернета или учебника химии.
Когда все будет готово, можно приступать к изготовлению молекулярной модели любого вещества.


Как слепить разные модели?
Лучше сразу лепить по схеме модель молекулы конкретного вещества, чем начинать объяснения о микрообъектах абстрактных изделий. Сначала расскажем о структурных связях элементов на примере разных веществ: метана, этана, этилена, метилена.
Для наглядности будем видоизменять каждую изготовленную молекулу, выстраивая из нее схему следующей познавательной модели. Это несложно сделать, так как во всех схемах участвует связь углерода и водорода.
Метан
Сначала возьмем за основу простую молекулу природного газа метана, она имеет формулу СН4. Чтобы изготовить соответствующую модель, скатайте из пластилина синего цвета четыре небольших шарика: они будут представлять водород. Затем подготовьте красный шарик, размером в несколько раз крупнее синих, – углерод. Структурные связи выполняйте спичками, присоединив к углероду 4 водорода. Получилась простейшая модель молекулы метана.


Органическое соединение этана С2Н6 в схематическом варианте выглядит сложнее метана, но конструктивно модель выполняется из тех же пластилиновых деталей и спичек, поэтому изготовить ее не составит труда.
Из скульптурной фигурки метана уберите одну спичку с синим элементом. В результате остается углерод с двумя водородными связями. Для образования этана нам понадобится два таких комплекта. Связав их между собой дополнительной спичкой, мы получим соединение этана.


Этилен
Чтобы составить модель этилена, делаем структуру с двойной связью. Для этого из конструкции этана убираем от каждого красного шара по одной спичке с синими элементами и добавляем еще одну соединительную спичку между углеродными шариками. Вот что у нас получилось.

Метилен
Теперь на примере метилена (СН2) поучимся делать цепочку связей. Для этого скатайте 3 шарика одинаковых размеров: один красный (углерод) и 2 синих (водород).
Составляем молекулу метилена с двойной связью, собирая цепочку по следующей схеме: водород-углерод-водород, то есть синий шар соединяем двумя спичками с красным и снова двумя спичками с синим шаром. Все элементы выстраиваем в одну линию.

С познавательной целью предлагаем собрать еще ряд молекул разных химических веществ.
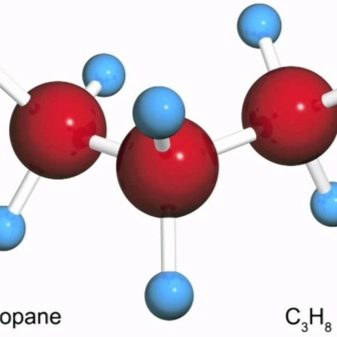
Пропан
Этот газ относится к соединениям, содержащим 3 атома углерода и 8 атомов водорода (С3Р8). Для пространственной модели нужно изготовить из пластилина 3 крупных красных шарика и 8 мелких синих горошин. В качестве соединительных связей нам понадобится 10 спичек. Сборка модели молекулы пропана происходит следующим способом.
- К одному из красных шаров с помощью спичек крепим 3 синих горошины.
- Конструкцию дублируем, так как нам нужны два одинаковых варианта.
- К оставшемуся третьему красному шару добавляем две синих горошины, закрепленных на спичках.
- Теперь все три части соединяем вместе. В центре должен находиться атом углерода с двумя атомами водорода, а по краям у каждого углерода должно быть по 3 атома водорода.
Тип связей, который отвечает за структуру молекулы пропана, такой же, как и у газов бутана, метана.

Аммиак
Представляет собой неорганическое бинарное соединение азота и водорода (NH3). Аммиак – газ, не имеющий цвета, но легко распознаваемый по характерному запаху. В предыдущих моделях мы использовали для лепки атома водорода синий пластилин, а для углерода – красный. Моделируя молекулу аммиака, также воспользуйтесь синим цветом для трех атомов водорода, то есть слепите 3 синих шарика.
Для азота выберите какой-либо другой цвет, например, желтый. Понадобится один шарик такого оттенка. Теперь с помощью спичек к азоту (желтый шар) присоедините 3 водорода (синие шары). Модель аммиака готова.


Этот галоген широко распространен в окружающем мире. Молекулярное строение газа крайне простое, оно содержит всего два атома (Cl2). Хлор тяжелее воздуха, имеет зеленовато-желтый оттенок и токсичный резкий запах.
Изобразить его молекулы несложно. Нужно вылепить из пластилина два зеленых шара и соединить их одной спичкой. Еще более простой способ – присоединить два шара боками друг к другу, не прибегая к помощи спичек или зубочисток.

Сложное вещество, представленное в природе разными вариантами, например, хлорид натрия (NaCl), сульфат кальция (CaSo4). NaCl еще называют поваренной солью, с ней знаком каждый из нас, так как она является пищевой.
Для изготовления соединения поваренной соли делаем два шара: небольшой зеленый (хлор) и крупный коричневый (натрий). Чтобы они стали единой молекулой, достаточно прижать шары друг к другу, но можно воспользоваться и спичкой, символизирующей соединительные связи.

Полезные советы
Современные родители и без советов знают, как развивать своих детей, но мы все же озвучим несколько рекомендаций.
Если хотите донести до школьника сложную информацию, находите нестандартные пути ее подачи. В нашем случае обучение химии происходит через 3D-моделирование. Полезные моменты заключаются в следующем.
- Дети усваивают новые знания.
- Способ получения информации сопровождается творческим процессом ваяния объемных фигурок. Он увлекает и дает возможность ученику заинтересоваться таким сложным предметом, как химия.
- Работа с пластилином развивает моторику рук, поэтому она полезна для мыслительной деятельности и творческого потенциала.
- Занятия лепкой помогают в становлении таких полезных качеств, как воображение, усидчивость и сосредоточенность.
Начинайте обучение с простых, но реально существующих моделей молекул. Ребенок сразу должен себя почувствовать причастным к настоящей науке.
Предложите сыну или дочери, пользуясь учебником (интернетом), самостоятельно найти формулы молекул, которые вы еще не проходили. Пусть ребенок с помощью найденной схемы и своего воображения изготовит макет без посторонней помощи. Его может заинтересовать, из каких молекул состоит воздух, кислород, вода, золото, алмаз или сладкий сахар.


Делаем модель молекулы воды из пластилина далее.
Хотела с сыном сделать, но он так занят был: учебный год заканчивался, в музыкалке концерты, конкурсы.
По два раза в день на репетиции ходил!
Но такое вполне с ребенком сделать можно.
Модели молекул.
- пенопластовые шары (диам.6-7 см)
- шарики для пин-понга (можно заменить пенопластовыми такого же диаметра).
- шпажки деревянные (или зубочистки)
Выбрать простенькие модели молекул (например, вода - НОН, метан - СН4 ).
Взять пенопластовые шарики и шарики для пин-понга (настольный теннис).
Покрасить шарики в разные цвета: для каждого вида атомов один цвет.
Например, атомы углерода (С) - синий цвет, атомы водорода (Н) - красный цвет.
Шпажки разломить или разрезать пополам.
Тупые стороны заострить ножом (так будет проще крепить).
В шариках для пин-понга сделать отверстия.
Для этого нагреть шило или гвоздь (брать гвоздь не руками, а плоскогубцами! Иначе можно обжечься!).
Нагреть можно на огне (газовая конфорка, зажигалка, свеча) или на конфорке электроплиты.
Проткнуть аккуратно дырку в шарике. Дырку сделать такого размера, чтобы в неё плотно вошла шпажка или зубочистка.
Нагреть клеевой пистолет.
Нанести немного клея на один конец шпажки и воткнуть шпажку в шар для пин-понга.
Сделать необходимое количество шпажек с шариками (для метана - 4 штуки).
Затем на другой конец шпажки с шариком нанести немного клея
и воткнуть в пенопластовый шар-основу (для метана это будет углерод (С)).
Таким же образом воткнуть остальные шары со шпажками в пенопластовый шар
под определенным углом, чтобы получилась модель соответствующей молекулы (можно посмотреть в интернете, как должна выглядеть).
Следить, чтобы расстояние между пин-понговыми шариками и пенопластовым было одинаковое расстояние.
Можно проявить фантазию и придумать свою молекулу.
Подождать застывания клея.
Подписать атомы контрастной краской.
Можно поставить на полочку, подвесить к потолку или подарить учительнице по химии.
Все разнообразие нашего мира построено из атомов и молекул. Удивительно, как проявления форм жизни образовались лишь на основе протонов, нейтронов и электронов. Элементарная основа позволяет каждому веществу и организму выполнять свою функцию. Так из семи нот пишется музыка разных направлений, разных стилей. Мы собрали 10 самых интересных фактов об атомах и молекулах.

Самый легкий из атомов – атом водорода

В периодической таблице химических элементов водород стоит на первом месте. Его ядро состоит лишь из одного протона, вокруг которого вращается единственный электрон. Простейшее строение определяет минимальную массу, которую может иметь атом – 1,008 а.е.м. или 1,7х10-24 г.
На Земле водород существует в виде соединений с другими веществами или образует двухатомную молекулу Н2. Если считать в массовом отношении, на его долю приходится 1% земной коры. Если перевести массу в количество атомов, то содержание водорода окажется более внушительным – 17%. Этот показатель ставит элемент на второе место после кислорода (52%).
Во Вселенной водород составляет 88,6% от общей доли атомов, находящихся в космосе в виде звездного вещества и космической пыли.
Главной молекулой живой природы является молекула ДНК

В молекуле ДНК сосредоточена информация о строении каждой клетки живого организма, словно это проектное бюро города, где собраны подробные планы всех зданий. Внешне она напоминает перевитую веревочную лестницу, состоящую из двух нитей и соединенную водородными связями. ДНК вирусов может представлять одну цепочку.
Информация зашифрована в генах, то есть участках молекулы. Ген представляет собой определенную последовательность нуклеотидов, способных передать код для построения белков и РНК (информационных, транспортных, рибосомных, матричных).
Спираль ДНК человека, если ее вытянуть, протянется почти на 2 м. Это тем более удивительно, что она умещается в ядре размером меньше микрометра. Свернуться в компактную хромосому молекуле помогают нуклеосомы. На них ДНК наматывается, как на катушку.
Пыль – это частица, состоящая из квадриллиона атомов

Пылью называют твердые минеральные или органические частицы размером не более 0,05 мм. Природа образования может быть как естественной, так и связанной с деятельностью человека (антропогенной). В воздух поднимаются вулканический пепел, морская соль, сухая почва, продукты горения после пожаров, пыльца растений. Человек способствует загрязнению воздуха продуктами отопления и горных разработок, выхлопами автотранспорта, удобрениями. Вспашка земли и оголение почвы выкосами травы опасны выветриванием и переносом верхнего слоя грунта ветром.
Если сравнивать твердую взвесь с газообразными загрязнителями воздуха, то последние присутствуют в виде отдельных молекул. Пыль же в каждой частице содержит огромное число молекул и еще большее число атомов.
Атом может иметь электрический заряд

В составе атома электроны несут отрицательный заряд, протоны – положительный. Нейтроны не имеют заряда, то есть нейтральны. Когда количество протонов равно количеству электронов, заряд атома равен нулю. В случае, если электронов больше или меньше, чем протонов, у атома появляется заряд. Он становится ионом.
Ядро, состоящее из нейтронов и протонов, обладает ощутимой массой. Нужно определенное количество энергии, чтобы заставить его терять протоны. Электроны, которые вращаются вокруг него, значительно легче могут перемещаться от одного атома к другому. Добавление электронов приводит к образованию отрицательного заряда, потеря частиц – положительного. Атомы с положительным зарядом называют катионами, атомы с избытком электронов становятся анионами.
Самый тяжелый из атомов – атом урана

Из природных элементов атом урана имеет самую большую массу – 238,0289 а.е.м. В природе находится в основном в виде изотопа U-238. Атом с его 92 протонами чрезвычайно перегружен, при любой возможности выбрасывает протоны и нейтроны с огромной скоростью.
В конце 19 века во Франции Анри Беккерель обнаружил радиоактивность урана, то есть способность терять частицы. Распад может иметь 14 циклов. Уран превращается в радий, радон и другие элементы, образуя на последней стадии свинец.

Стекло не является твердым телом

Твердость вещества – характеристика, основанная на прочности химических связей между атомами и молекулами. В жидкости частицы могут перемещаться относительно друг друга. В твердых телах они лишены такой возможности.
При производстве стекла молекулы кремния, обычно принимающие структуру кристаллической решетки, не успевают занят положенное им место. Стекло быстро остывает и частицы остаются перемешанными хаотично. Такое вещество называют аморфным, однако все же оно твердое.
Молекула меньше яблока во столько же раз, во сколько яблоко меньше Земли

Чтобы представить видимые и невидимые параметры окружающего мира, представим все молекулы одного кубического сантиметра воздуха в виде кирпичей. Их количества хватило бы для покрытия поверхности планеты на высоту 40-этажного дома.
Размеры молекул и атомов настолько малы, что в решении задач молекулярной физики используют относительные величины. Установить их удалось лишь с изобретением электронного микроскопа. Средний диаметр атома и простейшей молекулы составляет порядка 10-10 м. Так, размер молекулы белка – 43х10-10 м. Крупные молекулы достигают 10-7 м.
В ионный микроскоп можно разглядеть строение кристалла и даже определить межатомные расстояния.
Ученые смогли охладить молекулы монофторида стронция практически до абсолютного нуля

Выбор пал на монофторид стронция (SrF) неслучайно. Принцип охлаждения атомов основан на периодическом повторении поглощения и испускания фотонов под воздействием лазера. Таким образом атом теряет кинетическую энергию. Молекулы не настолько чувствительны. Мешает колебательная и вращательная энергия межатомных связей. У фторида стронция эти явления минимальны.
Группа ученых Йельского университета во главе с Д. Демиллем добилась охлаждения молекулы до 300 мкК (0,0003 К). За счет подобранной длины волны лазер погасил вращательные межатомные движения. В дальнейшем молекулы вели себя аналогично атому.
Практически такое достижение в перспективе можно использовать в квантовых компьютерах.
Скорость движения молекул воды может достигать 650 м/с

Молекулы воды находятся в постоянном тепловом движении. Они колеблются с большой частотой (одно колебание за 10-12 … 10-13 с) возле определенного положения, изредка прыгая на освободившееся соседнее место. Скорость движения при этом может приближаться к 600-650 м/с.
И все же молекулы не разлетаются, остаются жидкостью. Происходит это за счет водородных связей. В молекуле H2O пары электронов смещены в сторону кислорода. Водород, оставшийся практически без электрона, представляет собой положительно заряженное ядро. В результате протон водорода притягивает соседние атомы кислорода, образуя прочную межмолекулярную связь.
Благодаря такому сцеплению вода в условиях Земли принимает в основном жидкое состояние, а не кипит как аналогичные гидриды (серы, селена) при –80°С. Водородные связи определяют физические и химические свойства воды, на которых основана жизнь на нашей планете.
©


Несмотря на то, что в мире бактерий отсутствует истинная многоклеточность, многие бактерии, в том числе и патогены человека, формируют сложно устроенные сообщества — биопленки. Биопленки покрывают, например, зубы, подводные камни и другие поверхности, на которых могут жить бактерии (а жить они могут почти везде).
Бактерии в биопленке становятся практически неуязвимыми для антибиотиков и других противомикробных агентов, а если речь идет о бактериях, обитающих в организме животного, — то и для иммунной системы хозяина. Дело в том, что матрикс биопленки, окружающий бактериальные клетки, препятствует их непосредственному взаимодействию с антибиотиками. Продолжая аналогию с многоквартирным домом, жильцы которого платят налоги и централизованно оплачивают капитальный ремонт, можно сказать, что бактериальные клетки в составе биопленки, секретируя ее компоненты, поддерживают, таким образом, целостность во всех отношениях выгодного для них сообщества, получая взамен питание и защиту.
Из всех компонентов матрикса бактериальных пленок наиболее загадочным, пожалуй, является входящая в его состав внеклеточная ДНК. Чисто физически двойная спираль ДНК — это довольно жесткая и прочная протяженная молекула, которая, как железный прут, может играть роль опоры для желеобразного матрикса биопленки. Откуда берется внеклеточная ДНК? Оказывается, бактериальные клетки в составе биопленки обмениваются друг с другом сигнальными молекулами (это явление также известно как чувство кворума). Под действием определенных сигналов, испускаемых соседними клетками, часть клеток подвергается добровольной гибели и разрушению — аутолизу. При лизисе клеток их ДНК выходит наружу и остается в матриксе биопленки (L. Montanaro et al., 2011. Extracellular DNA in biofilms).
В биопленках ДНК связана с белками IHF и HU, относящимися к семейству DNABII (см. Bacterial DNA binding protein), которые поддерживают ее двойную спираль. Эксперименты показали, что в отсутствие DNABII биопленка буквально рассыпается, а бактерии, как жильцы разбитого бомбежкой дома, сталкиваются один на один с враждебной окружающей средой и в большинстве своем погибают.
А что будет, если в биопленке не будет ДНК? На самом деле, обработка сформировавшейся биопленки нуклеазами, расщепляющими ДНК, обычно не дает никаких результатов, и помешать формированию биопленки можно, только лишь обработав клетки нуклеазой на самой ранней стадии ее формирования. Почему же ДНК в составе биопленок не расщепляется нуклеазами? Ответу на этот вопрос посвящена недавняя работа, опубликованная в журнале Cell. Авторы исследования пришли к совершенно парадоксальному выводу: в зрелой биопленке большая часть ДНК представлена левозакрученной формой, или Z-ДНК, и потому нуклеазы никак на нее не действуют.
В живых клетках молекулы ДНК могут существовать в нескольких конформациях (рис. 1, см. также Nucleic acid double helix). Основная форма ДНК в клетках — это B-ДНК, и именно ее обычно имеют в виду, когда изображают красивую двойную спираль ДНК с большой и малой бороздками. A-ДНК отличается от B-формы ДНК по ряду геометрических параметров, в живой природе она встречается нечасто. Любопытно, что именно в форме A-ДНК находится ДНК в вирионах ряда вирусов архей, которые не так давно были выделены в отдельный реалм Adnaviria. И B-, и A-формы ДНК закручены вправо. Но в клетках также встречается, хотя и очень редко, левозакрученная форма, Z-ДНК. Как правило, она формируется при связывании специальных белков с последовательностями вида (GC)n.
Z-ДНК отличается от привычной нам B-ДНК не только направлением закрученности цепей, но и множеством других параметров, таких как ориентация азотистых оснований, конформация сахаров и других. И, самое главное, Z-ДНК не разрушается нуклеазами, которые расщепляют B-ДНК! Тем не менее, несмотря на множество геометрических различий, переход одной и той же последовательности из одной формы в ДНК в другую обратим и вполне возможен не только в пробирке при изменении ионной силы и других параметров раствора, но и в живой клетке — например, при связывании упоминавшихся выше специальных белков, которые способствуют изменению конформации ДНК.
Исследователи показали, что Z-ДНК присутствует в биопленках таких патогенных бактерий, как уропатогенная Escherichia coli, Klebsiella pneumoniae и Haemophilus influenza. Выявить наличие Z-ДНК можно с помощью распознающих ее моноклональных антител. Авторы отметили, что в молодых биопленках доля ДНК в B-конформации превосходит таковую для Z-конформации, однако по мере созревания биопленки почти вся правозакрученная ДНК переходит в левозакрученную форму. Ученым удалось даже увидеть Z-ДНК в составе биопленок: она выглядит как толстые волокна (рис. 2).


Рис. 2. Правозакрученная ДНК (голубой) и левозакрученная ДНК (желтый) в биопленках из мокроты пациента с муковисцидозом (слева) и из среднего уха шиншиллы с отитом (справа). Окрашивание с помощью моноклональных антител. Рисунок из обсуждаемой статьи в Cell
Как уже говорилось, Z-ДНК может сформироваться, если склонная к этому последовательность ДНК вида (GC)n будет связана белками, распознающими Z-ДНК. В качестве таких белков могут выступать специфичные по отношению к Z-ДНК моноклональные антитела, которые могут образовываться в организмах млекопитающих и в настоящее время даже коммерчески доступны. И действительно, в ходе проведенного авторами эксперимента обработка моноклональными антителами, специфично связывающими Z-ДНК, ускоряла формирование биопленки, активируя переход правозакрученной ДНК в составе матрикса в левозакрученную форму (рис. 3).

Склонить правозакрученную ДНК к переходу в левозакрученную можно и иным путем. Известно, что формированию Z-ДНК способствует хлорид церия (CeCl3). Хлорид церия связывается с сахарофосфатным остовом ДНК и нейтрализует электростатическое отталкивание между заряженными группами, делая левозакрученную конформацию энергетически выгодной. Обработка биопленок хлоридом церия приводила к их росту и увеличению массы бактериальных клеток в составе биопленки. Таким образом, смещение равновесия между B- и Z-формами ДНК в сторону последней способствует формированию биопленок. Более того, под действием хлорида церия повышался модуль Юнга биопленок, что свидетельствует о том, что увеличение количества Z-ДНК в биопленке повышает ее механическую жесткость.
Левозакрученную ДНК можно перевести в правозакрученную, обработав, например, хлорохином. Это вещество является интеркалятором, то есть внедряется в двойную спираль ДНК. Обработка биопленки хлорохином способствует ее развалу, поскольку под действием этого вещества доля Z-ДНК в биопленке уменьшается, из-за чего ее жесткость снижается. Более того, хлорохин действует на биопленки столь губительно, что бактериальные клетки начинают буквально вываливаться из них! После обработки хлорохином биопленки становятся чувствительными к действию нуклеаз, ведь ДНК переходит в распознаваемую этими ферментами правозакрученную форму.
Каким образом Z-ДНК образуется при естественном формировании биопленки? Ученые показали, что вышеупомянутые белки группы DNABII способствуют переходу правозакрученной ДНК в левозакрученную. Возможность непосредственного взаимодействия DNABII с Z-ДНК пока не доказана и, вероятно, белки DNABII стабилизируют Z-ДНК, не связываясь с ней напрямую. По-видимому, на ранних этапах формирования биопленки, когда в ней преобладает B-форма ДНК и она сохраняет чувствительность к нуклеазам, белки DNABII запускают переход B-ДНК в Z-ДНК.
Авторы исследования отмечают, что образование антител к Z-ДНК в ходе адаптивного иммунного ответа на вторжение бактерий может не только не помешать развитию инфекции, но и способствовать ее переходу в хроническую форму, ведь антитела, связывающие Z-ДНК, стабилизируют ее и, следовательно, укрепляют бактериальные биопленки.
Читайте также:

